
科目: 来源: 题型:
【题目】在同温、同压下,下列三个反应放出的热量分别用a、b、c表示,则a、b、c的关系是( )
2H2(g)+O2(g)===2H2O(g) ΔH=-a kJ·mol-1 ①
2H2(g)+O2(g)===2H2O(l) ΔH=-b kJ·mol-1 ②
H2(g)+1/2O2(g)===H2O(g) ΔH=-c kJ·mol-1 ③
A.a>b, b=2cB.a=b=cC.a<b,c=a/2D.无法比较
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学利用下图所示的实验装置进行铁跟水蒸气反应的实验,并继续研究铁及其化合物的部分性质。

请回答下列问题。
(1)硬质试管中发生的化学方程式___________________。
(2)该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色,则说明硬质试管中固体物质一定有_________,可能有_________(填写“化学式”),若溶液未变红色,则说明硬质试管中固体物质的成分是___________________(填写“化学式”)。

(3)该同学按上述实验方案进行了实验,结果溶液未变红色,原因是:______(用离子方程式表示)。
(4)该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出与上述白色沉淀变成红褐色的反应的化学方程式____________________________。
(5)一段时间后,该同学发现(3)中未变红的溶液变成红色,说明Fe2+具有_____性。由此可知,实验室中含Fe2+的盐溶液现用现配制的原因是_________,并且配制含Fe2+的盐溶液时应加入少量_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】亚硝酰硫酸(NOSO4H)纯品为棱形结晶,溶于硫酸,遇水易分解,常用于制染料。SO2和浓硝酸在浓硫酸存在时可制备NOSO4H,反应原理为:SO2+HNO3=SO3+HNO2、SO3+HNO2=NOSO4H。
(1)亚硝酰硫酸(NOSO4H)的制备。
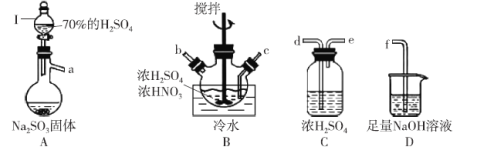
①打开分液漏斗I中的旋塞后发现液体不下滴,可能的原因是_______。
②按气流从左到右的顺序,上述仪器的连接顺序为_______ (填仪器接口字母,部分仪器可重复使用)。
③A中反应的方程式为_______。
④B中“冷水”的温度一般控制在20°C,温度不易过高或过低的原因为_______。
(2)亚硝酰硫酸(NOSO4H)纯度的测定。称取1.500g产品放入250 mL的碘量瓶中,并加入100.00 mL浓度为0.1000 mol·L-1的KMnO4标准溶液和10 mL25%的H2SO4,摇匀;用0.5000 mol·L-1 Na2C2O4标准溶液滴定,滴定前读数1.02 mL,到达滴定终点时读数为31.02 mL。
已知:
i.__KMnO4+__NOSO4H+__=__K2SO4+__MnSO4+__HNO3+__H2SO4
ii.2KMnO4+5Na2C2O4+8H2SO4=2MnSO4+10CO2↑+8H2O
①完成反应i的化学方程式:_______KMnO4+_______NOSO4H+_______=_______K2SO4+_______MnSO4+_______HNO3+_______H2SO4
②滴定终点的现象为_______。
③产品的纯度为_______。(保留3位有效数字)
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)除去NaCO3粉末中混入的NaHCO3杂质用__________方法,化学方程式为____。
(2)除去氧化铜粉末中混入的氧化铝粉末通常用________试剂,离子方程式为________。
(3)通常用________试剂除去CO2中的HCl气体,离子方程式为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上用铝土矿(主要成分为Al2O3,含Fe2O3等杂质)为原料冶炼铝的工艺流程如下:
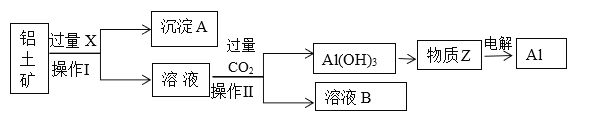
已知:2Al2O3![]() 4Al+3O2↑。
4Al+3O2↑。
(1)操作Ⅱ的名称___________,用到的玻璃仪器有_______________。
(2)X是___________,操作Ⅱ通入过量CO2的离子方程式:______________________________________。
(3)沉淀A的主要成分是________,在生活中有什么应用:________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】目前,处理烟气中 SO2 常采用两种方法:碱液吸收法和水煤气还原法。
Ⅰ.碱液吸收法
25℃时,Kb(NH3·H2O)=1.8×10-5;H2SO3:Ka1=1.5×10-2,Ka2=1.0×10-7;Ksp(CaSO4)=7.1×10-5。
第1步:用过量的浓氨水吸收 SO2,并在空气中氧化;
第2步:加入石灰水,发生反应 Ca2++2OH-+2NH4++SO42-CaSO4↓+2NH3·H2O K。
(1)25℃时,0.1 mol·L-1(NH4)2SO3 溶液的 pH_____(填“>”“<”或“=”)7。
(2)计算第2步中反应的 K=_____。
Ⅱ.水煤气还原法
已知:①2CO(g)+SO2(g)=S(l)+2CO2(g) ΔH1=-37.0 kJ·mol-1
②2H2(g)+SO2(g)=S(l)+2H2O(g) ΔH2=+45.4 kJ·mol-1
③CO 的燃烧热ΔH3=-283 kJ·mol-1
(3)表示液态硫(S)的燃烧热的热化学方程式为_________。
(4)反应②中,正反应活化能 E1_____(填“>”“<”或“=”)ΔH2。
(5)在一定压强下,发生反应①。平衡时SO2的转化率α(SO2)与投料比的比值[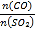 =y]、温度 T 的关系如图所示。
=y]、温度 T 的关系如图所示。
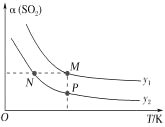
比较平衡时CO的转化率α(CO):N_____M。逆反应速率:N_____P(填“>”“<”或“=”)。
(6)某温度下,向10L恒容密闭容器中充入2molH2、2 molCO和2molSO2发生反应①、②,第5min时达到平衡,测得混合气体中CO2、H2O(g)的物质的量分别为1.6 mol、1.8 mol。
①该温度下,反应②的平衡常数K为_____。
②其他条件不变,在第 7 min 时缩小容器体积,SO2的平衡浓度_____(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,向50 mL饱和CuCl溶液中缓慢加入NaI固体并搅拌,溶液中c(I-)与c(Cu+)的变化曲线如图所示,已知:Ksp(CuI)=1.0×10-12,下列说法正确的是
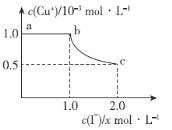
A.Ksp(CuCl)=1.0×10-9
B.图示中的x为10-6
C.向CuI饱和溶液中加入淀粉会出现蓝色
D.曲线bc段内,c(Cl-):c(I-)=106
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,两圆圈相交的部分表示圆圈内的物质相互发生的反应。已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g。下列说法正确的是( )
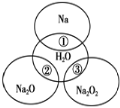
A.反应③最多能产生0.05molO2
B.反应①的离子方程式为Na+2H2O=Na++2OH-+H2↑
C.①、②、③都属于氧化还原反应
D.①、②、③充分反应后所得溶液中溶质的质量分数:①>②>③
查看答案和解析>>
科目: 来源: 题型:
【题目】利用膜技术原理和电化学原理制备少量硫酸和绿色硝化剂N2O5,装置如图所示,下列说法不正确的是

A. 电极a和电极c都发生氧化反应
B. 电极d的电极反应式为2H++2e-=H2↑
C. c电极上的电极反应式为N2O4-2e-+H2O=N2O5+2H+
D. 装置A中每消耗64gSO2,理论上装置A和装置B中均有2moH+通过质子交换膜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com