
科目: 来源: 题型:
【题目】某实验小组推测,某无色溶液中可能含有以下离子:K+、Al3+、Mg2+、Cu2+、NH4+、Cl-、CO32-、SO42-,进行如下实验:
①取适量该溶液,加入过量NaOH溶液后加热,产生使湿润的红色石蕊试纸变蓝色的气体,并得到澄清溶液。
②在①所得溶液中通入过量CO2,生成白色沉淀。
③另取原溶液于试管中,加足量BaCl2溶液后,得白色沉淀,再加稀盐酸,沉淀不溶解。
根据上述实验回答:
(1)写出①中反应生成气体的离子方程式_______________________________。
(2)该溶液中一定存在的离子有_____________,不能确定是否存在的离子有___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】举世闻名的侯氏制碱法的工艺流程如下图所示,下列说法正确的是
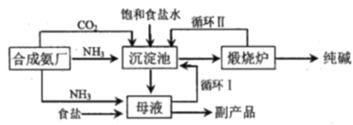
A.往母液中加入食盐的主要目的是使NaHCO3更多的析出
B.从母液中经过循环Ⅰ进入沉淀池的主要是Na2CO3、NH4Cl和氨水
C.沉淀池中反应的化学方程式:2NH3+CO2+2NaCl+H2O=2NH4Cl+Na2CO3
D.设计循环Ⅱ的目的是使原料二氧化碳利用率大大提升
查看答案和解析>>
科目: 来源: 题型:
【题目】某手机电池采用了石墨烯电池,可充电5分钟,通话2小时。一种石墨烯锂硫电池(2Li+S8=Li2S8)工作原理示意图如图。下列有关该电池说法正确的是
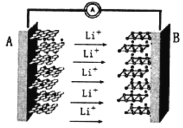
A.A电极为该电源的负极,电极材料主要是金属锂和石墨烯
B.B电极的反应:2Li++S8﹣2e=Li2S8
C.充电时,电极A与电源负极连接,作为阴极
D.为提高电池效率,该电池可选用稀硫酸作为电解质
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上电解制碱的技术是用阳离子交换膜法,主要原料是饱和食盐水。图一为阳离子交换膜法电解原理示意图。请回答下列问题:
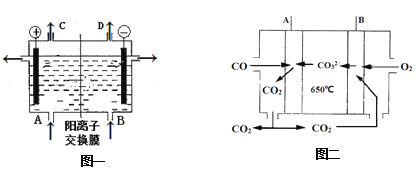
(1)反应的离子方程式是___。A、B、C、D所对应物质化学式分别为__________、____、______、_______,每通过0.1mol电子,就有0.1mol____(填离子符号)通过离子交换膜。
(2)若上述电解过程中用阴离子交换膜代替阳离子交换膜(已知:3Cl2 +6OH- = 5Cl-+ClO3-+3H2O),下列说法正确的组合是___________。
A.电解结束时,右侧溶液中含有ClO3—
B.电解槽内发生反应的总化学方程式为:NaCl + 3H2O ![]() NaClO3 + 3H2↑
NaClO3 + 3H2↑
C.用阴离子交换膜后,电解槽内两个电极发生的电极反应与原来一样
D.用阴离子交换膜后,阳离子的定向移动方向与原来相反
(3)如果用熔融碳酸盐CO燃料电池供电,图二为其工作原理,A、B极的电极反应分别是____、_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用有机含碘![]() 主要以I2和IO3-的形式存在
主要以I2和IO3-的形式存在![]() 废水制备单质碘的实验流程如下:
废水制备单质碘的实验流程如下:

已知:Ⅰ.碘的熔点为113℃,但固态的碘可以不经过熔化直接升华;
Ⅱ.粗碘中含有少量的硫酸钠杂质。
下列说法正确的是( )
A.操作②中发生反应的离子方程式为IO3-+3SO32-=I-+3SO42-
B.操作①和③中的有机相从分液漏斗上端倒出
C.操作④为过滤
D.操作⑤可用如图所示的水浴装置进行

查看答案和解析>>
科目: 来源: 题型:
【题目】金晶体的最小重复单元(也称晶胞)是面心立方体,即在立方体的8个顶点各有一个金原子,各个面的中心有一个金原子,每个金原子被相邻的晶胞共用。金原子的直径为dcm,用NA表示阿伏加德罗常数,M表示金的摩尔质量(单位:g·mol-1)。
(1)金晶体每个晶胞中含有________个金原子。
(2)欲计算一个晶胞的体积,除假定金原子是刚性小球外,还应假定_________。
(3)一个晶胞的体积为________cm3。
(4)金晶体的密度为________g·cm-3。
查看答案和解析>>
科目: 来源: 题型:
【题目】用X射线研究某金属晶体,测得在边长为360 pm的立方晶胞中含有4个金属原子,此时金属的密度为9.0 g/cm3。试回答下列问题:
(1)此金属晶胞属于哪一种类型?_______
(2)求每个晶胞的质量。_______
(3)求此金属的相对原子质量。_______
(4)求此金属原子的原子半径(pm)。_______
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A是一种淡黄色固体,可做供氧剂,C为具有磁性的黑色晶体,E的焰色反应为黄色,F为红褐色固体(部分产物已略去)。
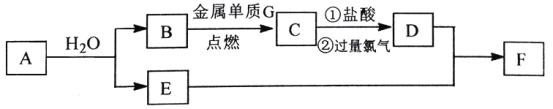
(1)物质A、F的化学式分别是_____________、_____________。
(2)C→D的过程中第②步反应的离子方程式是____________________________________。
(3)如何检验D中的金属阳离子,说明具体的操作和实验现象________________________。
(4)E溶液与地壳中含量最多的金属元素的单质发生反应的化学方程式为______________。
(5)G与D溶液也能发生反应,其反应的类型为___________________(填序号)。
a.化合反应 b.置换反应 c.复分解反应 d.氧化还原反应
查看答案和解析>>
科目: 来源: 题型:
【题目】有碳酸钠、碳酸氢钠的混合物19.0g,把它们加热到质量不再减轻,冷却后称量为15.9g。求:
(1)原混合物中碳酸钠的质量分数_________。(写出计算过程,结果保留3位有效数字)
(2)将原混合物19.0g完全溶解于蒸馏水水中,配成500mL溶液,则其中钠离子物质的量浓度为______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,关于pH=11的NH3·H2O溶液,下列分析正确的是
A.c(NH3·H2O)=103mol·L1
B.加入少量水,溶液中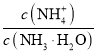 增大
增大
C.由水电离产生的c(OH)=1×1011mol·L1
D.加入等体积pH=3的盐酸,所得溶液:c(Cl)>c(NH4+)>c(H+)>c(OH)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com