
科目: 来源: 题型:
【题目】常温下,向0. 1 mol L-1 H2 A溶液中缓慢加入氢氧化钠(假设溶液体积不变),得到有关粒子的物质的量浓度分数与溶液pH值关系如图所示(M、N点对应的横坐标为6. 4和10.2)。 [![]() ]下列说法正确的是
]下列说法正确的是

A.Ka1(H2A)的数量级为10-5
B.N 点溶液中 c(Na+)>3c(HA-)
C.当溶液呈中性时,c(HA-)=c(Na+) >c(OH-)=c(H+)
D.由图可知HA-的水解程度小于电离程度
查看答案和解析>>
科目: 来源: 题型:
【题目】硫铁矿烧渣(主要成分Fe2O3、Fe3O4、FeO、SiO2等)是工业生产硫酸的废渣,利用硫铁矿烧渣制备铁红等产品的流程如下图所示:
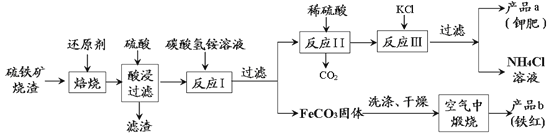
(1)硫铁矿烧渣焙烧时所添加的还原剂最有可能的是______。
A.铝 B.锌 C.碳
(2)酸浸、过滤后滤液中的主要成分是________。滤渣是__________。
(3)反应Ⅰ的溶液为防止被氧化,需加___________,其离子方程式为__________________。
(4)反应Ⅰ的反应温度一般需控制在15℃以下,其目的是____________________。
(5)空气中煅烧FeCO3生成产品b的化学反应方程式为_____________________。
(6)检验产品a中是否含有氯化物杂质的实验操作是:取少量产品a于试管中配成溶液,___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】镁能在二氧化碳中燃烧:2Mg+CO2![]() 2MgO+C,钠比镁更活泼,那么钠能在二氧化碳中燃烧吗?某研究性学习小组设计了如图装置进行探究。
2MgO+C,钠比镁更活泼,那么钠能在二氧化碳中燃烧吗?某研究性学习小组设计了如图装置进行探究。
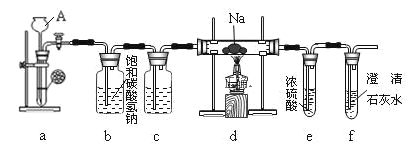
请回答下列问题:
(1)装置a中发生的是实验室制CO2的反应,反应方程式为___。
(2)装置b中发生反应的离子方程式为___,装置c的作用为___。
(3)实验过程中,在点燃d装置中的酒精灯前,必须经过必要的操作方可进行后续的实验,该必要的操作是___。
(4)实验发现钠在充满二氧化碳气体的玻璃管里剧烈地燃烧,产生大量的白烟并伴有黑色物质生成。取一部分生成物于试管中,往试管中加水,白色物质溶解于水,黑色物质不溶。过滤,得到澄清的滤液。往所得滤液中加澄清石灰水,溶液变浑浊。再滴入稀盐酸, 溶液中有气泡出现。试写出钠与二氧化碳反应的化学方程式:___。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室需配制80mL0.1mol/L的碳酸钠溶液,填空并回答下列问题:
(1)配制80mL1.0mol/L的Na2CO3溶液。
实际应称Na2CO3质量/g | 应选用容量瓶的规格/mL |
___ | ___ |
(2)配制时,其正确的操作顺序为___(用字母表示,每个字母只能用一次)。
A.将准确称量的Na2CO3固体倒入烧杯中,再加适量水溶解
B.将容量瓶盖紧,上下颠倒,摇匀
C.将已冷却的溶液沿玻璃棒注入容量瓶中
D.用30 mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
E.继续往容量瓶内小心加水,直到液面接近刻度线1~2cm处
F.改为胶头滴管加水,使溶液凹液面恰好与刻度线相切
(3)若出现如下情况,对所配溶液浓度将有何影响?(填“偏高”“偏低”或“无影响”)
若定容时仰视刻度线,结果会___;
若容量瓶中有少量蒸馏水,结果会___。
查看答案和解析>>
科目: 来源: 题型:
【题目】接触法制硫酸的三个阶段:煅烧、氧化、吸收。煅烧黄铁矿的化学方程式为:
4FeS2 + 11O2 → 2Fe2O3 + 8SO2。
完成下列填空:
(1)煅烧黄铁矿在________(填设备名称)中进行,此反应中被氧化的元素是___________。
(2)SO2的催化氧化:2SO2(g)+O2(g)![]() 2SO3(g),该反应的平衡常数表达式为K= ______;反应达到平衡,及时分离出SO3,则平衡向_________方向移动(选填“正反应”“逆反应”)。其他条件不变,降低温度平衡向正反应方向移动,则正反应为__________反应(选填“吸热”“放热”)。
2SO3(g),该反应的平衡常数表达式为K= ______;反应达到平衡,及时分离出SO3,则平衡向_________方向移动(选填“正反应”“逆反应”)。其他条件不变,降低温度平衡向正反应方向移动,则正反应为__________反应(选填“吸热”“放热”)。
(3)下图为二氧化硫与氧气反应的速率(ν)与时间(t)的关系,判断在t1时刻曲线发生变化的原因是______(选填编号)。

a. 增大O2的浓度
b. 扩大容器体积
c. 加入催化剂
d. 升高温度
改变条件后,平衡混合物中SO3的百分含量_______(选填“增大”“减小”“不变”)。
(4)SO3的吸收:SO3 + H2O → H2SO4 。假定制备硫酸的整个过程中S元素共损失10%,则含1000 kg FeS2的黄铁矿可以制得98%的浓硫酸_____________kg。
查看答案和解析>>
科目: 来源: 题型:
【题目】四种短同期主族元素X、Y、Z、W的原子序数依次增大。Z的简单离子半径在同周期中最小,25 ℃时, 0.01 molL 1 X、W的最高价氧化物对应的水化物溶液的pH和原子半径的关系如图所示,Y和W 同主族。下列说法错误的是 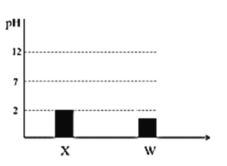
A.原子半径的大小顺序为Z>W>X>Y
B.元素Y分别与X、W元素至少形成两种化合物
C.Y、Z形成的化合物既能和酸反应又能和碱反应
D.X、Y、W对应的简单氢化物中,X的氢化物最稳定
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是模拟工业制硝酸原理的实验装置。先用酒精灯对硬质玻璃管里的三氧化二铬加热,然后把空气鼓入盛有浓氨水的锥形瓶,当三氧化二铬保持红热状态时,移去酒精灯。根据题意回答问题:

(1)硬质玻璃管里发生反应的化学方程式为______。当三氧化二铬红热时,要移去酒精灯,原因是:______。
(2)圆底烧瓶里的实验现象是______,鼓入空气的作用是______。
(3)实验过程中,如果慢慢地鼓入空气,石蕊溶液的颜色______。
(4)实验结束后,在圆底烧瓶内壁上有时会看到少量无色晶体,写出生成该晶体的化学方程式:______。
(5)工业上要获得浓度较大的硝酸,往往在稀硝酸中加入吸水剂硝酸镁或浓硫酸,然后______(填一种操作名称)。
(6)实验室里保存浓硝酸要用棕色瓶的原因是__________________(用化学方程式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】物质的量是高中化学中常用的物理量,请完成以下有关其计算的内容。
(1)0.2 g H2含有___________________个H原子。
(2)100 mL 某Al2(SO4)3溶液中,c(Al3+) = 2.0 mol/L,则其中c(SO42-) = _________mol/L。
(3)等质量的HCl、NH3、CO2、O2四种气体,在相同温度和相同压强条件下,体积最大的是________。
(4)当CO、CO2的分子个数之比为1:2时,原子总数之比为___________,质量之比为________;标准状况下,密度之比为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ、为测定金属钠样品(表面有 Na2O)中钠单质的质量分数,设计了如下实验(反应装置如图所示):
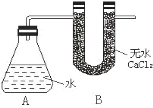
①称量 A、B 的总质量
②称取一定质量的钠样品
③将钠样品投入锥形瓶中,迅速塞紧带 U 形干燥管(内含无水 CaCl2 干燥 剂)的橡皮塞 。有关数据是:称取的金属钠样品质量为 a g,A、B反应前总质量为 m g,反应后 A、B 的总质量为 n g。 请根据题意回答下列问题:
(1)A 中钠和水反应过程可看到钠浮在水面,产生这一现象原因是:_____________
(2)用 a、m、n 表示的钠单质的质量分数为_______________
(3)如果没有 B 装置对实验结果有何影响___________。(填“偏大”或“偏小”“不影响”)
Ⅱ、现用金属钠和空气制备纯度较高的 Na2O2,可利用的装置如下图。回答下列问题:
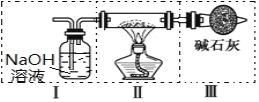
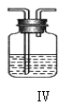
(4)上述装置Ⅳ中盛放的试剂是______,为完成实验应将装置Ⅳ接在_____(填写字母号)。
A.I 之前 B. II 和 III 之间 C.I 和 II 之间 D.III 之后
(5)点燃酒精灯后,观察到装置 II 中的现象为______________。
Ⅲ、现用制得纯度较高的 Na2O2进行相关实验。回答下列问题:
(6)用脱脂棉包住Na2O2粉末,置于石棉网上,通过细管向脱脂棉中吹CO2,脱脂棉_______(填“能”或“不能”)燃烧起来。
(7)盛有1.56 g Na2O2、3.36g NaHCO3的固体混合物放在密闭容器中加热,最后固体是___________(填化学式),质量为_________g.
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室需要0.10mol·L-1CuSO4溶液480mL。
①配制溶液时必需的仪器有:托盘天平(精确到0.1)、药匙、烧杯、玻璃棒、______、胶头滴管以及等质量的几片滤纸。
②配制该溶液需称取CuSO4·5 H2O晶体的质量为_______。
③下列操作会使所配溶液浓度偏低的是________。
A.容量瓶洗涤干净后未干燥
B.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
C.定容时俯视刻度线
D.烧杯和玻璃棒未洗涤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com