
科目: 来源: 题型:
【题目】由合成气制备二甲醚的主要原理如下。下列有关说法正确的是
① CO(g)+2H2(g)![]() CH3OH(g) ΔH1=-90.7 kJ·mol-1
CH3OH(g) ΔH1=-90.7 kJ·mol-1
② 2CH3OH(g)![]() CH3OCH3(g)+H2O(g) ΔH2=-23.5 kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH2=-23.5 kJ·mol-1
③ CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH3=-41.2 kJ·mol-1
CO2(g)+H2(g) ΔH3=-41.2 kJ·mol-1
A.将1mol CO(g)和2 mol H2(g)充分反应,反应会放出90.7 kJ能量
B.反应①的ΔS>0
C.反应③使用催化剂,ΔH3减少
D.反应3H2(g)+3CO(g)![]() CH3OCH3(g)+CO2(g)的ΔH=-246.1 kJ·mol-1
CH3OCH3(g)+CO2(g)的ΔH=-246.1 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。
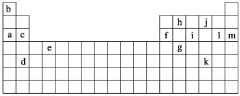
下列______(填写编号)组元素的单质可能都是电的良导体。
①a、c、h ②b、g、k ③c、h、l ④d、e、f
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期主族元素![]() 、
、![]() 、
、![]() 、
、![]() 原子序数依次增大,
原子序数依次增大,![]() 与
与![]() 同主族但最高化合价不同,
同主族但最高化合价不同,![]() 是金属性最强的短周期元素。下列说法不正确的是( )。
是金属性最强的短周期元素。下列说法不正确的是( )。
A.简单离子半径:![]()
B.最高价氧化物对应水化物的酸性:![]()
C.化合物![]() 能与水剧烈反应,产生白雾并放出具有刺激性气味的气体
能与水剧烈反应,产生白雾并放出具有刺激性气味的气体
D.![]() 的气态氢化物通入
的气态氢化物通入![]() 水溶液中产生淡黄色沉淀并放出有刺激性气味的气体
水溶液中产生淡黄色沉淀并放出有刺激性气味的气体
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸铅是一种重要的化工粉末材料,被广泛用于涂料和电池等行业。湿化学法从方铅矿(主要成分为![]() )直接制取硫酸铅粉末的转化流程图如下:
)直接制取硫酸铅粉末的转化流程图如下:
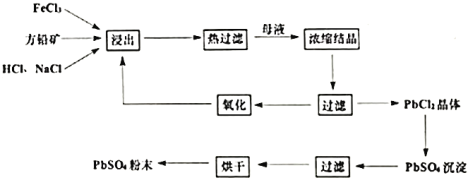
已知:①![]()
②![]()
![]()
回答下列问题:
(1)浸出过程中,产物中![]() 以
以![]() 形式存在,同时可观察到黄色沉淀,浸出过程中的反应的离子方程式为________________。反应后期,有少量气体产生,产生气体的化学方程式为________________。
形式存在,同时可观察到黄色沉淀,浸出过程中的反应的离子方程式为________________。反应后期,有少量气体产生,产生气体的化学方程式为________________。
(2)浓缩结晶过程中是将浸出液静置于冰水混合物中,从平衡角度解释使用冰水混合物的作用为________。
(3)氧化过程中通常加入![]() ,发生反应的离子方程式为__________。
,发生反应的离子方程式为__________。
(4)向![]() 固体中加入
固体中加入![]() ,发生反应的方程式为
,发生反应的方程式为![]()
![]() ,计算该反应的平衡常数为________。
,计算该反应的平衡常数为________。
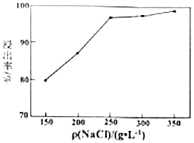
(5)单位体积溶液中加入![]() 的质量对方铅矿的浸出率的影响如图,高于
的质量对方铅矿的浸出率的影响如图,高于![]() 之后,浸出率基本不变,可能的原因是_____________。
之后,浸出率基本不变,可能的原因是_____________。
(6)传统工艺是经火法冶炼得到粗铅,然后电解精炼,再经高温熔融、氧化焙烧制取氧化铅,然后与硫酸反应制得硫酸铅。与传统工艺相比,湿化学法的优点是________(任写两点)。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有部分短周期元素的原子结构如下表:
元素编号 | 元素原子结构 |
X | 原子结构示意图为 |
Y | 最外层电子数是次外层电子数的2倍 |
Z | 原子核内含有12个中子,且其离子的结构示意图为 |
(1)写出X的元素符号:____________,元素Y的最简单氢化物的化学式为______________。
(2)Z元素原子的相对原子质量为____________。
(3)X和Z两种元素的最高价氧化物对应的水化物相互反应的离子方程式为______________。
(4)Y和Z两种元素的最高价氧化物发生氧化还原反应的化学方程式为__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有四种短周期元素A、B、C、D,它们的核电荷数依次增大。A与C,B与D分别是同主族元素。B、D质子数之和是A、C质子数之和的2倍。这四种元素中A、C、D的单质均可在B的单质中燃烧。
(1)A的元素名称是________,C的元素符号是________。
(2)D元素位于元素周期表的第______周期第______族。
(3)C元素的单质在B的单质中燃烧的产物的化学式是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】碱式硫酸铁[Fex(OH)y(SO4)z](其中Fe元素为+ 3价)是一种新型高效絮凝剂。一种利用废铁屑(含Fe和少量Al2O3、Fe2O3)生产碱式硫酸铁的工艺流程如下:
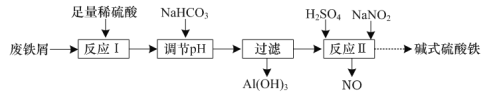
下列说法正确的是
A.x、y、z一定符合关系式:x=y=z
B.“过滤”所得滤液中只含溶质FeSO4
C.“反应Ⅰ”中包含的反应类型有置换反应、化合反应和复分解反应
D.在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,若有11.2 L(标准状况)的O2参与反应,则相当于节约2 mol NaNO2
查看答案和解析>>
科目: 来源: 题型:
【题目】图是某甲醇燃料电池的工作示意图。下列说法正确的是

A.电极b为电池的负极
B.电池工作时将电能转化为化学能
C.放电时a极处所发生的电极反应为:CH3OH-6e-+H2O=CO2↑+6H+
D.放电时溶液中H+向a极移动
查看答案和解析>>
科目: 来源: 题型:
【题目】有A、B、C、D四种元素,A元素的原子得2个电子、B元素的原子失去1个电子后所形成的微粒均与氩原子有相同的核外电子数。C元素的原子只有1个电子,A、D两元素原子核外电子总数比B元素原子质子数多9个。
(1)A的元素名称是_______,B的元素符号是______。
(2)D原子的原子结构示意图为____________,B+的离子结构示意图__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上用重铬酸钠(Na2Cr2O7)结晶后的母液(含少量杂质Fe3+)生产重铬酸钾(K2Cr2O7)。工艺流程如下:

⑴Na2Cr2O7可由FeO·Cr2O3先氧化、再酸化得到。其中FeO·Cr2O3发生氧化反应的化学方程式为4FeO·Cr2O3+7O2+20NaOH![]() 8Na2CrO4+4NaFeO2+10H2O。该反应中每生成1 mol NaFeO2,被Fe元素还原的O2的物质的量为______mol。
8Na2CrO4+4NaFeO2+10H2O。该反应中每生成1 mol NaFeO2,被Fe元素还原的O2的物质的量为______mol。
⑵“调节pH=4”后,溶液中c(Fe3+)=4×10-8 mol·L-1,则该温度下Ksp[Fe(OH)3]=______。
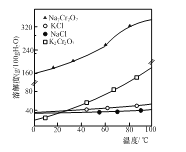
⑶已知部分物质的溶解度曲线如图所示。反应Ⅰ的化学反应类型为______。实验室由质量分数为10%的K2Cr2O7溶液获取K2Cr2O7晶体的方法是______。
⑷为测定K2Cr2O7样品纯度(杂质不参与反应),实验过程为:准确称量一定质量样品,与足量酸性KI 溶液充分反应后,用Na2S2O3标准溶液滴定生成的I2。实验过程中发生的物质转化关系分别为:Cr2O72-![]() Cr3+ S2O32-
Cr3+ S2O32-![]() S4O62-,根据电子得失守恒可知n(K2Cr2O7)∶n(Na2S2O3)=______。
S4O62-,根据电子得失守恒可知n(K2Cr2O7)∶n(Na2S2O3)=______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com