
科目: 来源: 题型:
【题目】反应①Fe(s)+CO2(g)![]() FeO(s)+CO(g)△H>0
FeO(s)+CO(g)△H>0
反应②Fe(s)+H2O(g)![]() FeO(s)+H2(g)△H<0
FeO(s)+H2(g)△H<0
若反应①在温度T1下进行,反应②在温度T2下进行,已知T1>T2,且c(CO2)>c(H2O)
(其他条件均相同),下面对两者反应速率大小判断正确的是( )
A. 反应①快 B. 反应②快 C. 一样大 D. 无法判断
查看答案和解析>>
科目: 来源: 题型:
【题目】下列对化学平衡移动的分析中,不正确的是( )
①已达平衡的反应C(s)+H2O(g)![]() CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
②已达平衡的反应N2(g)+3H2(g)![]() 2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高
2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高
③有气体参加的反应平衡时,若减小反应器容积时,平衡一定向气体体积增大的方向移动
④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡一定不移动
A. ①④ B. ①②③④ C. ②③④ D. ①②③
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E、F、G均为有机物,其中A常用来衡量一个国家石油化工发展水平的标志性物质,它们之间有如下转化关系。
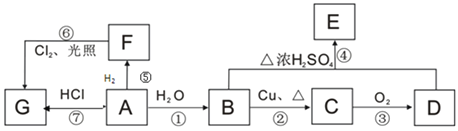
已知:![]() ,请回答下列问题:
,请回答下列问题:
(1)B、D中官能团的名称:B____________,D________________。
(2)指出下列编号对应反应的反应类型:①____________,⑥_____________。
(3)在F的同系物中最简单的有机物的空间构型为___________,电子式为____________。
(4)写出与E含有相同官能团(不含E)的所有同分异构体的结构简式:_________。
(5)写出下列编号对应反应的化学反应方程式:
②_______________________;
④______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验小组同学探究NH3与Cl2的反应,装置如图所示。常温常压下,将氨气收集在薄膜保鲜袋(无弹性)中,氯气收集在反应管中,关闭K,按图连接好装置;将氨气压入反应管,充分反应后打开K。下列说法错误的是

A.反应开始后,保鲜袋逐渐被吸入反应管
B.反应过程中,反应管中产生白烟
C.打开K后,水会倒吸入反应管
D.上述反应原理可用于检验输送氯气的管道是否泄漏
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学依照如下图所示流程提取海带中的碘元素。
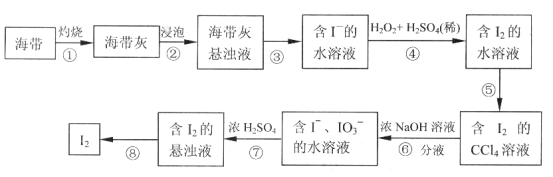
(1)步骤①中灼烧海带所用的仪器是__________(填序号)。
a.试管 b.坩埚 c.烧杯
(2)步骤④中用硫酸酸化的H2O2溶液将I-氧化成I2,反应的离子方程式是__________________。
(3)步骤⑤中采用的分离方法是___________________。
(4)经步骤⑤得到含I2的CCl4溶液后,继续采取步骤⑥⑦的目的是_______________。
(5)步骤⑦的反应中,当1molIO3-发生反应时,转移电子的物质的量是__________mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】蔥醌(AQDS)是一种具有氧化还原活性的廉价有机分子,蔥醌/碘化铵液流可充电电池(如图)以其环保、价廉、稳定等优点被研究及广泛应用。充电时,AQDS转化为AQDS (NH4)2。 下列说法错误的是
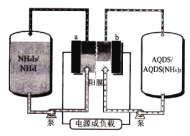
A.放电时 ,b极电势低于a极
B.充电时,a极的电极反应式为:3I--2e-= I3-
C.充电时,电路中每转移1 mole-, 膜两侧电解液的质量变化差为36 g
D.该装置中的阳膜也可以用阴膜代替
查看答案和解析>>
科目: 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是
A.13 g13 C含有的中子数目为6 NA
B.常温下 ,I LpH =4的醋酸溶液所含离子总数为2 ×10-4NA
C.100 g质量分数为 98% 的磷酸中所含氧原子总数为4 NA
D.0.1 mol Fe 完全溶于稀硝酸,转移的电子数目为0.3 NA
查看答案和解析>>
科目: 来源: 题型:
【题目】铝热法冶炼金属铬的矿渣中含有Cr2O7、Al2O3及少量Fe2O3,从中提取铬与铝有酸法和碱法两种工艺。请回答:
I.酸法。矿渣经硫酸浸取后,浸取液通过电沉积得到单质Cr;向剩余溶液中加碱回收得到Al(OH)3。
(1)为提高矿渣的浸取率,可采取的措施有_____(写出两点)。
(2)电沉积时,阴极的电极反应式为______________。
II. 碱法。工艺流程如下:
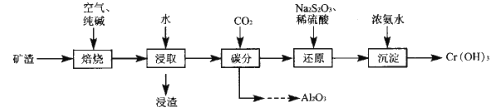
已知:①“焙烧”后固体成分为Na2CrO4、NaAlO2、NaFeO2。
②![]() 、Zn2+均可与EDTA1:1结合成络离子;Zn2+可与PAN1:1结合成紫红色络合物,且结合能力弱于EDTA。
、Zn2+均可与EDTA1:1结合成络离子;Zn2+可与PAN1:1结合成紫红色络合物,且结合能力弱于EDTA。
(3)浸渣的主要成分为Fe(OH)3。则“浸取”时发生反应的离子方程式为_________。
(4)“浸取”后所得溶液中Al的含量可用EDTA滴定法测定:
①取20.00mL浸取液于锥形瓶中,加入c1molL-1EDTA标准液V1mL(稍过量);
②依次用盐酸、醋酸钠—醋酸缓冲溶液调溶液至酸性,加热后滴入PAN指示剂;
③用c2molL-1ZnSO4标准液滴定至溶液恰好呈紫红色,消耗标准液V2mL。则“浸取”后所得溶液中Al的含量为_________gL-1(填计算式即可)。
(5)“碳分”时通入CO2后,通过_____ (填操作名称),即可得到纯净的Al2O3。
(6)“还原”时发生主要反应的离子方程式为__________。
(7)“沉淀”时,当c(Cr3+)≤10-5molL-1时,应调节溶液的pH至少为_________。(Ksp[Cr(OH)3]=1.0×10-32)
查看答案和解析>>
科目: 来源: 题型:
【题目】向2 L密闭容器中通入a mol气体A和b mol气体B,在一定条件下发生反应:xA(g)+yB(g)pC(g)+qD(g)已知:平均反应速率v(C)=![]() v(A);反应2 min时,A的浓度减少了
v(A);反应2 min时,A的浓度减少了![]() a mol,B的物质的量减少了
a mol,B的物质的量减少了![]() mol,有a mol D生成。
mol,有a mol D生成。
回答下列问题:
(1)反应2 min内,v(A)=________,v(B)=________。
(2)化学方程式中,x=________,y=________,p=________,q=________。
(3)反应平衡时,D为2a mol,则B的转化率为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】针对下表中的9种元素,用化学用语回答下列问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
1 | ① | ||||||
2 | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
(1)写出⑧的原子结构示意图:_________________________。
(2)形成物质种类最多的元素是__________________。
(3)用电子式表示⑤和⑨形成化合物的过程__________________。
(4)⑤⑥⑦最高正价氧化物对应水化物碱性由强至弱的顺序是_____________。
(5)④的单质与甲醇(CH3OH)形成的碱性燃料电池的负极方程式:________________。
(6)写出⑦的单质与三氧化二铁反应的化学方程式____________________。
(7)③和④的气态氢化物的稳定性顺序为:______________。④和⑧的气态氢化物的沸点顺序为:_____________,出现这种变化的原因是:_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com