
科目: 来源: 题型:
【题目】某溶液中可能含有K+、Na+、![]() 、Cl-中的一种或几种,为鉴别其中所含离子,现进行如下实验:
、Cl-中的一种或几种,为鉴别其中所含离子,现进行如下实验:

请回答下列问题:
(1)原溶液中一定存在的离子是______(填离子符号,下同),一定不存在的离子是______________,可能存在的离子是__________________。
(2)为进一步确定原溶液中可能存在的离子是否存在,应进行的实验操作及判断依据是_________
查看答案和解析>>
科目: 来源: 题型:
【题目】奥司他韦是一种高效、高选择性神经氨酸酶抑制剂,是目前治疗流感的最常用药物之一,是公认的抗禽流感、甲型H1N1等病毒最有效的药物之一。也是国家的战略储备药物。也有专家尝试使用奥司他韦作为抗新型冠状病毒肺炎药物。
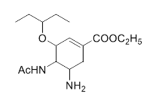
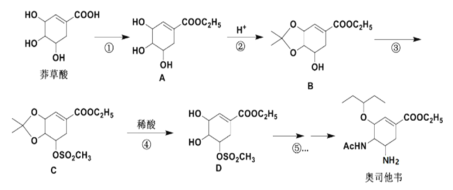
以莽草酸作为起始原料是合成奥司他韦的主流路线,合成路线如下:
已知:![]() +
+![]()
![]()
![]() +H2O,回答下列问题:
+H2O,回答下列问题:
(1)A中的含氧官能团名称有:________________,反应③的反应类型:____________。
(2)反应②的反应试剂:________________和H+。
(3)请写出①反应的化学方程式:_______________。
(4)芳香化合物X是B的同分异构体,则符合官能团只含酚羟基的X有_____种。
(5)碳原子上连有4个不同的原子或基团时,该碳称为手性碳。D中有____个手性碳
(6)设计由对甲基苯甲醛制备对醛基苯甲酸![]() 的合成路线____________。
的合成路线____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知298K,1.01×105Pa条件下:2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ·mol-1;
CO(g)+![]() O2(g)=CO2(g) △H=-282.9kJ·mol-1则该条件下CO(g)+H2O(g) = H2(g)+CO2(g)的反应热是
O2(g)=CO2(g) △H=-282.9kJ·mol-1则该条件下CO(g)+H2O(g) = H2(g)+CO2(g)的反应热是
A. - 41.1 kJ·mol-1B. + 200.7 kJ·mol-1
C. - 766.5 kJ·mol-1D. + 41.1 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】已知反应:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。
(1)参加反应的HNO3和作为氧化剂的HNO3的个数比为________。
(2)若有64 g Cu被氧化,则被还原的HNO3的质量是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】FeCl2是一种常用的还原剂、媒染剂。某化学实验小组在实验室里用如下两种方法来制备无水FeCl2。有关物质的性质如下:
C6H5Cl(氯苯) | C6H4Cl2(二氯苯) | FeCl3 | FeCl2 | |
溶解性 | 不溶于水,易溶于苯、乙醇 | 不溶于C6H5Cl、C6H4Cl2、苯,易溶于乙醇,易吸水 | ||
熔点/℃ | -45 | 53 | 304 | 670 |
沸点/℃ | 132 | 173 | 316,易升华 | 700 |
(1)用H2还原无水FeCl3制取FeCl2。有关装置如下:

①H2还原少量无水FeCl3制取FeCl2的化学方程式为_____________。
②按气流由左到右的方向,上述仪器的连接顺序为B→A→___→___→___→E(填字母,装置可多次使用);A中长颈漏斗的作用_____________。
③C中盛放的试剂是_____________。
(2)利用反应2FeCl3+C6H5Cl![]() 2FeCl2+C6H4Cl2+HCl↑,制取无水FeCl2并测定FeCl3的转化率。按如图装置,在三颈烧瓶中放入32.5 g无水氯化铁和过量的氯苯,反应开始前先通N2一段时间,控制反应温度在一定范围加热3 h,反应完成后继续通一段时间N2至装置冷却后,分离提纯得到粗产品。
2FeCl2+C6H4Cl2+HCl↑,制取无水FeCl2并测定FeCl3的转化率。按如图装置,在三颈烧瓶中放入32.5 g无水氯化铁和过量的氯苯,反应开始前先通N2一段时间,控制反应温度在一定范围加热3 h,反应完成后继续通一段时间N2至装置冷却后,分离提纯得到粗产品。
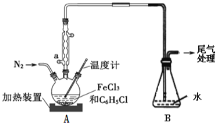
①仪器a的作用是__________。
②反应中提供过量氯苯的作用是__________。
③反应结束后,冷却实验装置A,将三颈烧瓶内物质倒出,经过滤、洗涤、干燥后,得到粗产品。洗涤所用的试剂可以是____,回收滤液中C6H5Cl的操作方法是______。
④反应后将锥形瓶中溶液配成250 mL,量取25.00 mL所配溶液,用0.400 mol/L的NaOH溶液滴定,终点时消耗NaOH溶液为19.60 mL,则氯化铁的转化率为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在容积不变的密闭容器中存在如下反应:2A(g)+B(g)![]() 3C(g);ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )
3C(g);ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )

A. 图Ⅰ表示的是t1时刻增大反应物的浓度对反应速率的影响
B. 图Ⅱ表示的一定是t1时刻加入催化剂后对反应速率的影响
C. 图Ⅲ表示的是催化剂对平衡的影响,且甲的催化效率比乙高
D. 图Ⅲ表示的是温度对化学平衡的影响,且乙的温度较高
查看答案和解析>>
科目: 来源: 题型:
【题目】磷酸氯喹用于治疗对氯喹敏感的恶性疟、间日疟及三日疟。若干位药物研发和临床专家研究发现,该药物在细胞水平上能有效抑制新型冠状病毒的感染。
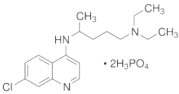
(1)磷酸氯喹是由多种元素形成的物质,其中氯元素的基态氯原子,电子占据的最高能层符号为_____;磷元素的简单氢化物PH3的中心原子杂化方式是_____,属于_______(填“极性”或“非极性”)分子;其他的四种元素的第一电离能从大到小的顺序为_________。
(2)N与P为同族元素,比较其最高价氧化物的水化物酸性并从结构的角度说明理由:________
(3)H3PO4与Fe3+形成H3[Fe(PO4)2],此性质常用于掩蔽溶液中的Fe3+。基态Fe3+的核外电子排布式为___________;![]() 做为配体为铁离子提供______。
做为配体为铁离子提供______。
(4)磷化铜(Cu3P2)用于制造磷青铜。磷青铜是含少量锡、磷的铜合金,主要用作耐磨零件和弹性原件,其晶胞结构如图所示:
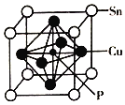
①其化学式为__________
②铜或铜盐的焰色反应为_____色,金属元素能产生焰色实验的微观原因为______。
③若晶体密度为ρg/cm3,摩尔质量为Mg/mol,NA代表阿伏加德罗常数,则最近的Cu原子核间距为________________pm。
查看答案和解析>>
科目: 来源: 题型:
【题目】碳的氧化物对环境的影响较大,研究和开发碳的氧化物的应用对发展低碳经济,构建生态文明社会具有重要的意义。
(1)已知:①甲醇的燃烧热ΔH=-726.4 kJ·mol-1;
②H2(g)+![]() O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
③H2O(g)=H2O(l) ΔH=-44 kJ·mol-1
则二氧化碳和氢气合成液态甲醇、生成气态水的热化学方程式为_____________。
(2)在T1时,向体积为2L的恒容容器中充入物质的量之和为3mol的CO和H2,发生反应CO(g)+2H2(g)CH3OH(g),反应达到平衡时CH3OH(g)的体积分数(φ)与![]() 的关系如图所示:
的关系如图所示:
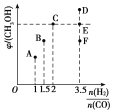
①当起始![]() =2时,经过5min达到平衡,CO的转化率为0.6,则0~5min内平均反应速率v(H2)=______。若此刻再向容器中加入CO(g)和CH3OH(g)各0.4mol,达到新平衡时H2的转化率将________(填“增大”“减小”或“不变”)。
=2时,经过5min达到平衡,CO的转化率为0.6,则0~5min内平均反应速率v(H2)=______。若此刻再向容器中加入CO(g)和CH3OH(g)各0.4mol,达到新平衡时H2的转化率将________(填“增大”“减小”或“不变”)。
②当![]() =3.5时,达到平衡后,CH3OH的体积分数可能是图像中的________(填“D”“E”或“F”)点。
=3.5时,达到平衡后,CH3OH的体积分数可能是图像中的________(填“D”“E”或“F”)点。
(3)已知由CO2生成CO的化学方程式为CO2(g)+O(g)CO(g)+O2(g),其正反应速率为v正=k正·c(CO2)·c(O),逆反应速率为v逆=k逆·c(CO)·c(O2),k为速率常数。2500 K时,k逆=1.21×105L·s-1·mol-1,k正=3.02×105L·s-1·mol-1,则该温度下该反应的平衡常数K为________。(保留小数点后一位小数)
(4)CH3OH—O2在新型聚合物催化下可发生原电池反应,其装置如图:
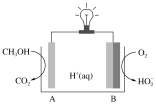
①外电路中每转移3mol电子,溶液中生成_______molH+
②写出电极B的电极反应式:__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下发生反应:2A(g)+2B(g) ![]() xC(g)+2D(g),在2L密闭容器中,把4molA和2molB混合,2min后达到平衡时生成1.6molC,又测得反应速率v(D)=0.2mol·L-1·min-1,下列说法正确的是
xC(g)+2D(g),在2L密闭容器中,把4molA和2molB混合,2min后达到平衡时生成1.6molC,又测得反应速率v(D)=0.2mol·L-1·min-1,下列说法正确的是
A. A和B的转化率均是20% B. x = 2
C. 平衡时B的物质的量为1.2mol D. 平衡时气体压强比原来减小
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,向1L0.1mol·L-1一元酸HR溶液中逐渐通入氨气[已知常温下NH3·H2O电离平衡常数K=1.76×10-5],使溶液温度和体积保持不变,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述正确的是
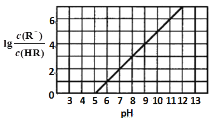
A.0.1mol·L-1HR溶液的pH为5
B.当pH=6时,水电离出的氢离子浓度为1.0×10-6
C.当通入0.1 mol NH3时,c(![]() )>c(R-)>c(H+)>c(OH-)
)>c(R-)>c(H+)>c(OH-)
D.当 pH=7时,c(![]() )=c(R-)
)=c(R-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com