
科目: 来源: 题型:
【题目】(1)亚硝酰氯(ClNO)是有机合成中常用试剂,已知:2NO(g)+Cl2(g)![]() 2ClNO(g) △H<0,一定温度下,将2 molNO与2 molCl2置于2L密闭容器中发生反应。
2ClNO(g) △H<0,一定温度下,将2 molNO与2 molCl2置于2L密闭容器中发生反应。
①下列可判断反应达平衡状态的是___________(填序号字母)。
A. 混合气体的平均相对分子质量不变 B. 混合气体密度保持不变
C. NO和Cl2的物质的量之比保持不变 D. 每消耗1 moI NO同时生成1molClNO
②为了加快化学反应速率,同时提高NO的转化率,其他条件不变时,可采取的措施有_________(填选项序号字母)。
A. 升高温度 B. 缩小容器体积 C. 再充入Cl2气体 D. 使用合适的催化剂
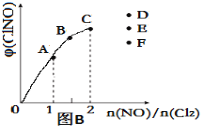
③一定条件下在恒温恒容的密闭容器中,按一定比例充入NO(g)和Cl2(g),平衡时ClNO的体积分数随n(NO)/n(Cl2)的变化图像如图(B)所示,当n(NO)/n(Cl2)=2.5时,达到平衡状态,ClNO的体积分数可能是下图中D、E、F三点中的________点。
(2) 在体积为10 L的密闭容器中充入3 mol NO和2 mol Cl2,在不同温度下发生反应2NO(g)+Cl2(g)![]() 2ClNO(g),ClNO的百分含量随时间的变化如图所示。已知T1>T2>T3。
2ClNO(g),ClNO的百分含量随时间的变化如图所示。已知T1>T2>T3。
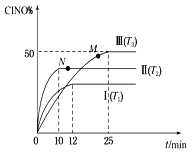
①与实验Ⅰ相比,实验Ⅱ除温度不同外,还改变的条件是__________________。
②实验Ⅲ反应至25 min达到平衡,用NO物质的浓度变化表示的反应速率为__________________。达到平衡时,若实验Ⅲ达到平衡时的热量变化为Q kJ,则该反应的热化学方程式为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】金属冶炼、电镀、电路板生产等过程会产生大量的 Cu2+,Cu2+是一种重金属离子,严重影响水生动植物的生长发育,对人体健康也有很大危害,必须经过处理达标后方可排放。某电路板生产企业的水质情况及国家允许排放的污水标准如下表:
项目 | 废水水质 | 排放标准 |
pH | 1.0 | 6~9 |
Cu2+(mg/L) | 1470 | ≤0.5 |
氨氮(mg/L) | 2632 | ≤15 |
Ⅰ.为研究上述废水中 Cu2+的处理方法并实现 Cu 的资源化回收,有研究者进行了如下实验: 向一定体积的废水中加入一定量废铁屑和焦炭粉,置于搅拌器上搅拌 90min、静置,经分析测得上清液中铜含量约为 72mg/L;滤出上清液,向滤液中加入一定量 FeS 固体,充分搅拌后静置,经分析测得其中铜含量已经达标。
(1)在 pH=1.0 的废水中,氨氮的主要存在形式是_____(用化学式表示)。
(2)①加入废铁屑后,废水中的铜含量明显减少,反应的离子方程式是_____
②加入焦炭可以加快反应速率,原因是_________________________________
(3)结合化学用语解释加入 FeS 固体使废水达标的原因_________________________。
(4)在处理废水过程中使用的铁粉会因表面布满一层铜膜而失效,因此要对失效的铁粉进行活化处理,同时回收铜。处理方法为:用一定浓度的氨水浸泡包覆铜膜的铁粉,露置在空气中一段时间后,可以将表面的 Cu 转化为[Cu(NH3)4]2+与铁粉分离。
请写出 Cu 转化为 [Cu(NH3)4]2+的离子方程式:_____。
Ⅱ为研究废水处理的最佳 pH,取五份等量的 I 中上清液, 分别用 30%的 NaOH 溶液调节 pH 值至 8.5、9、9.5、10、11,静置后,分析上层清液中铜元素的含量。实验结果如图所示。查阅资料可知:Cu(OH)2 + 4NH3![]() [Cu(NH3)4]2+ + 2OH-。
[Cu(NH3)4]2+ + 2OH-。
(5)根据实验结果,你认为最佳的 pH 约为_____________________________。结合资料解释实验结果呈图中 b~d 段曲线所示的原因:_________________________。

查看答案和解析>>
科目: 来源: 题型:
【题目】在某2 L恒容密闭容器中充入2 mol X(g)和1 mol Y(g)发生反应:2X(g)+Y(g)![]() 3Z(g),反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是( )
3Z(g),反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是( )
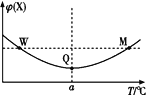
A.M点时,Y的转化率最大B.升高温度,平衡常数减小
C.W点时 v正 = v逆D.W、M两点Y的正反应速率相同
查看答案和解析>>
科目: 来源: 题型:
【题目】坦桑石的主要化学成分为Ca2Al3(SiO4)3(OH),还可含有V、Cr、Mn等元素。
(1)下列状态中的铝微粒,电离最外层的一个电子所需能量最大的是____________。
①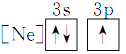 ②
②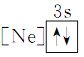 ③
③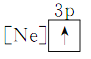 ④
④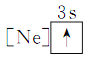
(2)烟酸铬是铬的一种化合物,其合成过程如下:
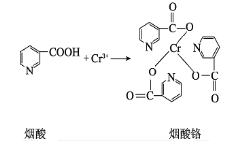
①Cr原子的价层电子排布图为 _______________。这样排布电子遵循的原则是 ______________。
②烟酸中所含元素的第一电离能I1(N)_____ I1(O),原因是_________________ 。
③烟酸中碳、氮原子的杂化方式分别为 _________________、__________________。
(3)SiCl4、SiF4都极易水解。二者都属于______(填“极性”或“非极性”)分子,其熔点关系为SiF4 ______SiCl4(填“>”“<”或“=”)。
(4)将Mn掺入GaAs晶体(图甲)可得到稀磁性半导体材料(图乙),图甲、图乙晶体结构不变。
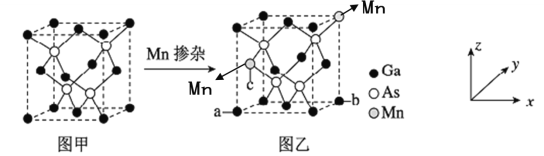
①图乙中a点和b点的原子坐标参数分别为(0,0,0)和(1,1,0),则c点的原子坐标参数为_______。
②设图甲晶体的密度为ρg·cm-3,用NA表示阿伏伽德罗常数的数值,则该晶胞中距离最近的两个砷原子之间的距离为 ___________ pm。(用含ρ、NA的关系式表示最简化的计算式即可)
查看答案和解析>>
科目: 来源: 题型:
【题目】(1) 在含Fe3+的S2O![]() 和I-的混合溶液中,反应S2O
和I-的混合溶液中,反应S2O![]() (aq) + 2I-(aq)=2SO
(aq) + 2I-(aq)=2SO![]() (aq) + I2(aq)的分解机理及反应进行中的能量变化如图所示。
(aq) + I2(aq)的分解机理及反应进行中的能量变化如图所示。
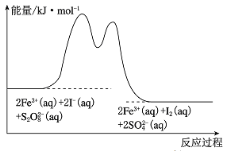
步骤①:2Fe3+(aq) + 2I-(aq) = I2(aq)+ 2Fe2+(aq)
步骤②:2Fe2+(aq) + S2O![]() (aq) = 2Fe3+(aq) + 2SO
(aq) = 2Fe3+(aq) + 2SO![]() (aq)
(aq)
下列有关该反应的说法不正确的是 _______。
A. 该反应为吸热反应
B. Fe3+是该反应的催化剂,能提高反应体系中活化分子百分数
C. 反应速率v(S2O![]() )=2v(SO
)=2v(SO![]() )
)
D. 若不加Fe3+,则正反应的活化能比逆反应的大
(2)一定条件下,工业上可采用CH3OH→CO+2H2的方法来制取高纯度的CO和H2。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。
① 甲醇脱氢反应的第一步历程,有两种可能方式:
方式A:CH3OH*→CH3O*+H* Ea=+103.1kJ·mol-1 方式B:CH3OH*→CH3*+OH* Eb=+249.3kJ·mol-1
由活化能E值推测,甲醇裂解过程主要经历的方式应为_____________。(填“A”或“B”)
②下图为计算机模拟的各步反应的能量变化示意图。

该历程中,放热最多的步骤的化学方程式为 ________________________________ 。
(3)已知298K时,A、B分别为无色气体、深色气体,发生反应:A(g)![]() 2B(g)
2B(g)
①反应达平衡后,扩大容器的体积,再次达到平衡时混合气体的颜色 ____(填“变深”、“变浅”或“不变”)。
②恒容密闭容器中发生上述反应,已知v正=k正·p(A),v逆=k逆·p2(B),Kp=____________ 。(用k正、k逆表示)。若初始压强为100kPa.k正=2.8×104 s-1,当B的体积分数为40%时,v正= _____kPa·s-1[其中p(A)和p(B)分别是A和B的分压, 分压=p总×气体体积分数,k正、k逆为速率常数]
查看答案和解析>>
科目: 来源: 题型:
【题目】25 ℃时,向25mL0.1 mol·L-1 NaOH溶液中逐滴加入0.2mol·L-1醋酸溶液,滴定曲线如图所示,下列说法正确的是( )
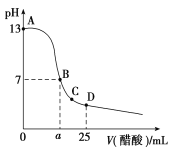
A.在A、B间任一点的溶液中一定都有:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B.C点对应的溶液中,水电离出的H+浓度大于10-7 mol·L-1
C.用含a的代数式表示CH3COOH的电离平衡常数K=![]()
D.D点对应的溶液中,存在如下关系:c(CH3COO-)-c(CH3COOH)= 2c(H+)-c(OH-)
查看答案和解析>>
科目: 来源: 题型:
【题目】粗硅提纯常见方法之一是先将粗硅与HCl反应制得SiHCl3,经提纯后再用H2还原:SiHCl3(g)+H2(g) ![]() Si(s)+3HCl(g)。在2L密闭容器中,不同温度及不同n(H2)/n(SiHCl3)时,反应物X的平衡转化率关系如图。下列判断合理的是
Si(s)+3HCl(g)。在2L密闭容器中,不同温度及不同n(H2)/n(SiHCl3)时,反应物X的平衡转化率关系如图。下列判断合理的是
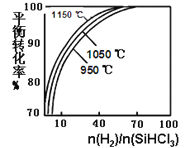
A. X是H2
B. 1150℃反应的平衡常数大于950℃时反应的平衡常数
C. 减小Si(s)的量,有利于提高SiHCl3的转化率
D. 工业上可采用增大压强的方法提高产率
查看答案和解析>>
科目: 来源: 题型:
【题目】t ℃时,pH=2的稀硫酸和pH=11的NaOH溶液等体积混合后溶液呈中性,则该温度下,1体积的稀硫酸和10体积的NaOH溶液混合后溶液呈中性,则稀硫酸的pH(pHa)与NaOH溶液的pH(pHb)的关系是( )
A.pHa+pHb=12B.pHa+pHb=13C.pHa+pHb=14D.pHa+pHb=15
查看答案和解析>>
科目: 来源: 题型:
【题目】碘化钠在医疗及食品方面有重要作用。实验室用NaOH、单质碘和水合肼(N2H4·H2O)为原料制备碘化钠。已知:水合肼具有还原性。回答下列问题:
(1)水合肼的制备有关反应原理为:CO(NH2)2(尿素)+NaClO+2NaOH=N2H4·H2O+NaCl+Na2CO3
①制备次氯酸钠和氢氧化钠混合液装置的连接顺序为 ________________(按气流方向用小写字母表示)。
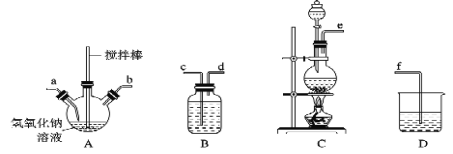
②若该实验温度控制不当,反应后测得三颈烧瓶内ClO-与ClO3-的物质的量之比为1:5,则Cl2与NaOH反应时,被氧化的氯元素与被还原的氯元素物质的量之比为_______________。
③制备水合肼时,应将_____________________滴到 ________________中(填“NaClO溶液”或“尿素溶液”),且滴加速度不能过快。
(2)碘化钠的制备采用水合肼还原法制取碘化钠固体,其制备流程如图所示:
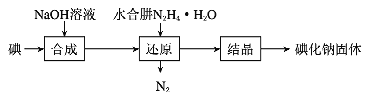
在“还原”过程中,主要消耗反应过程中生成的副产物IO![]() ,该过程的化学方程式为 _______________________________________________。
,该过程的化学方程式为 _______________________________________________。
工业上也可用硫化钠或铁屑还原碘酸钠制备碘化钠,但水合肼还原法制得的产品纯度更高,其原因是 ___________________________________________________________________________________。
(3)测定产品中碘化钠含量的实验步骤
a、称取10.00g样品并溶解,在250mL容量瓶中定容;
b、量取25.00mL待测液于锥形瓶中,然后加入足量的FeCl3溶液,充分反应后再加入X溶液作指示剂;
c、用0.2100mol·L-1的Na2S2O3标准液滴定至终点(2Na2S2O3+I2=Na2S4O6+2NaI),重复实验多次,测得消耗标准液体积为15.00mL。
①S2O![]() 的结构式如图所示,其中S*的化合价为____________。
的结构式如图所示,其中S*的化合价为____________。
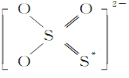
②X溶液为 ___________ ;滴定终点的现象为 __________________。
③该样品中NaI的质量分数为_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】用KMnO4氧化盐酸溶液,反应方程式如2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O,若产生的Cl2在标准状况下体积为56 L,计算:
(1)参加反应的HCl的物质的量________________
(2)反应中被氧化的HCl的物质的量__________________
(3)并用双线桥标出电子转移的方向和数目___________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com