
科目: 来源: 题型:
【题目】X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如下:
元素代号 | X | Y | Z | M | Q | R |
原子半径/nm | 0.160 | 0.143 | 0.102 | 0.075 | 0.077 | 0.037 |
主要化合价 | +2 | +3 | +6,-2 | +5,-3 | +4,-4 | +1 |
(1)Y在元素周期表中的位置是___。
(2)元素Q和R形成的化合物A是果实催熟剂,用A制备乙醇的化学方程式是___。
(3)单质铜和元素M的最高价氧化物对应水化物的稀溶液发生反应的离子方程式为___。
(4)元素X的金属性比元素Y___(填“强”或“弱”),用原子结构的知识解释原因___。
(5)元素Q、元素Z的含量影响钢铁性能,采用如图装置A在高温下将钢样中元素Q、元素Z转化为QO2、ZO2。
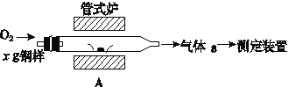
①气体a的成分是__(填化学式)。
②若钢样中元素Z以FeZ的形式存在,在A中反应生成ZO2和稳定的黑色氧化物,则反应的化学方程式是___。
查看答案和解析>>
科目: 来源: 题型:
【题目】在体积为2L的恒容密闭容器中,充入2molCO2和6molH2,一定条件下反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。
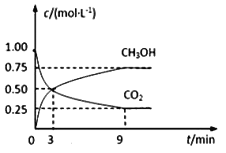
(1)0~9min内,v(H2)=__mol·L1·min1。
(2)能说明上述反应达到平衡状态的是__(填编号)。
a.反应中CO2与CH3OH的物质的量浓度之比为1:1
b.混合气体的密度不随时间的变化而变化
c.单位时间内消耗3 mol H2,同时生成1 mol H2O
d.CO2的体积分数在混合气体中保持不变
e.混合气体的压强不随时间的变化而变化
(3)平衡时H2的转化率为___。
(4)平衡时混合气体中H2O(g)的体积分数是__。
(5)一定温度下,第9分钟时v正(CH3OH)__(填“大于”、“小于”或“等于”)第3分钟时v逆 (CH3OH)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学依照如图所示流程提取海带中的碘元素。
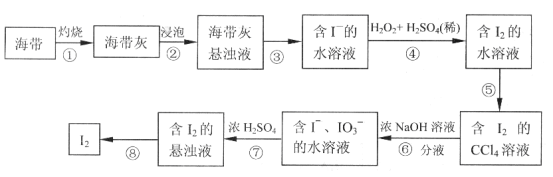
(1)步骤①中灼烧海带所用的仪器是___(填序号)。
a.试管 b.坩埚 c.烧杯 d.锥形瓶
(2)步骤④中用硫酸酸化的H2O2溶液将I-氧化成I2,反应的离子方程式是__。
(3)步骤⑤中采用的分离方法是___。
(4)经步骤⑤得到含I2的CCl4溶液后,继续采取步骤⑥⑦的目的是__。
(5)步骤⑦的反应中,当1molIO3-发生反应时,转移电子的物质的量是__mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】丙烷是液化石油气主要成分之一,是一种优良的燃料。试回答下列问题:
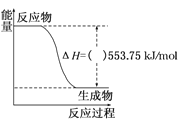
(1)如图是一定量丙烷完全燃烧生成CO2和1mol H2O(l)过程中的能量变化图,(图中的括号内填入“+”或“﹣”)_____。写出表示丙烷燃烧热的热化学方程式:_________________________
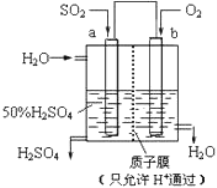
(2)科研人员设想用如图所示装置生产硫酸。
①上述生产硫酸的总反应方程式为_____________,b 是___________ 极(填“正”或“负”),b 电极反应式为______________________________,a 电极发生______________ (填“氧化反应”或“还原反应”)。②生产过程中H+向_____(填 a 或 b)电极区域运动。
(3)将两个铂电极插入氢氧化钾溶液中,向两极分别通入甲烷和氧气,可构成甲烷燃料电池,已知通入甲烷的一极为负极,其电极反应式为:_______________________。电池在放电过程中,溶液的pH值将______________ 。(填“下降”“上升”或“不变”)
查看答案和解析>>
科目: 来源: 题型:
【题目】等物质的量的![]() 和
和![]() 的混合物9.20g与100mL盐酸反应。
的混合物9.20g与100mL盐酸反应。
(1)欲求标准状况下生成![]() 的体积时,还需要什么数据_______。
的体积时,还需要什么数据_______。
(2)若![]() 和
和![]() 不是等物质的量混合,则9.20g固体与盐酸完全反应时,在标准状况下生成
不是等物质的量混合,则9.20g固体与盐酸完全反应时,在标准状况下生成![]() 的气体的体积范围(V)为____。
的气体的体积范围(V)为____。
查看答案和解析>>
科目: 来源: 题型:
【题目】乙烯是重要有机化工原料。结合以下路线回答:
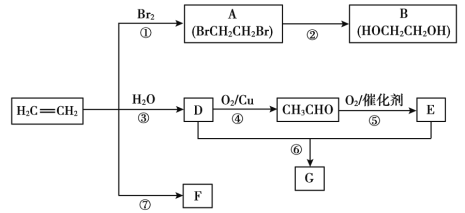
已知:2CH3CHO+O2![]() 2CH3COOH
2CH3COOH
(1)反应①的化学方程式是__。
(2)B的官能团是__。
(3)F是一种高分子,可用于制作食品袋,其结构简式为__。
(4)G是一种油状、有香味的物质,有以下两种制法。
制法一:实验室用D和E反应制取G,某学习小组在实验室制取乙酸乙酯的主要步骤如下:
i.配制2mL浓硫酸、3mLD(含18O)和2mLE的混合溶液。
ii.按如图连接好装置并加入混合液,用小火均匀加热3~5min。
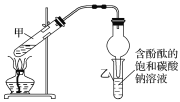
iii.待试管乙收集到一定量产物后停止加热,撤出试管乙用力振荡,然后静置待分层。
iv.分离出乙酸乙酯,洗涤、干燥。
回答问题:
①装置中球形干燥管,除起冷凝作用外,另一重要作用是___。
②步骤②安装好实验装置,加入药品前还应检查__。
③反应中浓硫酸的作用是__;写出能表示18O位置的制取乙酸乙酯的化学方程式:__。
④上述实验中饱和碳酸钠溶液的作用是__(填字母)。
a.中和乙酸并吸收乙醇
b.中和乙酸和乙醇
c.降低乙酸乙酯的溶解度
d.加速酯的生成,提高其产率
⑤步骤③所观察到的现象是__;从试管乙中分离出乙酸乙酯的实验操作名称是___。
制法二:工业上用CH2=CH2和E直接反应获得G。
a.反应类型是__。
b.与制法一相比,制法二的优点是__。
查看答案和解析>>
科目: 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两等份。向其中一份中逐渐加入铜粉,最多能溶解19.2 g(己知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示。下列分析或结果错误的是( )
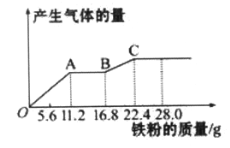
A. 第二份溶液中最终溶质为FeSO4
B. 原混合酸中NO3-物质的量为0.4mol
C. OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气
D. 取20 mL原混合酸加水稀释至1 L后溶液c(H+) =0.1mol L-l
查看答案和解析>>
科目: 来源: 题型:
【题目】今年是门捷列夫发现元素周期律150周年。下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法错误的是

A. 原子半径:W<X
B. 常温常压下,Y单质为固态
C. 气态氢化物热稳定性:Z<W
D. X的最高价氧化物的水化物是强碱
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:N2O4(g)![]() 2NO2(g) ΔH=+52.70kJ·mol-1
2NO2(g) ΔH=+52.70kJ·mol-1
(1)在恒温、恒容的密闭容器中,进行上述反应时,下列描述中,能说明该反应已达到平衡的是___。
A.v正(N2O4)=2v逆(NO2)
B.容器中气体的平均相对分子质量不随时间而变化
C.容器中气体的密度不随时间而变化
D.容器中气体的分子总数不随时间而变化
(2)t℃恒温下,在固定容积为2L的密闭容器中充入0.054molN2O4,30秒后达到平衡,测得容器中含n(NO2)=0.06mol,则t℃时反应N2O4(g)![]() 2NO2(g)的平衡常数K=___。若向容器内继续通入少量N2O4,则平衡___移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后NO2的体积分数__原平衡时NO2的体积分数(填“大于”、“小于”或“等于”)。
2NO2(g)的平衡常数K=___。若向容器内继续通入少量N2O4,则平衡___移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后NO2的体积分数__原平衡时NO2的体积分数(填“大于”、“小于”或“等于”)。
(3)取五等份NO2,分别加入到温度不同、容积相同的恒容密闭容器中,发生反应:2NO2(g)![]() N2O4(g)。反应相同时间后,分别测定体系中NO2的百分含量(NO2%),并作出其百分含量随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是___。
N2O4(g)。反应相同时间后,分别测定体系中NO2的百分含量(NO2%),并作出其百分含量随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是___。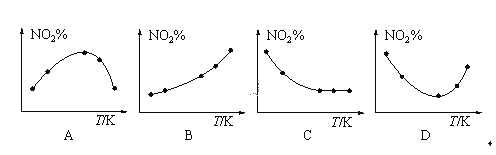
查看答案和解析>>
科目: 来源: 题型:
【题目】电动汽车(标志为“![]() ”)在改善城市交通、保护环境等方面的作用至关重要。下列说法不正确的是
”)在改善城市交通、保护环境等方面的作用至关重要。下列说法不正确的是
A. 电动汽车的使用有助于减少氮氧化物的排放
B. 燃油汽车也可以悬挂该标志
C. 电动汽车使用时涉及化学能与电能的转换
D. 电动汽车充电、放电过程均有电子转移
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com