
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.用系统命名法命名有机物![]() 和
和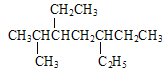 主链碳原子数均为7个
主链碳原子数均为7个
B.某烃的分子式为C10H14,它不能使溴水褪色,但可使酸性KMnO4溶液褪色,且分子结构中只有一个烷基,符合条件的烃有4种
C.碳原子数小于或等于8的单烯烃中,与HBr加成产物只有一种结构,符合条件的单烯烃有6种
D.苯甲醛分子中所有的原子不一定共平面
查看答案和解析>>
科目: 来源: 题型:
【题目】尼泊金甲酯用作化妆品防腐剂,其结构为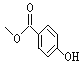 。下列有关说法正确的是( )
。下列有关说法正确的是( )
A.1mol尼泊金甲酯完全燃烧消耗7molO2
B.该化合物能与溴水反应,也能与NaHCO3反应
C.该化合物的同分异构体可能含有羧基
D.1mol该化合物最多可与4molH2反应
查看答案和解析>>
科目: 来源: 题型:
【题目】利用光伏电池提供电能处理废水中的污染物(有机酸阴离子用R-表示),并回收有机酸HR,装置如图所示。下列说法错误的是
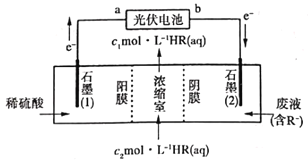
A.在光伏电池中a极为正极B.石墨(2)极附近溶液的pH降低
C.HR溶液:c2<c1D.若两极共收集3mol气体,则理论上转移4mol电子
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化铁是一种重要的无机材料,化学性质稳定,催化活性高,具有良好的耐光性、耐热性和对紫外线的屏蔽性,从某种工业酸性废液(主要含Na+、Fe2+、Fe3+、Mg2+、Al3+、Cl-、SO42-)中回收氧化铁流程如下:

已知:常温下Ksp[Mg(OH)2]=1.2×10-11;Ksp[Fe(OH)2]=2.2×10-16;Ksp[Fe(OH)3]=3.5×10-38;Ksp[Al(OH)3]=1.0×10-33
(1)写出在该酸性废液中通入空气时发生的离子反应方程式:___________,指出使用空气的优点是:_________。
(2)已知Fe3+(aq)+3OH-(aq)===Fe(OH)3(s)ΔH=-Q1kJ·mol-1,题(1)中每生成1 mol含铁微粒时,放热Q2,请你计算1 mol Fe2+全部转化为Fe(OH)3(s)的热效应ΔH=_________。
(3)常温下,根据已知条件计算在pH=5的溶液中,理论上下列微粒在该溶液中可存在的最大浓度c(Fe3+)=___________,c(Mg2+)=___________。
(4)有人用氨水调节溶液pH,在pH=5时将Fe(OH)3沉淀出来,此时Fe(OH)3沉淀中可能混有的杂质是______ (填化学式,下同),用_______试剂可将其除去。
查看答案和解析>>
科目: 来源: 题型:
【题目】苦艾精油由天然艾叶萃取精炼而成,中药常用于温经通络,益气活血,祛寒止痛等。现代科学从其中分离出多种化合物,其中四种的结构如下,下列说法正确的是
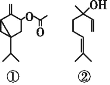
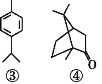
A.①②均能与氢氧化钠溶液反应
B.①②③均能使酸性高锰酸钾溶液褪色
C.②的分子式为C10H18O,与④互为同分异构体
D.④的一氯代物有5种
查看答案和解析>>
科目: 来源: 题型:
【题目】冬季下雪后,城市道路常使用融雪剂,其主要成分的 化学式为 XY2,X、Y 均为周期表前 20 号元素,其阳离子和阴离子电子层结构相同,且 1 mol XY2 含有 54 mol 电子。
(1)该融雪剂的化学式是___________,该物质中化学键类型是___________。
(2)元素 D、E 原子的最外层电子数是其电子层数的 2 倍,D 与 Y 相邻,则 D 的 离子结构示意图是___________;D 与 E 能形成一种结构类似于 CO2 的三原子 分子,且每个原子均达到了 8e-稳定结构,该分子的电子式为___________, 化学键类型为___________ (填“离子键”或“共价键”)。
(3)W 是与 D 同主族的短周期元素,Z 是第三周期金属性最强的元素,Z 的单质 在 W 的常见单质中反应时有两种产物:不加热时生成___________,其化学键类型为___________;加热时生成___________,其化学键类型为___________,电子式为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)如图是降冰片烷的碳架结构:
![]()
①其分子式为________。
②降冰片烷发生一氯取代时,取代位置有________种。
(2)“立方烷”是新合成的一种烃,其分子呈正方体结构,该分子的碳架结构如图所示:
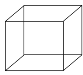
①“立方烷”的分子式为________。
②其一氯代物共有________种。
(3)写出分子中含碳碳叁键的2-甲基-1,3-丁二烯的所有的同分异构体________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)氨气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的 NO 和 NH3,在 一定条件下发生反应:6NO(g) + 4NH3(g)![]() 5N2(g) +6H2O(g)。
5N2(g) +6H2O(g)。
①能说明该反应已达到平衡状态的标志是 ___________
a.反应速率 v( NH3) =v( N2)
b.容器内压强不再随时间而发生变化
c.容器内 N2 的物质的量分数不再随时间而发生变化
d.容器内 n(NO)∶n(NH3)∶n(N2)∶n(H2O) = 6∶4∶5∶6
e.12molN-H 键断裂的同时生成 5mol N≡N 键
f.混合气体的总质量不随时间的变化而变化
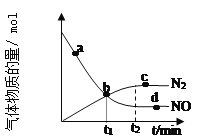
②某次实验中测得容器内 NO 及 N2 的物质的量随时间变化如图所示,图中 b 点 对应的速率关系是v(正) ___________ v(逆)(填﹥、﹤或﹦),d 点对应的速率关系是v(正) ___________ v(逆)
(填﹥、﹤或﹦)。
(2)298 K 时,若已知生成标准状况下 2.24LNH3时放出热量为 4.62kJ。写出合成氨反应的热化学方程式___________。在该温度下,取 1molN2和 3mol H2 放在一密闭容器中,在催化剂存在时进行反应。测得反应放出的热量总小于 92.4 kJ, 其原因是___________。
(3)一定条件下,在 2L密闭容器内,反应 2NO2(g)![]() N2O4(g) ΔH=-180 kJ·mol-1,n(NO2)随时间变化如下表:
N2O4(g) ΔH=-180 kJ·mol-1,n(NO2)随时间变化如下表:
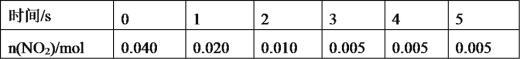
①用 N2O4 表示 0~2 s 内该反应的平均速率为__________。在第 5s 时,NO2 的转化 率为____________。(转化率是指某一反应物转化的百分率。)
②根据上表可以看出,随着反应进行,反应速率逐渐减小,其原因是______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某华人科学家和他的团队研发出“纸电池” (如图)。这种一面镀锌、一面镀二氧化锰的超薄电池在使用印刷与压层技术后,变成一张可任意裁剪大小的“电纸”,厚度仅为0.5毫米,可以任意弯曲和裁剪。纸内的离子“流过”水和氧化锌组成电解液,电池总反应式为: Zn+2MnO2+H2O=ZnO+2MnO(OH)。下列说法正确的是

A.该电池的正极材料为锌
B.该电池反应中二氧化锰发生了氧化反应
C.电池的正极反应式为2MnO2 +2H2O+2e-= 2MnO(OH)+2OH-
D.当有0.1mol锌溶解时,流经电解液的电子数为1.204×1023
查看答案和解析>>
科目: 来源: 题型:
【题目】A~I分别表示中学化学中常见的一种物质,它们之间相互关系如图所示(部分反应物、生成物没有列出)。且已知G为主族元素的固态氧化物,F是红褐色难溶于水的沉淀,A、B、C、D、E、F六种物质中均含同一种元素。
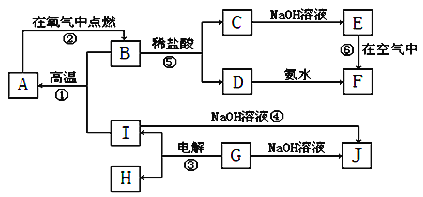
请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含同一种元素是___。
(2)写出C、G物质的化学式:C___,G___。
(3)写出④、⑥反应的化学方程式:
反应④:___;
反应⑥:___。
(4)从能量变化的角度看,①②③反应中属于吸热反应的是___。(填序号)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com