
科目: 来源: 题型:
【题目】钼酸钠(Na2MoO4)可与重金属盐产生沉淀,是目前应用较多的一种新型水处理剂。利用精钼矿![]() 主要成分是MoS2,含少量PbS等
主要成分是MoS2,含少量PbS等![]() 来制取钼酸钠晶体的工艺流程如下图所示。
来制取钼酸钠晶体的工艺流程如下图所示。
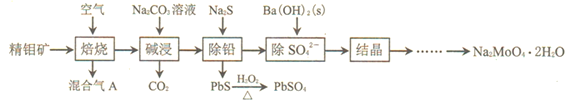
请回答下列问题:
⑴混合气A中含有一种大气污染物,其化学式为___________。
⑵焙烧的过程中采用如图1所示的“多层逆流焙烧”。
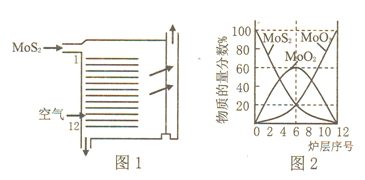
①多层逆流焙烧的优点是___________![]() 任答两点
任答两点![]() 。
。
②依据如图2,写出第6—12层MoO2参加反应的化学方程式___________。
⑶写出碱浸时发生反应的离子方程式___________。
⑷PbS与H2O2反应时,温度高于40℃后,反应速率反而减慢,原因是___________。
⑸流程图中“除SO42-”的过程中,当BaMoO4开始沉淀时,SO42-的去除率为97.0%,已知原Na2MoO4溶液中c(MoO42-)=0.48mol/L, c(SO42-)=0.040mol/L,Ksp(BaSO4) = 1.0×10-10,则Ksp(BaMoO4) = ___________。![]() 过程中溶液体积变化忽略不计
过程中溶液体积变化忽略不计![]()
⑹锂和二硫化钼形成的二次电池的总反应为:xLi + nMoS2![]() Lix(MoS2)n,则电池放电时的正极反应式是___________。
Lix(MoS2)n,则电池放电时的正极反应式是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法错误的是![]()
![]()
A.近年屡屡引起热议的“抗糖”一词中的“糖”,指的是六大营养物质之一的糖类,由C、H、O三种元素组成
B.培育绣球花的过程中,土壤为酸性时花朵呈蓝色,土壤为碱性时花朵呈红色。为获得红色花朵,可施用硫酸铵
C.“自热火锅”极大的方便了人们的生活,自热包的主要成分为CaO,加水后反应放热,从而加热火锅
D.《神农本草经》中记载:“石膏,味辛,微寒,主中风寒热,心下逆气惊喘。“石膏”的化学式为CaSO4·2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】向容积均为0.5L的甲、乙、丙三个密闭容器中分别充入一定量的A和B,发生反应:A(g)+xB(g)![]() 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别如图表所示:
2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别如图表所示:
容器 | 甲 | 乙 | 丙 |
温度/℃ | T1 | T2 | T2 |
反应物起始量 | 1.5molA 0.5molB | 1.5molA 0.5molB | 3.0molA 1.0molB |
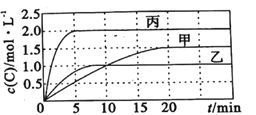
则: (1)该反应为____________(填 “放热反应”或“吸热反应”)
(2)丙容器中前5分钟的A的反应速率为__________
(3)该可逆反应达到平衡后,为在提高反应速率的同时提高B的转化率,可采取的措施有___________(填标号)。
a.按体积比1:1再充入A和B b.改用高效催化剂 c.升高温度 d.增加A的浓度 e. 增加C的浓度
(4)乙容器中的化学平衡常数为_____________
查看答案和解析>>
科目: 来源: 题型:
【题目】重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为FeOCr2O3,还含有硅、铝等杂质。制备流程如图所示:
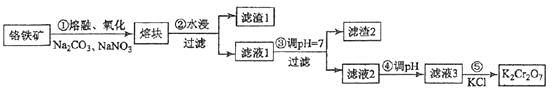
回答下列问题:
⑴步骤①的主要反应为:FeOCr2O3+Na2CO3+NaNO3![]() Na2CrO4 + Fe2O3 + CO2+ NaNO2
Na2CrO4 + Fe2O3 + CO2+ NaNO2
上述反应配平后FeOCr2O3与NaNO3的系数比为__________。该步骤不能使用陶瓷容器,原因是________________(可用化学方程式表示)。
⑵步骤④调滤液2的pH使之变_________(填“大”或“小”),原因是_________(用离子方程式表示)。
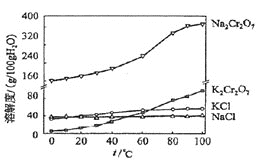
⑶有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,蒸发浓缩,冷却结晶,过滤得到K2Cr2O7固体。冷却到10℃得到的K2Cr2O7固体产品最多,步骤⑤的反应类型是___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】科学家研究出一种以天然气为燃料的“燃烧前捕获系统”,其简单流程如图所示(条件及物质未标出)。
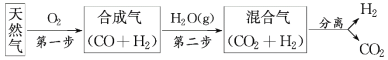
(1)已知:CH4、CO、H2的燃烧热分别为890.3 kJ·mol-1、283.0 kJ·mol-1、285.8 kJ·mol-1,则上述流程中第一步反应2CH4(g)+O2(g)===2CO(g)+4H2(g)的ΔH=____________。
(2)\在300 ℃、8 MPa下,将CO2和H2按物质的量之比1∶3 通入一密闭容器中发生反应CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),,达到平衡时,测得CO2的平衡转化率为50%,则该反应条件下的平衡常数表达式为K=________
CH3OH(g)+H2O(g),,达到平衡时,测得CO2的平衡转化率为50%,则该反应条件下的平衡常数表达式为K=________
(3)CO2经催化加氢可合成低碳烯烃:2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g) ΔH。在0.1 MPa时,按n(CO2)∶n(H2)=1∶3投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
C2H4(g)+4H2O(g) ΔH。在0.1 MPa时,按n(CO2)∶n(H2)=1∶3投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
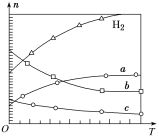
①该反应的ΔH________0(填“>”或“<”)。
②曲线c表示的物质为________。
③为提高H2的平衡转化率,除改变温度外,还可采取的措施是_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】2003年3月,日本筑波材料科学国家实验室一个研究小组发现首例带结晶水的晶体在 5K 下呈现超导性。报报道,该晶体中含有最简式为 CoO2的层状结构,结构如右图(小球表示Co原子,大球表示O原子)。
下列用粗线画出的CoO2层状结构的晶胞(晶胞是在晶体中具有代表性的最小重复单元)示意图不符合化学式的是
A.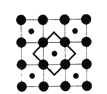 B.
B.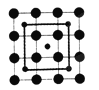
C.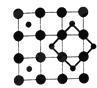 D.
D.
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验小组为探究![]() 漂白性的原因进行如下实验。已知
漂白性的原因进行如下实验。已知![]() 易溶于水,能溶于乙醇。
易溶于水,能溶于乙醇。![]() 的水溶液中存在下列平衡:
的水溶液中存在下列平衡:
![]()
![]() ;
;
![]()
![]() 。
。
实验室用亚硫酸钠粉末与硫酸制取![]() ,装置如图
,装置如图![]() 气密性良好
气密性良好![]() 。
。

(1)盛装![]() 的硫酸的仪器名称是________。使用
的硫酸的仪器名称是________。使用![]() 的硫酸比用
的硫酸比用![]() 的硫酸反应效果好,其原因是________。装置B的作用是________。
的硫酸反应效果好,其原因是________。装置B的作用是________。
(2)第一次实验:
C装置中混合溶液 | 品红的水溶液 | 品红的乙醇溶液 |
实验现象 | 红色褪去 | 无变化 |
从上述实验可知使品红水溶液褪色的微粒可能为________![]() 写出两种即可
写出两种即可![]() 。
。
(3)实验小组为进一步探究![]() 是使品红水溶液褪色的原因之一,进行第二次实验:取与第一次实验等体积等浓度的品红水溶液于装置C中,再加入少量NaOH固体,品红水溶液无明显变化,然后通入
是使品红水溶液褪色的原因之一,进行第二次实验:取与第一次实验等体积等浓度的品红水溶液于装置C中,再加入少量NaOH固体,品红水溶液无明显变化,然后通入![]() 气体,C装置中品红水溶液褪色。以上实验______
气体,C装置中品红水溶液褪色。以上实验______![]() 填“能“或“不能”
填“能“或“不能”![]() 证明
证明![]() 是使品红溶液褪色的原因之一,试用离子方程式说明理由:________。
是使品红溶液褪色的原因之一,试用离子方程式说明理由:________。
(4)请你设计探究![]() 是使品红水溶液褪色的原因之一的实验方案:________。
是使品红水溶液褪色的原因之一的实验方案:________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法错误的是( )
A. C2H6和C4H10一定是同系物B. C2H4和C4H8一定都能使溴水退色
C. C3H6不只表示一种物质D. 烯烃中各同系物中碳的质量分数相同
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,在恒容密闭容器中发生如下反应:2A(g)+B(g) 3C(g),若反应开始时充入2 mol A和2 mol B,达平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是( )
A. 1 mol B和3 mol C
B. 2 mol A、1mol B和1 mol He(不参加反应)
C. 1 mol B和1 mol C
D. 2 mol A、3mol B和3 mol C
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com