
科目: 来源: 题型:阅读理解
| 催化剂 |
| 水解 |
| 催化剂 |
| 发酵 |
| 催化剂 |
| 聚合 |
| 催化剂 |
| 催化剂 |
| 催化剂 |
| 发酵 |


查看答案和解析>>
科目: 来源: 题型:



| △ |
| △ |
| △ |
| △ |
| △ |
| △ |
查看答案和解析>>
科目: 来源: 题型:
 ),根据质量守恒定律,可判断出另一个反应产物为
),根据质量守恒定律,可判断出另一个反应产物为查看答案和解析>>
科目: 来源: 题型:
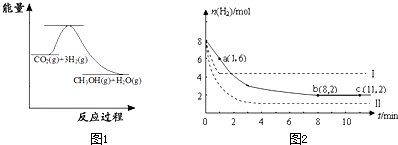
查看答案和解析>>
科目: 来源: 题型:
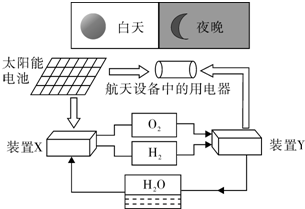 如图是一种航天器能量储存系统原理示意图.
如图是一种航天器能量储存系统原理示意图.查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
 我国的环境空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空气中所含二氧化硫的质量)限值如下表所示
我国的环境空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空气中所含二氧化硫的质量)限值如下表所示| 浓度限值(mg/m3) | ||
| 一级标准 | 二级标准 | 三级标准 |
| 0.15 | 0.50 | 0.70 |
查看答案和解析>>
科目: 来源: 题型:


查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com