
科目: 来源: 题型:
【题目】将1molCO和1molNO2充入密闭容器中,在催化剂存在下发生反应NO2(g)+CO(g)![]() CO2(g)+NO(g)并达到化学平衡,发现有50%的CO转化为CO2。在其它条件不变的情况下,若将1molCO和2molNO2充入上述反应器中,则反应达到化学平衡时,混合气体中CO2的体积分数是( )
CO2(g)+NO(g)并达到化学平衡,发现有50%的CO转化为CO2。在其它条件不变的情况下,若将1molCO和2molNO2充入上述反应器中,则反应达到化学平衡时,混合气体中CO2的体积分数是( )
A.1/9B.1/6C.2/9D.1/3
查看答案和解析>>
科目: 来源: 题型:
【题目】过渡金属元素氧化物的应用研究是目前科学研究的前沿之一,试回答下列问题:
Ⅰ.二氧化钛作光催化剂能将居室污染物甲醛、苯等有害气体可转化为二氧化碳和水,达到无害化.有关甲醛、苯、二氧化碳及水说法正确的是__。
A.苯与B3N3H6互为等电子体
B.甲醛、苯分子中碳原子均采用sp2杂化
C.苯、二氧化碳是非极性分子,水和甲醛是极性分子
D.水的沸点比甲醛高得多,是因为水分子间能形成氢键
Ⅱ.2007年诺贝尔物理学奖为法国科学家阿尔贝费尔和德国科学家彼得格林贝格尔共同获得,以表彰他们在巨磁电阻效应(CMR效应)研究方面的成就。某钙钛型复合氧化物(如图1),以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物具有CMR效应。
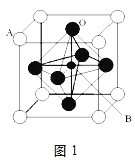
(1)用A、B、O表示这类特殊晶体的化学式:__。
(2)已知La为+3价,当被钙等二价元素A替代时,可形成复合钙钛矿化合物La1-xAxMnO3,(x<0.1),此时一部分锰转变为+4价。导致材料在某一温度附近有反铁磁-铁磁、铁磁-顺磁转变及金属-半导体的转变,则La1-xAxMnO3中三价锰与四价锰的物质的量之比为:__(用含x的代数式表示)。
(3)Mn的核外电子排布式为:___。
(4)下列有关说法正确的是___。
A.镧、锰、氧分别位于周期表f、d、p区
B.氧的第一电离能比氮的第一电离能大
C.锰的电负性为1.59,Cr的电负性为1.66,说明锰的金属性比铬强
D.铬的堆积方式与钾相同,则其堆积方式如图2:
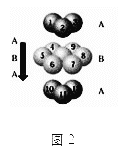
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁酸钾(K2FeO4)是新型多功能水处理剂。其生产工艺如下:

回答下列问题:
(1)反应①应在温度较低的情况下进行,因温度较高时NaOH与Cl2反应生成NaClO3,写出温度较高时反应的离子方程式____________。
(2)在溶液I中加入NaOH固体的目的是_______(填字母)。
A.与反应液I中过量的Cl2继续反应,生成更多的NaClO
B.NaOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供碱性的环境
D.使NaClO3转化为NaClO
(3)反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响。图1为不同的温度下,不同质量浓度的Fe(NO3)3对K2FeO4生成率的影响;图2为一定温度下,Fe(NO3)3质量浓度最佳时,NaClO浓度对K2FeO4的生成率的影响。

工业生产中最佳温度为_______,此时Fe(NO3)3与NaClO两种溶液的最佳质量浓度之比为_____。
(4)反应③中的离子反应方程式为_________________;溶液Ⅱ中加入饱和KOH得到湿产品的原因是__________________。
(5)高铁酸钾作为水处理剂是能与水反应其离子反应是:4FeO42-+l0H2O=4Fe(OH)3(胶体)十3O2↑+8OH-。则其作为水处理剂的原理是:①_______________;②_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某强酸性溶液X可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的一种或几种,取该溶液进行连续实验,实验过程如下:
中的一种或几种,取该溶液进行连续实验,实验过程如下:
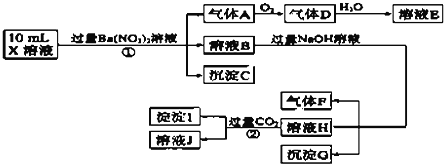
测定A、F、I均为![]() ,10mLX溶液中
,10mLX溶液中![]() ,沉淀C物质的量小于
,沉淀C物质的量小于![]() ,根据以上信息,下列说法正确的是
,根据以上信息,下列说法正确的是![]()
A.由实验![]() 可知,气体A一定是NO,沉淀C一定是
可知,气体A一定是NO,沉淀C一定是![]() ,原溶液中肯定含有
,原溶液中肯定含有![]()
B.溶液E和气体F不能发生化学反应
C.由实验![]() 可知,沉淀I可能是
可知,沉淀I可能是![]() 和
和![]()
D.原溶液中肯定含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,不能确定是否含有
,不能确定是否含有![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】下列解释工业生产或应用的化学用语中,不正确的是( )
A. FeCl3溶液刻蚀铜电路板:2Fe3+ + Cu==2Fe2++ Cu2+
B. 向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3·H2O== Al(OH)3↓ + 3NH4 +
C. 将少量二氧化碳通入次氯酸钠溶液中:CO2+H2O+2ClO-== CO32-+2HClO
D. Na2CO3溶液处理水垢:CaSO4(s)+CO32(aq)![]() CaCO3(s)+SO42(aq)
CaCO3(s)+SO42(aq)
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)写出以乙炔为原料制备![]() (聚氯乙烯)的过程中所发生的反应类型:____________、_____________。
(聚氯乙烯)的过程中所发生的反应类型:____________、_____________。![]() (聚乙烯)材料目前被公认为安全材料,也可用于制作保鲜膜和一次性餐盒。辨别
(聚乙烯)材料目前被公认为安全材料,也可用于制作保鲜膜和一次性餐盒。辨别![]() 和
和![]() 有三种方法,一是闻气味法:具有刺激性气味的是___________________;二是测密度法:密度大的应是___________________;三是燃烧法:
有三种方法,一是闻气味法:具有刺激性气味的是___________________;二是测密度法:密度大的应是___________________;三是燃烧法:![]() 的单体和
的单体和![]() 的单体在足量空气中燃烧的实验现象的明显区别是__________。
的单体在足量空气中燃烧的实验现象的明显区别是__________。
(2)![]() (
(![]() )是一种阻隔性高、韧性强、化学稳定性好的理想包装材料,广泛用于肉制品、豆制品等的包装。写出合成
)是一种阻隔性高、韧性强、化学稳定性好的理想包装材料,广泛用于肉制品、豆制品等的包装。写出合成![]() 的单体的同分异构体的结构简式_________。
的单体的同分异构体的结构简式_________。
(3) “白色污染”是指各种塑料制品对环境的污染。焚烧塑料会生成有毒物质二噁英,二噁英是含有如图所示母体的系列化合物,下列关于如图所示物质的说法不正确的是___________________(填序号)。

a.该物质在氧气中完全燃烧的产物是![]() 和
和![]()
b.该物质属于烃
c.该物质的一卤代物只有2种
查看答案和解析>>
科目: 来源: 题型:
【题目】A(C10H20O2)具有兰花香味,可用作香皂、洗发香波的芳香赋予剂。
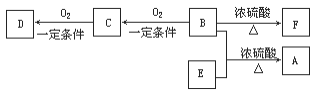
已知:
ⅰ.B分子中没有支链。
ⅱ.D能与碳酸氢钠溶液反应放出二氧化碳。
ⅲ.D、E互为具有相同官能团的同分异构体。E分子烃基上的氢若被Cl取代,其一氯代物只有一种。
ⅳ.F可以使溴的四氯化碳溶液褪色。
(1)B可以发生的反应有_______(选填序号)。
a.取代反应 b.加聚反应 c.消去反应 d.氧化反应
(2)D、F分子所含的官能团的结构简式依次是_______、________。
(3)写出与D、E具有相同官能团的一种同分异构体的结构简式___________。
(4)写出B和E反应生成A的化学方程式是_______________。
(5)写出C与新制Cu(OH)2反应的化学方程式_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】从环己烷可制备1,4-环己二醇,下列有关7步反应(其中无机产物都已略去),其中有3步属于加成反应。(提示:路线⑤的反应可利用1,3-环己二烯与Br2的1,4-加成反应)请回答下列问题:
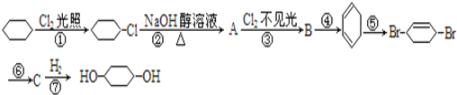
(1)分别写出B、C的结构简式:B_________________、C_________________。
(2)写出反应类型④_________________,⑤_________________,⑥_________________。
(3)写出反应①的化学方程式________________________________________________。(有机物写结构简式,并注明反应条件)
(4)写出反应②的化学方程式________________________________________________(有机物写结构简式,并注明反应条件)
(5)写出反应⑥的化学方程式________________________________________________(有机物写结构简式,并注明反应条件)
查看答案和解析>>
科目: 来源: 题型:
【题目】将反应2Fe3++2I-2Fe2++I2设计成如下图所示的原电池。

下列说法不正确的是( )
A.盐桥中的K+移向FeCl3溶液
B.反应开始时,乙中石墨电极上发生氧化反应
C.电流计读数为零时,反应达到化学平衡状态
D.电流计读数为零后,在甲中溶入FeCl2固体,乙中石墨电极为负极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com