
科目: 来源: 题型:
【题目】三种常见单萜类化合物的结构如下图所示。下列说法正确的是( )
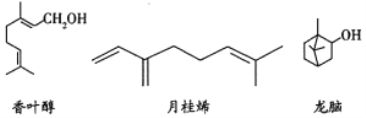
A. 香叶醇和龙脑互为同分异构体,分子式均为![]()
B. 可用金属钠鉴别香叶醇和月桂烯
C. 龙脑分子中所有碳原子在同一个平面上
D. 1mol月桂烯最多能与![]() 发生加成反应
发生加成反应
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,在体积为5L的密闭容器中,充入1mol A气体,发生如下可逆反应:2A(g)![]() B(g)+C(?),2min后反应达到平衡,A为0.4mol。当改变反应条件时符合如图的变化(P0表示1个大气压)。则下列叙述中不正确的是
B(g)+C(?),2min后反应达到平衡,A为0.4mol。当改变反应条件时符合如图的变化(P0表示1个大气压)。则下列叙述中不正确的是
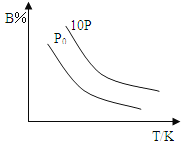
A.0~2min时间内B物质的平均反应速率为0.03mol/(L·min)
B.该反应的正反应是放热反应,且C为非气体物质
C.达到平衡后,保持温度和容器体积不变,再充入1mol A,平衡向正反应方向移动
D.若温度和容器体积不变,起始时充入B和C各0.5mol,则达到平衡时,n(A)小于0.4mol
查看答案和解析>>
科目: 来源: 题型:
【题目】药物瑞德西韦(Remdesivir)对新冠病毒有明显抑制作用,化合物M是合成瑞德西韦的中间体,下列关于M的说法错误的是( )
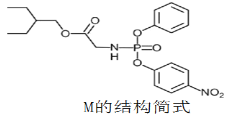
A.核磁共振氢谱共有10个吸收峰
B.分子中含有3种含氧官能团
C.分子中N原子一个是sp2杂化,一个是sp3杂化
D.1mol该物质与足量NaOH溶液反应时可以得到4种有机化合物
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、W为原子序数递增的四种短周期元素,其中Z为金属元素,X、W为同一主族元素。X、Z、W分别与Y形成的最高价化合物为甲、乙、丙。结合如图转化关系,下列判断错误的是( )

A.反应③可用于工业上制取W的单质
B.X位于元素周期表第二周期ⅣA族
C.非金属性:X>W
D.工业上通过电解乙来制取Z的单质
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁钢轨全部为无缝钢轨,钢轨焊接可以采用铝热法,其原理如图所示。下列叙述错误的是( )

A.铝热法炼铁的原理是
B.该实验需要关注的安全事项之一是纸漏斗与盛沙子的蒸发皿的距离不要太远,否则熔融的铁水易溅出伤人
C.点燃镁条,镁条剧烈燃烧,放出大量的热,使氧化铁粉末和铝粉在较高的温度下发生剧烈的反应
D.![]() 和
和![]() 的质量比要控制在
的质量比要控制在![]() ,且要混合均匀,以保证
,且要混合均匀,以保证![]() 和
和![]() 都能完全反应
都能完全反应
查看答案和解析>>
科目: 来源: 题型:
【题目】有一溶液,其中可能含有Fe3+、Al3+、Fe2+、Mg2+、Cu2+、NH4+、K+、CO32-、SO42-、Br- 等离子的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如图所示:
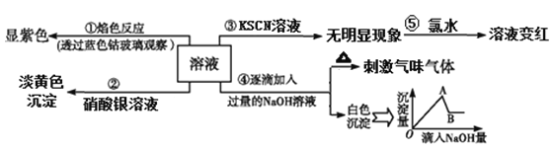
请你根据上图推断:
(1)实验①、②能确定原溶液中一定存在________和_______(填离子符号);
(2)实验⑤中所发生的氧化还原的离子方程式为__________________________________。
(3)实验④中产生的刺激性气味的气体,工人常利用该物质的浓溶液检查氯气管道是否漏气,反应的化学方程式是_______________________________________________
(4)写出实验④中,由A→B过程中所发生反应的离子方程式:________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:0.5 ℃,有毒)常温下是一种黄色气体,遇水易水解。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成,并以液态储存。

(1)甲组的同学拟制备原料气NO和Cl2,均采用上图制备装置:
①写出NOCl的N元素化合价:_______
②为制备纯净干燥的气体,下表中缺少的药品是(填写在横线上):
实验项目 | 装置Ⅰ | 装置Ⅱ | |
制备的气体 | 烧瓶中 | 分液漏斗中 | |
a .制备纯净干燥的Cl2 | MnO2 | _______ | _______ |
b .制备纯净干燥的NO | Cu | _______ | _______ |
(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:
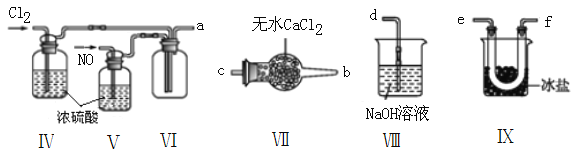
①装置连接顺序为a→____________________________(按气流自左向右方向,用小写字母表示)。
②装置Ⅳ、Ⅴ除可进一步干燥NO、Cl2外,另一个作用是______________________________。
③装置Ⅵ在实验结束,拆解装置前,应作怎样的处理?_________________________。
④装置Ⅷ中吸收尾气时,NOCl发生的非氧化还原反应的化学方程式为___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,1mol化学键断裂形成气态原子所需要的能量用![]() 表示。结合表中信息判断下列说法不正确的是( )
表示。结合表中信息判断下列说法不正确的是( )
共价键 | H-H | F-F | H-F | H-Cl | H-I |
E(kJ/mol) | 436 | 157 | 568 | 432 | 298 |
A. 432kJ/mol>E(H-Br)>298kJ/mol B. 表中最稳定的共价键是H-F键
C. H2(g)→2H(g) △H=+436kJ/mol D. H2(g)+F2(g)=2HF(g) △H=-25kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】兴趣小组探究SO2气体还原Fe3+、I2,它们使用的药品和装置如图所示:
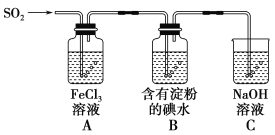
(1)SO2气体和Fe3+反应的氧化产物、还原产物分别是________、________
(2)下列实验方案适用于在实验室制取所需SO2的是________。
A.Na2SO3溶液与HNO3 B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧 D.铜与浓H2SO4共热
(3)装置C的作用是__________________________________________________。
(4)装置B中反应的离子方程式_________________________________________________。
(5)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入酸性KMnO4溶液,紫红色褪去。
方案②:往第二份试液中加入NaOH溶液,产生白色沉淀,并迅速转为灰绿,最后呈红褐色。
方案③:往第三份试液中加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是方案_____,原因是__________________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com