
科目: 来源: 题型:
【题目】硝酸生产中,500 ℃时,NH3和O2可能发生如下反应:
①4NH3 (g)+5O2(g) ![]() 4NO(g)+6H2O(g)ΔH=-9072 kJ·mol-1 K=1.1×1026
4NO(g)+6H2O(g)ΔH=-9072 kJ·mol-1 K=1.1×1026
②4NH3(g)+4O2(g) ![]() 2N2O(g)+6H2O(g)ΔH=-1104.9 kJ·mol-1 K=4.4×1028
2N2O(g)+6H2O(g)ΔH=-1104.9 kJ·mol-1 K=4.4×1028
③4NH3(g)+3O2(g) ![]() 2N2 (g)+6H2O(g)ΔH=-1269.02 kJ·mol-1 K=7.1×1034
2N2 (g)+6H2O(g)ΔH=-1269.02 kJ·mol-1 K=7.1×1034
其中,②、③是副反应。若要减少副反应,提高单位时间内NO的产率,最合理的措施是( )
A.增大O2浓度
B.使用合适的催化剂
C.减小压强
D.降低温度
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与社会、生活密切相关,对下列现象或事实的解释正确的是( )
现象或事实 | 解释 | |
A | 用热的纯碱溶液去油污 | Na2CO3可直接与油污反应 |
B | 漂白粉在空气中久置变质 | 漂白粉中的CaCl2与空气中的CO2反应生成CaCO3 |
C | 施肥时,草木灰(主要成分K2CO3)不能与NH4Cl混合使用 | K2CO3与NH4Cl在潮湿的土壤中会反应生成氨气,降低肥效 |
D | FeCl3溶液可用于铜质印刷线路板制作 | Cu能从FeCl3溶液中把铁还原为游离态 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,体积和pH都相同的盐酸和AlCl3溶液加水稀释时的pH变化曲线如图,下列有关说法正确的是( )
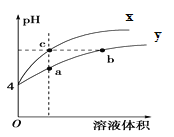
A.Al(OH)3的电离方程式为:Al(OH)3=Al3++3OH-
B.a点溶液中有: c(H+)+c(Al3+)=c(OH-) +3c(Cl-)
C.曲线X表示盐酸稀释过程的pH变化
D.b、c两溶液c(OH-)及c(Cl-)均相等
查看答案和解析>>
科目: 来源: 题型:
【题目】由乙烯推测丙烯的结构或性质,正确的是( )
A.分子中3个碳原子在同一直线上
B.分子中所有原子都在同一平面上
C.分子中共价键的夹角均为120°
D.分子中共价键数为8,其中有一个碳碳双键
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法或有关化学用语的表达正确的是
A. 1s电子云呈球形,表示电子绕原子核做圆周运动
B. 钠原子由1s22s22p63p1→ls22s22p63p1时,原子释放能量,由基态转化成激发态
C. 因氧元素的电负性比氮元素的大,故氧原子的第一电离能比氮原子的大
D. 基态Fe原子的外围电子排布图为
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中不正确的是( )
①通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动
②氢氧化铁胶体能稳定存在的主要原因是胶体带正电
③氨溶于水得到溶液氨水能导电,所以氨水是电解质;
④电解质放在水中一定能导电,非电解质放在水中一定不导电。
⑤Na2SO3是弱酸盐,所以它是弱电解质
A.①④B.①④⑤C.①②③④D.①②③④⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】根据如图所示电化学实验装置图,回答有关问题。

(1)若只闭合S1,该装置属于_______,能量转化形式为_______,锌极作_______极。
(2)若只闭合S2,该装置属于_______,能量转化形式为_______,锌极上的电极反应式为_______。
(3)若只闭合S3,该装置属于_______,铜极作_______极,锌极上的电极反应式为_______,总反应的化学方程式为_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验装置和方法进行相应实验,能达到实验目的是( )

A.装置A用于检验1-溴丙烷的消去产物
B.装置B用于石油的分馏
C.装置C用于实验室制硝基苯
D.装置D用于除去甲烷中混有的乙烯
查看答案和解析>>
科目: 来源: 题型:
【题目】改革开放40年,“发展与保护”的方针使我国在取得了很多世界瞩目的科技成果的同时,文物也得到了很好的保护。下列说法不正确的是( )
|
|
|
|
A.蛟龙号潜水器用到钛合金,22号钛元素属于过渡元素 | B.港珠澳大桥水下钢柱镶锌块的防腐方法为牺牲阳极的阴极保护法 | C.除锈剂使有锈迹的银器见新,是化学变化 | D.变形的金属香炉整形复原,是化学变化 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】镍及其化合物用途广泛。某矿渣的主要成分是NiFe2O4(铁酸镍)、NiO、FeO、CaO、SiO2等,如下图是从该矿渣中回收NiSO4的工艺路线:
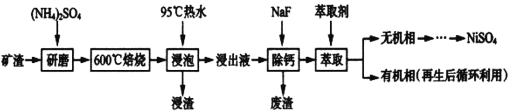
已知:(NH4)2SO4在350℃以上会分解生成NH3和H2SO4,NiFe2O4在焙烧过程中生成NiSO4、Fe2(SO4)3。锡(Sn)位于第五周期第IVA族。
(1)焙烧前将矿渣与(NH4)2SO4混合研磨,混合研磨的目的是_______________。
(2)“浸泡”过程中Fe2(SO4)3生成FeO(OH)的离子方程式为_________________________,“浸渣”的成分除Fe2O3、FeO(OH)外还含有___________________(填化学式)。
(3)为保证产品纯度,要检测“浸出液”的总铁量:取一定体积的浸出液,用盐酸酸化后,加入SnCl2将:Fe3+还原为Fe2+,所需SnC12的物质的量不少于Fe3+物质的量的_____倍:除去过量的SnCl2后,再用酸性K2Cr2O7标准溶液滴定溶液中的Fe2+,还原产物为Cr3+,滴定时反应的离子方程式为_________________________________________。
(4)“浸出液”中c(Ca2+)=1.0×10-3mol·L-1,当除钙率达到99%时,溶液中c(F-)=___mol· L-1。[已知KSP(CaF2)=4.0×10-11]
(5)已知正十二烷可用作该工艺的萃取剂。用电化学制备正十二烷的方法为:向烧杯中加入50mL甲醇,不断搅拌加入少量金属钠,再加入11mL正庚酸搅拌均匀,装好铂电极,接通电源反应,当电流明显减小时切断电源,然后提纯正十二烷。已知电解总反应为:2C6H13COONa+2CH3OH![]() C12H26+2CO2↑+H2↑+2CH3ONa,则阳极的电极反应式为______________________________________
C12H26+2CO2↑+H2↑+2CH3ONa,则阳极的电极反应式为______________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com