
科目: 来源: 题型:阅读理解
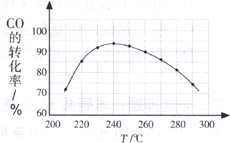 (2010?广州一模)二甲醚(CH3OCH3)在未来可能替代柴油和液化气作为洁净液体燃料使用.
(2010?广州一模)二甲醚(CH3OCH3)在未来可能替代柴油和液化气作为洁净液体燃料使用.| c(CH3OCH3)?c(CO2) |
| c3(CO)?c3(H2) |
| c(CH3OCH3)?c(CO2) |
| c3(CO)?c3(H2) |
查看答案和解析>>
科目: 来源: 题型:
| 8.8×10-3V |
| m |
| 8.8×10-3V |
| m |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 实验要求 | 选项 |
| 除去食盐中少量沙子(SiO2) | |
| 除去食盐中I2 | |
| 证明地瓜粉中含有淀粉 | |
| 证明Na2CO3溶液呈碱性 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com