
科目: 来源: 题型:
【题目】一定温度下在一容积不变的密闭容器中发生可逆反应2X(g) ![]() Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是( )
Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是( )
A. 混合气体的密度不再变化 B. 反应容器中Y的质量分数不变
C. X的分解速率与Y的消耗速率相等 D. 单位时间内生成1 mol Y的同时生成2 mol X
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:2M(g)![]() N(g);△H <0。现将M和N的混和气体通入体积为1L的恒温密闭容器中,反应体系中物质浓度随时间变化关系如右图所示。下列说法正确的是( )
N(g);△H <0。现将M和N的混和气体通入体积为1L的恒温密闭容器中,反应体系中物质浓度随时间变化关系如右图所示。下列说法正确的是( )

A.a、b、c、d四个点中处于平衡状态的点是a、b、d
B.反应进行至25min时,曲线发生变化的原因是加入了 0.4molN
C.若调节温度使35min时体系内N的百分含量与15min时相等,应升高温度
D.若40min后出现如图所示变化,则可能是加入了某种催化剂
查看答案和解析>>
科目: 来源: 题型:
【题目】I .甲、乙、丙3位同学,在已知盐酸是强酸的基础上,通过实验验证醋酸是弱酸,分别设计了如下实验方案:
甲:分别准确配制0.1 mol/L的盐酸和醋酸各250 mL,再用pH试纸分别测定两溶液的pH。
乙:分别准确配制0.1 mol/L的盐酸和醋酸各250 mL。各取出20 mL于锥形瓶中,逐滴加入0.1 mol/L标准NaOH溶液(不需配制),分别记录恰好中和时用去NaOH溶液的体积。
丙:分别准确配制pH=1的盐酸和醋酸各250 mL。各取出10 mL加水稀释到100 mL后比较稀释后溶液的pH。回答下列问题:
(1)甲同学的实验结果为盐酸和醋酸的pH分别为pH1和pH2,则pH1_____pH2(填“>”“<”或“=”),所以此实验方案________(填“可行”或“不可行”)。
(2)乙同学的实验结果为盐酸和醋酸分别用去NaOH溶液V1 mL和V2 mL,则V1____V2(填“>”“<”或“=”),所以此实验方案______(填“可行”或“不可行”)。
(3)丙同学的实验方案不可行的原因是____________________________________。
II. 测定Na2S2O3样品纯度。
取10.0 g Na2S2O3·5H2O样品,配成 250mL溶液,准确量取25.00 mL溶液,以淀粉作指示剂,用0.1000 mol·L-1碘的标准溶液滴定。三次平行实验测得的数据如下:
实验序号 | 消耗标准溶液体积/mL |
1 | 19.98 |
2 | 17.90 |
3 | 18.10 |
已知:2Na2S2O3+I2=Na2S4O6+2NaI
①滴定终点的颜色为__________________。
②该Na2S2O3·5H2O样品的纯度为___%(保留2位小数)(已知Na2S2O3·5H2O的M=248g mol·-1)。
③若样品中含Na2SO3(还原性:SO32->I-),则测得的结果_______(填“偏高”“偏低”或“无影响”)
查看答案和解析>>
科目: 来源: 题型:
【题目】已知 25 ℃时部分弱电解质的电离平衡常数数据如下表:
化学式 | HSCN | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.3×10-1 | 1.8×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | 3.0×10-8 |
回答下列问题:
(1)写出碳酸的主要的电离方程式_________________。若将碳酸饱和溶液稀释10 倍,则稀释后的溶液中 c(H+)______原来的十分之一(填“大于”、“小于”或“等于”).
(2)物质的量浓度均为 0.1mol/L 的五种溶液:pH 由小到大的顺序为_______(用编号填写)。
a.CH3COONa b. Na2CO3 c. NaClO d.NaHCO3 e.NaSCN
(3)常温下,有浓度均为1 mol·L-1的下列4种溶液:①H2SO4溶液②NaHCO3溶液③NH4Cl溶液④NaOH溶液,其中由水电离的H+浓度由大到小的顺序是__________。(均填序号)
(4)常温下,几种弱电解质的pK(pK=-lg K)如下表所示:
电解质 | H3BO3 | CH3NH2 | HN3 | H2CrO4 |
pK | 9.3 | 3.4 | 4.7 | pK1=0.74,pK2=6.5 |
请回答下列问题:
①硼酸(H3BO3)在水中存在电离平衡:H3BO3+H2O![]() B(OH)4-+H+。由此推断,硼酸是___(填字母)。
B(OH)4-+H+。由此推断,硼酸是___(填字母)。
a.一元酸 b.三元酸 c.强酸 d.弱酸
②常温下,在H3BO3、HN3、H2CrO4中酸性最强的是______________(填化学式)。
③H2CrO4的二级电离常数表达式Ka2=_________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列叙述正确的是
4NO(g)+6H2O(g),下列叙述正确的是
A.达到化学平衡时,4v正(O2) = 5v逆(NO)
B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D.化学反应速率关系是:2v正(NH3) = 3v正(H2O)
查看答案和解析>>
科目: 来源: 题型:
【题目】恒温恒容下.将l molX和2 molY置于密闭容器中发生反应:X(s)+2Y(g)![]() 2Z(g),10 min后达到平衡状态,下列说法正确的是
2Z(g),10 min后达到平衡状态,下列说法正确的是
A. 平衡前,容器中压强随反应进行而减小
B. 平衡后,容器中Y和Z的物质的量之比一定为1:1
C. 10 min后,升高温度,Y的反应速率不变
D. 生成Z的物质的量一定小于2 moI
查看答案和解析>>
科目: 来源: 题型:
【题目】已知水电离平衡如图所示,且pOH=-lg c(OH-)。下列说法错误的是
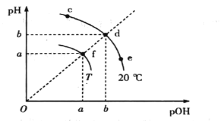
A.各点对应的水的离子积:Kw(f)>Kw(e)=Kw(d)
B.加热f点纯水,其组成由f点沿fd直线向d方向迁移
C.向c点溶液中通入少量HCl,其组成由c点沿cde曲线向e点移动
D.df直线上各点对应的水溶液(或纯水)一定显中性
查看答案和解析>>
科目: 来源: 题型:
【题目】稀氨水中存在着下列平衡:NH3·H2O![]() NH4++OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入的物质或采取的措施是( )
NH4++OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入的物质或采取的措施是( )
①NH4Cl固体 ②硫酸 ③NaOH固体 ④水 ⑤加热 ⑥少量MgSO4固体
A. ①②③⑤B. ③C. ③④⑥D. ③⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】已知反应:2NO2(红棕色)![]() N2O4(无色)△H<0。将一定量的NO2充入注射器中并密封,改变活塞位置的过程中,气体透光率随时间的变化如图所示(气体颜色越深,透光率越小)。下列说法不正确的是( )
N2O4(无色)△H<0。将一定量的NO2充入注射器中并密封,改变活塞位置的过程中,气体透光率随时间的变化如图所示(气体颜色越深,透光率越小)。下列说法不正确的是( )

A. b点达到平衡状态
B. b点与a点相比,c(NO2)、c(N2O4)均减小
C. d点:v(正)<v(逆)
D. 若在c点将温度降低,其透光率将增大
查看答案和解析>>
科目: 来源: 题型:
【题目】在一个不传热的固定容积的密闭容器中可逆反应![]() 当m、n、p、q为任意整数时,达到平衡的标志是
当m、n、p、q为任意整数时,达到平衡的标志是
①体系的压强不再改变
②体系的温度不再改变
③各组分的浓度不再改变
④各组分的质量分数不再改变
⑤反应速率v(A):v(B):v(C):v(D)=m:n:p:q
⑥单位时间内m mol A断键反应,同时pmol C也断键反应。
A.③④⑤⑥B.②③④⑥C.①③④⑤D.①③④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com