
科目: 来源: 题型:
【题目】某学生用0.100 mol·L-1的NaOH标准溶液滴定未知浓度的盐酸,其操作可分解为如下几步:
A.移取20.00 mL待测盐酸溶液注入洁净的锥形瓶,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液;
D.取标准NaOH溶液注入碱式滴定管至刻度“0”以上2~3 mL;
E.调节液面至“0”或“0”以下刻度,记下读数;
F.把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定至终点并记下滴定管液面的刻度。
回答下列问题:
(1)正确操作步骤的顺序是(用字母序号填写)_________。
(2)排去碱式滴定管中气泡的方法应采用下图操作中的________(填标号),然后轻轻挤压玻璃球使尖嘴部分充满碱液。

(3)滴定过程中,眼睛应注视______________。
(4)判断到达滴定终点的实验现象是__________________。
(5)数据记录如下:
滴定次数 | 待测盐酸的体积/mL | 标准NaOH溶液体积 | |
滴定前的刻度/mL | 滴定后的刻度/mL | ||
第一次 | 20.00 | 0.40 | 20.50 |
第二次 | 20.00 | 4.10 | 24.00 |
第三次 | 20.00 | 1.00 | 24.00 |
根据上述数据,可计算出该盐酸的浓度约为_____________(保留小数点后两位数)。
(6)在上述实验中,下列操作(其他操作正确)会造成测定结果偏低的有_____(填字母)。
A.酸式滴定管使用前,水洗后未用待测盐酸润洗
B.锥形瓶水洗后未干燥
C.碱式滴定管尖嘴部分有气泡,滴定后消失
D.滴定终点读数时俯视读数
E.滴定终点读数时仰视读数
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,等体积、c(H+)相同的盐酸和醋酸溶液分别加水稀释,溶液中的c(H+)随溶液体积变化的曲线如图所示。据图判断下列说法正确的是
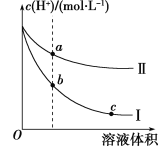
A.曲线Ⅱ表示的是盐酸的变化曲线
B.b点溶液的导电性比c点溶液的导电性强
C.取等体积的a点、b点对应的溶液,消耗的NaOH的量相同
D.b点酸的总浓度大于a点酸的总浓度
查看答案和解析>>
科目: 来源: 题型:
【题目】关于0.1mol/L Na2CO3溶液,下列判断不正确的是
A.粒子种类与NaHCO3溶液相同
B.升高温度,c(CO32-)增大
C.加入CaCl2溶液,c(CO32-)减小
D.c(H+)+c(Na+)=2c(CO32-)+c(HCO3-)+c(OH-)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A.基于硫代硫酸钠与稀硫酸反应生成S和![]() ,在定量测定反应速率时,既可用S对标记遮盖法,也可用排水法测
,在定量测定反应速率时,既可用S对标记遮盖法,也可用排水法测![]() 体积,计算出其反应速率
体积,计算出其反应速率
B.将两块未擦去氧化膜的铝片分别投入![]() 溶液、
溶液、![]() 溶液中,一段时间后,铝片表面都观察不到明显的反应现象
溶液中,一段时间后,铝片表面都观察不到明显的反应现象
C.将20g硝酸钠和17g氯化钾放入100mL烧杯中,加35mL水,并加热、搅拌,使溶液浓缩至约为原来的一半时,趁热过滤即可得到硝酸钾晶体
D.试管内壁附着的硫黄可以用热的KOH溶液洗涤,也可以用![]() 洗涤
洗涤
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,用 0.1000 mol·L![]() NaOH溶液滴定 20.00mL0.1000 mol·L
NaOH溶液滴定 20.00mL0.1000 mol·L![]()
![]() 溶液所得滴定曲线如图。下列说法正确的是
溶液所得滴定曲线如图。下列说法正确的是

A.点①所示溶液中:![]()
B.点②所示溶液中:![]()
C.点③所示溶液中:![]()
D.滴定过程中可能出现:![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】下列化学实验事实及其解释或结论都正确的是![]()
![]()
A.向浓度均为![]() 的
的![]() 、
、![]() 混合溶液中逐滴加入氨水,先生成蓝色沉淀,说明
混合溶液中逐滴加入氨水,先生成蓝色沉淀,说明![]()
B.取少量溶液X,向其中加入适量新制氯水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有![]()
C.向![]() 溶液中加入KI溶液,有白色沉淀生成,再加入四氯化碳振荡,四氯化碳层呈紫色,白色沉淀可能为CuI
溶液中加入KI溶液,有白色沉淀生成,再加入四氯化碳振荡,四氯化碳层呈紫色,白色沉淀可能为CuI
D.某待测溶液可能含有等浓度的下列离子中的若干种:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 。现取少量待测溶液于试管,加入足量NaOH溶液得到白色沉淀,加热产生无色气体,则原溶液中是否含有
。现取少量待测溶液于试管,加入足量NaOH溶液得到白色沉淀,加热产生无色气体,则原溶液中是否含有![]() 、
、![]() ,需通过焰色反应确定
,需通过焰色反应确定
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关同分异构体数目的叙述中,正确的是( )
A.戊烷有2种同分异构体
B.C8H10中只有3种属于芳香烃的同分异构体
C.甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种
D.CH3CH2CH2CH3光照下与氯气反应,只生成1种一氯代烃
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:![]() 时
时
化学式 |
|
|
|
电离平衡常数 |
|
|
|
下列说法正确的是 ( )
A. 醋酸稀释过程中,![]() 逐渐减小
逐渐减小
B. ![]() 溶液中:
溶液中:![]()
C. 向醋酸或HCN溶液中加入![]() ,均产生
,均产生![]()
D. 物质的量浓度相同时![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】已知几种盐溶液的pH如表所示:
① | ② | ③ | |
均为0.1 mol·L-1溶液 | NaHCO3 | Na2CO3 | NaClO |
常温下溶液pH | 9.7 | 11.6 | 10.3 |
下列说法正确的是
A.三种溶液中水的电离程度:①>③>②
B.每种溶液都只存在1种微粒的电离平衡
C.①与②中均存在:c(CO32-)+c(HCO3-)+c(OH-)=c(Na+)+c(H+)
D.向NaClO溶液中通入少量CO2的反应为ClO-+CO2+H2O=HClO+HCO3-
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关实验操作、现象和结论都正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 向稀硝酸中加入过量的铁粉充分反应后,滴入KSCN溶液 | 溶液变为血红色 |
|
B | 向盛有某溶液的试管中滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口 | 试纸颜色无明显变化 | 原溶液中无 |
C | 向淀粉溶液中加入稀硫酸,加热,冷却后加入新制 | 未见红色沉淀 | 淀粉未发生水解 |
D | 向含有酚酞的 | 溶液红色变浅 | 证明 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com