
科目: 来源: 题型:
【题目】低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:2NH3(g)+NO(g)+NO2(g)![]() 2N2(g)+3H2O(g) ΔH<0。在恒容的密闭容器中,下列有关说法正确的是( )
2N2(g)+3H2O(g) ΔH<0。在恒容的密闭容器中,下列有关说法正确的是( )
A.单位时间内消耗NO和N2的物质的量比为1∶2时,反应达到平衡
B.平衡时,其他条件不变,升高温度可使该反应的平衡常数增大
C.平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小
D.其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大
查看答案和解析>>
科目: 来源: 题型:
【题目】铟产业被称为“信息时代的朝阳产业”。元素周期表中铟的数据见图,下列说法完全正确的是
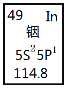
A.铟元素的质量数是114.8
B.铟元素的相对原子质量是115,中子数为66
C.铟元素是一种主族元素,位于第五周期第ⅢA族
D.铟原子最外层有3个能量相同的电子
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组为研究上述反应中钾元素的熔出率(液体中钾元素的质量占样品质量的百分率)与温度的关系,进行实验(保持其它条件不变),获得数据曲线如图。
主要反应是:NaCl(l)+KAlSi3O8(s)KCl(l)+NaAlSi3O8(s)+Q;
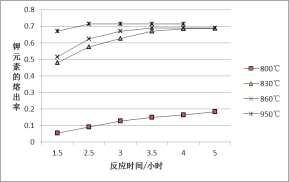
(1)分析数据可知,Q_______0(选填“>”或“<”)。
(2)950℃时,欲提高钾的熔出速率可以采取的措施是_______(填序号)。
a.延长反应时间 b.充分搅拌
c.增大反应体系的压强 d.将钾长石粉粹成更小的颗粒
(3)要使钾元素的熔出率和熔出速率都达到最大,反应温度应为_____________。
(4)工业上常用KCl冶炼金属钾。反应方程式为:Na(l)+KCl(l)![]() NaCl(l)+K(g)用平衡移动原理解释该方法可行的原因:_________________。
NaCl(l)+K(g)用平衡移动原理解释该方法可行的原因:_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,体积一定的密闭容器中进行如下反应:X(g)+Y(g)![]() Z(g)+W(s) ΔH>0,下列叙述不正确的是
Z(g)+W(s) ΔH>0,下列叙述不正确的是
A. 在容器中加入氩气,反应速率不变
B. 加入少量W,逆反应速率不变
C. 升高温度,正反应速率增大,逆反应速率减小
D. 将容器的体积压缩,可增大单位体积内活化分子数,有效碰撞次数增大
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度范围内用氯化钠熔浸钾长石(主要成份为KAlSi3O8)可制得氯化钾,主要反应是:NaCl(l)+KAlSi3O8(s)![]() KCl(l)+NaAlSi3O8(s) △H=-Q kJ/mol。
KCl(l)+NaAlSi3O8(s) △H=-Q kJ/mol。
(1)写出Cl原子的核外电子排布式_______, NaCl的熔点比KCl______ (选填“高”或“低”)。
(2)指出钾长石中存在的化学键类型__________________。
(3)上述反应涉及的位于同一周期的几种元素中,有一种元素的最高价氧化物的水化物和其余元素的最高价氧化物的水化物均能发生反应,该元素是_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学设计实验如图所示:
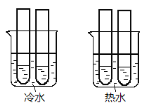
(1)两个烧杯中的试管都分别盛有2 mL 0.1mol/LH2C2O4溶液和4 mL 0.1 mol/L 酸性KMnO4溶液,分别混合并振荡,记录溶液褪色所需时间。该实验目的是研究____________,但该实验始终没有看到溶液褪色,推测原因________________。
(2)已知草酸(H2C2O4)受热分解的化学方程式为:H2C2O4 → H2O+CO↑+CO2↑,写出FeC2O4在密闭容器中高温分解的化学方程式____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】以天然气、焦炭、水为初始原料,可以制得CO和H2,进而人工合成汽油。(流程示意图如下,反应③的H2也由反应①得到。)
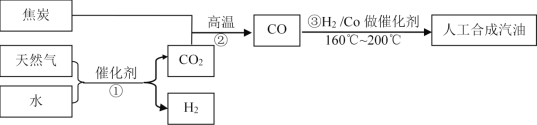
若反应①、②、③的转化率均为100%,且将反应①中得到的CO2和H2全部用于合成人工汽油。
(1)通过计算说明上述方案能否得到理想的产品_______________。
(2)当CO2的使用量应控制为反应①中CO2产量的______________(填比例范围),可以得到理想的产品。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列不能用勒夏特列原理解释的事实是( )
A. 氯水中有下列平衡:Cl2+H2O![]() HCl+HClO,光照后氯水颜色变浅
HCl+HClO,光照后氯水颜色变浅
B. 合成氨工业使用高压以提高氨的产量
C. 对于H2(g)+I2(g)![]() 2HI(g),达平衡后,缩小容器体积可使体系颜色变深
2HI(g),达平衡后,缩小容器体积可使体系颜色变深
D. 汽水型饮料打开瓶盖后产生大量气体
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:环己烯可以通过1,3-丁二烯与乙烯发生环化加成反应得到:
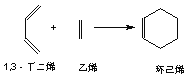
实验证明,下列反应中,反应物分子的环外双键比环内双键更容易被氧化:
![]()
![]()
![]()
现仅以1,3-丁二烯为有机原料,无机试剂任选,按下列途径合成甲基环己烷:

(1)写出结构简式: A _____________;B ______________
(2)加氢后产物与甲基环己烷互为同系物的是_____________
(3)1 mol A与1 mol HBr加成可以得到___________种产物。
查看答案和解析>>
科目: 来源: 题型:
【题目】肉桂酸是香料、化妆品、医药、塑料和感光树脂等的重要原料.实验室用下列反应制取肉桂酸.
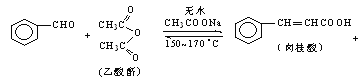 CH3COOH
CH3COOH
药品物理常数
苯甲醛 | 乙酸酐 | 肉桂酸 | 乙酸 | |
溶解度(25℃,g/100g水) | 0.3 | 遇热水水解 | 0.04 | 互溶 |
沸点(℃) | 179.6 | 138.6 | 300 | 118 |
填空:
合成:反应装置如图所示.向三颈烧瓶中先后加入研细的无水醋酸钠、苯甲醛和乙酸酐,振荡使之混合均匀. 在150~170℃加热1小时,保持微沸状态.
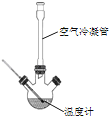
(1)空气冷凝管的作用是__.
(2)该装置的加热方法是__.加热回流要控制反应呈微沸状态,如果剧烈沸腾,会导致肉桂酸产率降低,可能的原因是______.
(3)不能用醋酸钠晶体(CH3COONa3H2O)的原因是______.
粗品精制:将上述反应后得到的混合物趁热倒入圆底烧瓶中,进行下列操作:
反应混合物![]()
![]()
![]()
![]()
![]() 肉桂酸晶体
肉桂酸晶体
(4)加饱和Na2CO3溶液除了转化醋酸,主要目的是_______.
(5)操作I是__;若所得肉桂酸晶体中仍然有杂质,欲提高纯度可以进行的操作是__(均填操作名称).
(6)设计实验方案检验产品中是否含有苯甲醛_______.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com