
科目: 来源: 题型:
【题目】铜板上铁铆钉长期暴露在潮湿的空气中,形成一层酸性水膜后铁铆钉会被腐蚀,示意图如图所示。下列说法不正确的是
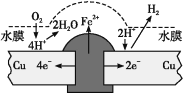
A.因铁的金属性比铜强,所以铁铆钉被氧化而腐蚀
B.若水膜中溶解了SO2,则铁铆钉腐蚀的速率变小
C.铜极上的反应是2H++2e =H2↑、O2+4e+4H+=2H2O
D.在金属表面涂一层油脂,能防止铁铆钉被腐蚀
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:①CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1=-Q1②H2(g)+![]() O2(g)=H2O(g) ΔH2=-Q2③H2(g)+
O2(g)=H2O(g) ΔH2=-Q2③H2(g)+![]() O2(g)=H2O(l) ΔH3=-Q3。常温下取体积比为4∶1的甲烷和氢气共11.2 L(已折合成标准状况)经完全燃烧恢复到常温,放出的热量为( )
O2(g)=H2O(l) ΔH3=-Q3。常温下取体积比为4∶1的甲烷和氢气共11.2 L(已折合成标准状况)经完全燃烧恢复到常温,放出的热量为( )
A.0.4Q1+0.05Q2B.0.4Q1+0.1Q2C.0.4Q1+0.05Q3D.0.4Q1+0.1Q3
查看答案和解析>>
科目: 来源: 题型:
【题目】共价化合物分子中各原子有一定的连接方式,某分子可用球棍模型表示如图,A的原子半径最小,C、D位于同周期,D的常见单质常温下为气态,下列说法正确的是( )
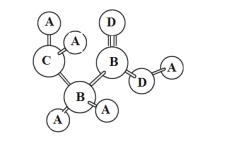
A.B的同素异形体数目最多2种
B.A与C不可以形成离子化合物
C.通过含氧酸酸性可以比较元素B和C的非金属性
D.C与D形成的阴离子CD2-既有氧化性,又有还原性
查看答案和解析>>
科目: 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是( )
A.氨水应密闭保存,置低温处
B.将铜粉和锌粉混合后放入稀硫酸中,产生气体的速率比不加铜粉快
C.黄绿色的氯水光照后颜色变浅
D.常温下,用水稀释烧碱溶液pH会降低
查看答案和解析>>
科目: 来源: 题型:
【题目】图中的曲线是表示其他条件一定时,2NO(g)+O2(g)2NO2(g) ΔH<0反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v正>v逆的点是( )

A.a点
B.b点
C.c点
D.d点
查看答案和解析>>
科目: 来源: 题型:
【题目】碘化钠在医疗及食品方面有重要的作用。实验室用NaOH、单质碘和水合肼(N2H·H2O)为原料制备碘化钠。已知:水合肼具有还原性。回答下列问题:
(1)水合肼的制备有关反应原理为:CO(NH2)2(尿素)+NaClO+2NaOH![]() N2H4·H2O+NaCl+Na2CO3
N2H4·H2O+NaCl+Na2CO3
①制取次氯酸钠和氧氧化钠混合液的连接顺序为__________(按气流方向,用小写字母表示)。
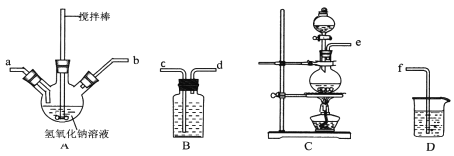
若该实验温度控制不当,反应后测得三颈瓶内ClO-与ClO3-的物质的量之比为5:1,则氯气与氢氧化钠反应时,被还原的氯元素与被氧化的氯元素的物质的量之比为________。
②制备水合肼时,应将___________滴到 __________ 中(填“NaClO溶液”或“尿素溶液”),且滴加速度不能过快。
(2)碘化钠的制备采用水合肼还原法制取碘化钠固体,其制备流程如图所示:
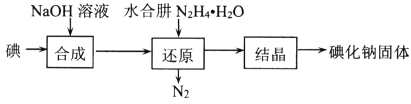
在“还原”过程中,主要消耗反应过程中生成的副产物IO3-,该过程的离子方程式为______________________________________。工业上也可以用硫化钠或铁屑还原碘酸钠制备碘化钠,但水合肼还原法制得的产品纯度更高,其原因是_________________________________。
(3)测定产品中NaI含量的实验步骤如下:
a.称取10.00g样品并溶解,在500mL容量瓶中定容;
b.量取25.00mL待测液于锥形瓶中,然后加入足量的FeCl3溶液,充分反应后,再加入M溶液作指示剂:
c.用0.2100mol·L-1的Na2S2O3标准溶液滴定至终点(反应方程式为;2Na2S2O3+I2=Na2S4O6+2NaI),重复实验多次,测得消耗标准溶液的体积为15.00mL。
①M为____________(写名称)。
②该样品中NaI的质量分数为_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】难溶盐CaCO3在下列溶液中溶解度最大的是( )
A.0.1 mol·L-1CH3COOHB.0.10 mol·L-1CaSO4C.纯水D.1.0 mol·L-1Na2CO3
查看答案和解析>>
科目: 来源: 题型:
【题目】锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是

A. 铜电极上发生氧化反应
B. 电池工作一段时间后,甲池的c(SO42-)减小
C. 电池工作一段时间后,乙池溶液的总质量增加
D. 阴阳离子离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
查看答案和解析>>
科目: 来源: 题型:
【题目】某校学生用如图所示装置进行实验,以探究苯与溴发生反应的原理并分离提纯反应的产物,请回答下列问题:

请回答下列问题:
(1)冷凝管所起的作用为冷凝回流和导气,冷凝水从_______口进入(填“a”或“b”)。
(2)实验开始时,关闭K2、开启K1和分液漏斗活塞,滴加苯和液溴的混合液,反应开始。III中小试管内苯的作用是_________________________。
(3)能说明苯与液溴发生了取代反应的现象是____________________。
(4)反应结束后,要让装置Ⅰ中的水倒吸入装置Ⅱ中,这样操作的目的是_________________,简述这一操作的方法:________________________________。
(5)将三颈烧瓶内反应后的液体依次进行下列实验操作就可得到较纯净的溴苯。
①用蒸馏水洗涤,振荡,分液;②用5%的NaOH溶液洗涤,振荡,分液;
③用蒸馏水洗涤,振荡,分液;④加入无水CaCl2粉末干燥;⑤____________(填操作名称)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com