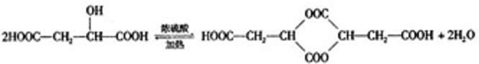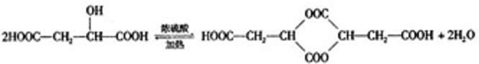(2010?南宁一模)(1)已知pH=2的高碘酸(H
5IO
6)溶液与Ph=12的NaOH溶液等体积混合,所得混台液显酸性;则高碘酸是
弱酸
弱酸
(填“强酸”或“弱酸”),理由是:
由于高碘酸溶液的c(H+)与NaOH溶液的c(OH-)相等,二者等体积混合后,混合液显酸性,说明酸过量,原高碘酸溶液中只有一部分高碘酸的分子发生了电离,所以高碘酸是弱酸
由于高碘酸溶液的c(H+)与NaOH溶液的c(OH-)相等,二者等体积混合后,混合液显酸性,说明酸过量,原高碘酸溶液中只有一部分高碘酸的分子发生了电离,所以高碘酸是弱酸
.
已知0.01mol?L
-1的碘酸( HIO
6))或高锰酸(HMnO
4)溶液与pH=12的NaOH溶液等体积混合,所得混合液显中性,且知高碘酸和硫酸锰( MnSO
4)在溶液中反应生成高锰酸、碘酸和硫酸,则此反应的离子方程式是
5H5IO6+2Mn2+=11H++MnO4-+5IO3-+7H2O
5H5IO6+2Mn2+=11H++MnO4-+5IO3-+7H2O
.
(2)体积不变的密闭容器内部有一不漏气且可滑动的话塞将容器分成左右两个室,左室内充入一定体积的CO和H
2O气体,右室充入SO
2和O
2两种气体共4mol,且SO
2和O
2的物质的量之比为2:1,左右两室内各可发生如下反应:
左室 CO(g)+H
2O(G)?CO
2(g)+H
2(g);△H<0
右室 2SO
2(g)+O
2(g)?2SO
3(g);△H<0

反应开始时活塞停留在离左端点
处,反应在恒温下进行,当达平衡状态时,活塞处于容器中间.反应达平衡时,生成SO
32
2
mol,此时若再向左室中充入与原物质的量之比相同的CO和H
2O气体,则达到新平衡时CO的物质的量分数
不变
不变
,SO
2的物质的量分数
减小
减小
.(填“不变”或“变小”或“变大”)