
科目: 来源: 题型:
| 浓硝酸 |
| 一定量NaOH |
| D的溶液 |
查看答案和解析>>
科目: 来源: 题型:

| Cl2 |
| 高温 |
| 一定条件 |
| +CO、H2 |
| 水 |
| 水 |




查看答案和解析>>
科目: 来源: 题型:
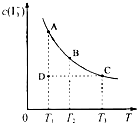 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq);某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下列说法中不正确的是( )
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq);某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下列说法中不正确的是( )查看答案和解析>>
科目: 来源: 题型:
 下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( ) 下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
|
查看答案和解析>>
科目: 来源: 题型:
 实验室用50mL 0.50mol?L-1盐酸、50mL 0.55mol?L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到表中的数据:
实验室用50mL 0.50mol?L-1盐酸、50mL 0.55mol?L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到表中的数据:| 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | NaOH溶液 | ||
| 1 | 20.2 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com