某化学实验小组同学为了证明、比较SO
2和氯水的漂白性,设计了如图1所示的实验装置.
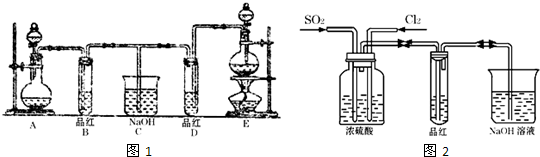
(1)实验室常选用制CO
2的发生装置制SO
2,实验室用MnO
2跟浓盐酸反应制备Cl
2时,应选用上图A、E两发生装置中
E
E
装置(填装置序号)制Cl
2,通过
分液漏斗
分液漏斗
(填写仪器名称)向烧瓶中加入适量的浓盐酸,反应离子方程式为
:MnO
2+4H
++2Cl
-Mn
2++Cl
2↑+2H
2O
:MnO
2+4H
++2Cl
-Mn
2++Cl
2↑+2H
2O
.
(2)反应开始后,发现B、D两个试管中的品红溶液都褪去,停止通气后,给B、D两个试管加热,两个试管中的现象分别为B:
溶液由无色变成红色
溶液由无色变成红色
,D:
溶液没有明显变化
溶液没有明显变化
.
(3)甲乙两名同学分别利用如图2所示装置探究两种气体按不同比例混合后的漂白性.试分析:
①在气体进入品红溶液之前,先将SO
2和Cl
2通过盛有浓硫酸装置的目的是:
使两种气体充分混合,通过观察气泡的速度控制气体流量,使二者按一定比列混合
使两种气体充分混合,通过观察气泡的速度控制气体流量,使二者按一定比列混合
.
②甲同学在实验过程中发现:通气一段时间后,品红溶液几乎不褪色,其原因是:
SO2和Cl2按1:1进气,二者恰好完全反应,生成无漂白性的H2SO4和HCl,SO2+Cl2+2H2O═H2SO4+2HCl
SO2和Cl2按1:1进气,二者恰好完全反应,生成无漂白性的H2SO4和HCl,SO2+Cl2+2H2O═H2SO4+2HCl
(结合反应方程式).

 取等物质的量浓度的NaOH溶液两份A和B,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1 mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题:
取等物质的量浓度的NaOH溶液两份A和B,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1 mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题: