
科目: 来源: 题型:
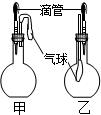 (2009?黄浦区二模)如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球的影响).则滴管和烧瓶中所用试剂可能是( ) (2009?黄浦区二模)如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球的影响).则滴管和烧瓶中所用试剂可能是( )
|
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
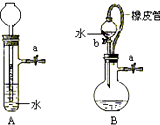 根据如图及描述,回答下列问题:
根据如图及描述,回答下列问题:查看答案和解析>>
科目: 来源: 题型:


查看答案和解析>>
科目: 来源: 题型:
 某工业废水中含有Ba2+,Cu2+,Ag+,选择合适试剂,将这三种离子逐一沉淀分离.其流程图如下:
某工业废水中含有Ba2+,Cu2+,Ag+,选择合适试剂,将这三种离子逐一沉淀分离.其流程图如下:| Ba2+ | Cu2+ | Ag+ | |
| Cl- | 溶 | 溶 | 不 |
| CO32- | 不 | 不 | 不 |
| SO42- | 不 | 溶 | 不 |
| S2- | 溶 | 不 | 不 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com