
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:阅读理解
| 步骤编号 | 实验操作 | 预期现象和结论 |
| ① | 在试管中加入2mllmol/L氯化铁,观察溶液颜色,加热一段时间. 在试管中加入2mllmol/L氯化铁,观察溶液颜色,加热一段时间. |
加热后溶液颜色变深.说明升温促进氯铁水解, 生成更多的氢氧化铁胶体. 加热后溶液颜色变深.说明升温促进氯铁水解, 生成更多的氢氧化铁胶体. |
| ② | 在上述溶液中通入HCl气体 在上述溶液中通入HCl气体 |
上述溶液颜色变浅.说明加入酸使平衡左移,酸抑制氯化铁水解. 上述溶液颜色变浅.说明加入酸使平衡左移,酸抑制氯化铁水解. |
| ③ | 用量筒取10mllmol/L氯化铁于烧杯中,用pH计测出pH值.另取90ml蒸馏水加入烧杯,充分搅拌,再用pH计测出pH值. 用量筒取10mllmol/L氯化铁于烧杯中,用pH计测出pH值.另取90ml蒸馏水加入烧杯,充分搅拌,再用pH计测出pH值. |
前后测得pH值之差小于1.说明加水稀释后平衡右移,生成更多的H+.故增大氯化铁浓度,不利其水解. 前后测得pH值之差小于1.说明加水稀释后平衡右移,生成更多的H+.故增大氯化铁浓度,不利其水解. |
无 无 |
无 无 | |
| … | … | … |
查看答案和解析>>
科目: 来源: 题型:阅读理解
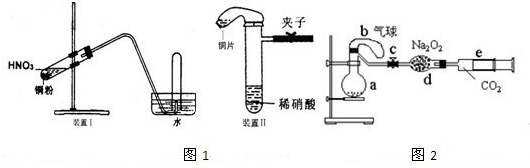
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com