
科目: 来源: 题型:
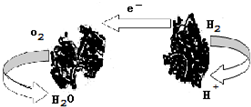 如图为一种新型的生物燃料电池,它有两个涂覆着酶的电极,处于充满空气和少量氢气的玻璃槽中,由于气体可以混合从而省去了昂贵的燃料隔离膜.下列对其工作原理叙述正确的是( )
如图为一种新型的生物燃料电池,它有两个涂覆着酶的电极,处于充满空气和少量氢气的玻璃槽中,由于气体可以混合从而省去了昂贵的燃料隔离膜.下列对其工作原理叙述正确的是( )查看答案和解析>>
科目: 来源: 题型:
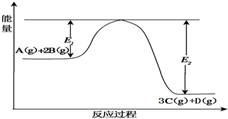 某可逆反应过程能量变化如图所示,下列说法中正确的是( )
某可逆反应过程能量变化如图所示,下列说法中正确的是( )| A、该反应热化学方程式为:A(g)+2B(g)?3C(g)+D(g)△H>0 | B、其它条件不变,升高温度,A的转化率增大 | C、其它条件不变,增大压强,释放热量减少,平衡常数K减小 | D、其它条件不变,加催化剂,反应速率增大,E1和E2均减小,△H不变 |
查看答案和解析>>
科目: 来源: 题型:
| 放电 |
| 充电 |
| A、放电时,Mo3S4发生氧化反应 |
| B、放电时,正极反应式:Mo3S4+2xe-→Mo3S42x- |
| C、充电时,Mg2+向阴极迁移 |
| D、充电时,阴极反应式:xMg2++2xe-→xMg |
查看答案和解析>>
科目: 来源: 题型:
| ||
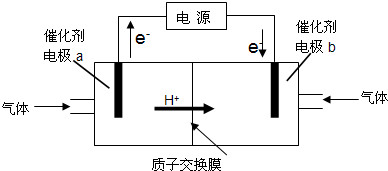
查看答案和解析>>
科目: 来源: 题型:
 依据氧化还原反应:
依据氧化还原反应:查看答案和解析>>
科目: 来源: 题型:
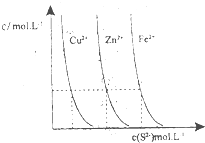 以下是对化学反应变化过程及结果的研究.按要求回答问题:
以下是对化学反应变化过程及结果的研究.按要求回答问题:| 弱酸化学式 | CH3COOH | HCN | H2CO |
| 电离平衡常数(25℃) | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K1=5.6×10-11 |
| 放电 |
| 通电 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 13 | 2 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com