
科目: 来源: 题型:
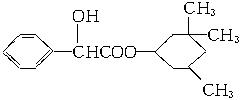
A.该物质属于芳香烃
B.该有机物难溶于水
C.分子式为C17H23O3
D.1 mol该物质最多可与2 mol NaOH发生反应
查看答案和解析>>
科目: 来源: 题型:
A.含有核电荷数和质子数相等的微粒一定是原子
B.标准状况下,
C
D.O、S、Se的氢化物中,稳定性最好的其沸点也最高
查看答案和解析>>
科目: 来源: 题型:
A.向Na2CO3溶液中加入少量NaHCO3的固体,溶液pH减小
B.某化学反应的ΔH<0、ΔS<0,则该反应一定是自发反应
C.由水电离出的c(H+)=10-14 mol·L-1的溶液中:Na+、![]() 、Cl-、
、Cl-、![]() 能大量共存
能大量共存
D.已知热化学方程式2SO2(g)+O2(g) ![]() 2SO3(g) ΔH=-Q kJ·mol-1(Q>0),则将2 mol SO2(g)和1 mol O2(g)置于一密闭容器中充分反应后放出Q kJ的热量
2SO3(g) ΔH=-Q kJ·mol-1(Q>0),则将2 mol SO2(g)和1 mol O2(g)置于一密闭容器中充分反应后放出Q kJ的热量
查看答案和解析>>
科目: 来源: 题型:
A
B.纯水在
C.在NH3+NO![]() N2+H2O反应中,被还原和被氧化的N原子数
N2+H2O反应中,被还原和被氧化的N原子数
D.pH相同的等体积的盐酸和醋酸分别与足量锌粒反应产生的气体体积
查看答案和解析>>
科目: 来源: 题型:
肉桂醛(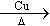 )在自然界中存在于桂油中,是一种常用的植物调味油,工业主要用CH2=CH2和甲苯为主要原料进行合成:
)在自然界中存在于桂油中,是一种常用的植物调味油,工业主要用CH2=CH2和甲苯为主要原料进行合成:
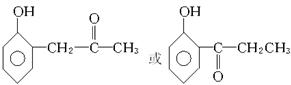
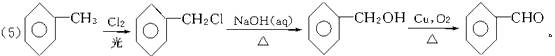
请回答:
(1)E中含氧官能团的名称是_____________________。
(2)反应①—④中属于加成反应的是____________________________________。
(3)反应②的化学方程式是____________________________________。
(4)写出符合下列要求的E的同分异构体的结构简式(写出一种即可)__________________。
a.遇FeCl3溶液显紫色
b.苯环上有两个取代基
c.不能发生银镜反应
d.除苯环外不存在其他的环状结构
e.不存在C=C
(5)用流程图表示出由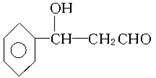 制备
制备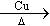 的方案,例如:
的方案,例如:
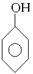 。
。
查看答案和解析>>
科目: 来源: 题型:
请完成下列各题:
(1)前4周期中,基态原子中未成对电子数为4的元素原子的电子排布式为________________。
(2)NaCl晶体中,与Na+等距离且最近的Na+有________________个。
(3)N 原子的第一电离能___________(填 “>”“<” 或“=”)O原子的第一电离能,N2分子中存在_______个σ键和_______个π键,NH3的沸点比PH3_________(填“高”或“低”),![]() 中N原子的杂化方式为________________,
中N原子的杂化方式为________________,![]() 的空间构型为________________。
的空间构型为________________。
查看答案和解析>>
科目: 来源: 题型:
(1)工业纯碱中含少量NaCl,若实验室只提供盐酸、天平、蒸发皿、玻璃棒、铁架台(带铁夹、铁圈),请设计一个方案,测定纯碱样品的纯度。_____________________。
(2)过碳酸钠(Na2CO4)中含有少量Na2O2,已知:2Na2CO4+2H2SO4![]() 2Na2SO4+2CO2↑ + O2↑ +2H2O为测定其纯度,甲、乙两位同学各称取m g该样品选用下列图示仪器药品进行实验,甲的仪器连接顺序是①⑦③⑥④ ,乙同学是①②。
2Na2SO4+2CO2↑ + O2↑ +2H2O为测定其纯度,甲、乙两位同学各称取m g该样品选用下列图示仪器药品进行实验,甲的仪器连接顺序是①⑦③⑥④ ,乙同学是①②。
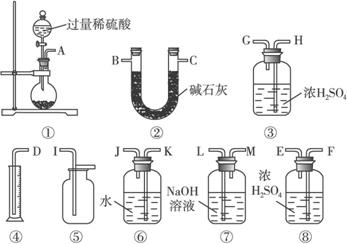
请回答下列问题:
①甲同学想通过实验测得的数据是________________,他使用装置③________________(填“有”或“没有”)必要。
②乙同学想测得的数据是________________。
③考虑到装置①中的水蒸气和空气中的水蒸气都会被装置②吸收,按乙测得的数据计算出的结果不准确,为此,请你帮助乙同学将实验装置进行改进,要求只能选用上列仪器,且每种仪器最多只能使用一次,写出各仪器接口的连接顺序________________。
④按你设计的实验装置进行实验,若所得实验前后装置②的质量分别是w
⑤由于受到仪器的限制,你帮乙改进后的装置所测得的过碳酸钠的质量分数仍稍偏低, 其原因是________________________________________________。
查看答案和解析>>
科目: 来源: 题型:阅读理解
(1)工业高炉炼铁采用焦炭、铁矿石等于高炉中共热,并鼓入适量空气,让高温下产生的CO气体还原铁矿石制得铁。这种方法不可避免地混入了非金属单质——碳。纯铁的抗腐蚀能力相当强,而铁碳合金却易发生电化腐蚀。
①写出钢铁发生吸氧腐蚀时的正极反应____________________________________。
②为保护钢铁制品不被腐蚀,可采用的电化学防护方法是(答出一种电化学防护方法的名称)____________________________________。
(2)焊接无缝钢轨时常采用铝热反应制备铁,中学教材中也有Al和Fe2O3的铝热反应实验。
①有人推测,铝热反应实验中所得熔融物中可能混有Al。若用一个简单实验证明含Al,则应选用的试剂是____________,能证明含铝的现象是__________________________。
②若经实验证实熔融物含铝,欲将该熔融物完全溶解,下列试剂中最适宜的是____________(填序号)。
A.浓硫酸 B.稀硫酸
C.稀HNO3 D.NaOH溶液
③实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低,直到还原成铵根离子(![]() )。某同学取一定量熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中逐滴加入4 mol·L-1的NaOH溶液,所加NaOH溶液的体积(mL) 与产生沉淀的物质的量(mol)的关系如图所示:
)。某同学取一定量熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中逐滴加入4 mol·L-1的NaOH溶液,所加NaOH溶液的体积(mL) 与产生沉淀的物质的量(mol)的关系如图所示:

试回答下列问题:
Ⅰ.图中DE段沉淀的物质的量没有变化,此段发生反应的离子方程式为_________________。
Ⅱ.通过图象判断溶液中的离子结合OH-能力最强的是________________,最弱的是________________。
Ⅲ.EF段反应的离子方程式是________________,A与B 的差值是________________mol。
查看答案和解析>>
科目: 来源: 题型:
![]()
(1)若A 是一种溶液,其溶质由三种不同短周期元素构成,这三种元素中有两种处于同一主族,且三种元素原子的最外层电子数之和为8,则X的化学式可能为____________、____________(填两种不同类别的物质);若此时X为一种18电子的分子, 则C的化学式为____________,在B的溶液中加入新制的AgCl悬浊液,白色浑浊立即变成黑色浑浊,由此现象可以得出的结论是____________________________________。
(2)若A是一种10电子分子,B在通常情况下遇X即生成C,又知
(3)若A是一种黄色的固体非金属单质,则反应②的化学方程式是_________________。
某温度T时,在一定条件下的
①物质B的转化率____________________________________。
②该温度下反应②的平衡常数____________________________________。
③在上述相同的条件下,向相同的容器中投入2 mol C,请在右下图中画出从反应开始至t2时间达到平衡后各物质的物质的量与时间的关系图。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com