
科目: 来源: 题型:
(9分)
某科研小组在实验室合成SO3的反应为![]() 。现在如图所示体积可变的密闭容器中充入1.0molSO2和0.5molO2。已知反应前气体的总体积为5.0L,在等温条件下得到平衡时,测得气体的密度为20g·L-1 。
。现在如图所示体积可变的密闭容器中充入1.0molSO2和0.5molO2。已知反应前气体的总体积为5.0L,在等温条件下得到平衡时,测得气体的密度为20g·L-1 。
(1)求SO3在平衡混合气体中的体积分数;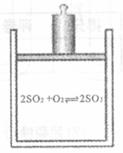
(2)求该条件下反应![]() 的平衡常数。
的平衡常数。
查看答案和解析>>
科目: 来源: 题型:
用盐酸与碳酸钙固体反应时,能使反应速率明显加快的是
A.用大块状碳酸钙固体而不用小块状碳酸钙固体 B.温度升高10 0C
C.将盐酸改为硫酸 D.盐酸的量增加一倍
查看答案和解析>>
科目: 来源: 题型:
下列
各组反应(表内物质均为反应物)刚开始时,放出H2的速率最大的是
| 编号 | 金属(粉末状) | 物质的量 | 酸的浓度 | 酸的体积 | 反应温度 |
| A | Mg | 0.1mol | 6mol/L硝酸 | 10mL | 60℃ |
| B | Mg | 0.1mol | 3mol/L盐酸 | 10mL | 30℃ |
| C | Fe | 0.1mol | 3mol/L盐酸 | 10mL | 60℃ |
| D | Mg | 0.1mol | 3mol/L盐酸 | 10mL | 60℃ |
查看答案和解析>>
科目: 来源: 题型:
在一定温度下,向a L某恒容密闭容器中加入1mol X气体和2mol Y气体,发生如下反应:X(g)+2Y(g) ![]() 2Z(g),此反应达到平衡的标志是
2Z(g),此反应达到平衡的标志是
A.容器内气体密度不随时间变化
B.v正(X): v逆(Y)= l:2
C.容器内X、Y、Z的浓度之比为1:2:2
D.单位时间消耗0.1 molX同时生成0.2molZ
查看答案和解析>>
科目: 来源: 题型:
将ag块状的碳酸钙与足量的盐酸反应,反应体系内损失的质量随时间t的变化曲线如图中的实线所示。在相同条件下,再取a g粉末状碳酸钙与同浓度的盐酸反应,则相应的曲线如图中的虚线所示。其中正确的是

查看答案和解析>>
科目: 来源: 题型:
实验室用锌粒与2mol/L硫酸溶液制取氢气,下列措施不能增大产生氢气的速率的是
A.用锌粉代替锌粒 B.改用热的2mol/L硫酸溶液
C.改用3mol/L的硫酸溶液 D.改用18mol/L的浓硫酸
查看答案和解析>>
科目: 来源: 题型:
在恒温下的定容密闭容器中,反应2SO2+O2![]()
![]() 2SO3已经达到平衡状态的标志是
2SO3已经达到平衡状态的标志是
A.容器中SO2、O2和SO3共存
B.SO2和SO3的物质的量浓度相等
C.容器中的SO2、O2、SO3的物质的量之比为2:1:2
D.反应器内压强不再变化
查看答案和解析>>
科目: 来源: 题型:
四位同学同时进行反应A+3B==2C+2D的速率测定实验,分别测得反应速率如下,其中反应进行得最快的是
A.V(A)=0.15mol·(L·s )-1 B.V(B)= 0.6mol·(L·s )-1[
C. V(C)=0.4mol·(L·s )-1 D.V(D)= 0.45mol·(L·s )-1
查看答案和解析>>
科目: 来源: 题型:
(10分)在25℃时,向100mL含氯化氢14.6g的盐酸溶液里放入5.60g纯铁粉(不考虑反应前后溶液体积的变化),反应开始至2min末,收集到1.12L(标准状况)氢气,在此之后,又经过4min,铁粉完全溶解,则:
(1)在前2min内用FeCl2表示的平均反应速率是____________
(2)在后4min内用HCl表示的平均反应速率是______________
(3)前2min与后4min相比,反应速率较快的是_____________________________________________,其原因是__________________________________________。
(4)反应结束后,溶液中Cl-的物质的量浓度为________________。
查看答案和解析>>
科目: 来源: 题型:
2SO2(g)+O2(g)![]() 2SO3(g)是制备硫酸的重要反应。下列叙述正确的是
2SO3(g)是制备硫酸的重要反应。下列叙述正确的是
A.催化剂V2O5不改变该反应的逆反应速率
B.增大反应体系的压强,反应速率一定增大
C.该反应是放热反应,降低温度将缩短反应达到平衡的时间
D.在t1、t2时刻,SO3(g)的浓度分别是c1,c2,则时间间隔t1~t2内,SO3(g)生成的平均速率为![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com