
科目: 来源: 题型:
(12分)21世纪是钛的世纪。下面是利用钛白粉(TiO2)生产海绵钛(Ti)的一种工艺流程:
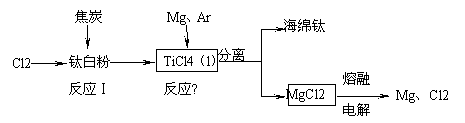 |
已知:
① Mg(s)+Cl2 (g)=MgCl2 (s) △H=-641 kJ·mol-1
② Cl2(g)+1/2Ti (s)=1/2TiCl4 (l) △H=-385 kJ·mol-1
(1)钛白粉是利用TiO2+发生水解生成钛酸(H2TiO3)沉淀,再煅烧沉淀制得的。TiO2+发生
水解的离子方程式为 。
(2)反应Ⅰ在800~900℃下进行,还生成一种可燃性无色气体,该反应的化学方程式
 为 ;反应Ⅱ的热化学方程式为 。
为 ;反应Ⅱ的热化学方程式为 。
(3)该工艺流程中,可以循环使用的物质有 。
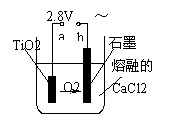
(4)在800℃~1000℃时电解TiO2也可制得海绵钛,装置如右
图所示。图中b是电源的 极,阴极的电极反应式为 。
查看答案和解析>>
科目: 来源: 题型:
(9分)工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤。
(1)某温度下,SO2(g)+1/2O2(g)![]() SO3(g);△H==-98kJ/mol。开始时在100L的密闭容器中加
SO3(g);△H==-98kJ/mol。开始时在100L的密闭容器中加
入4.0molSO2(g)和10.0molO2(g),当反应达到平衡时共放出热量196kJ,该温度下平衡常数
K=____________________
(2)一定条件下,向一带有活塞的密闭容器中充入2molSO2(g)和1molO2(g),发生下列反应:
2SO2(g)+O2(g)![]() 2SO3(g)达到平衡后改变下列条件,SO2、O2、SO3气体平衡浓度都比原来增
2SO3(g)达到平衡后改变下列条件,SO2、O2、SO3气体平衡浓度都比原来增
大的是____________(填字母)。
A.保持温度和容器体积不变,充入2molSO3 B.保持温度和容器体积不变,充入2molN2
C.保持温度和容器体积不变,充入0.5molSO2和0.25molO2
D.保持温度和容器内压强不变,充入1molSO3
E.升高温度 F.移动活塞压缩气体
(3)某人设想以右图所示装置用电化学原理生产硫酸,写出通入
SO2的电极的电极反应式:_____________
(4)若通入SO2的速率为2.24L/min(标准状况),为稳定
持续生产,硫酸溶液的浓度应维持不变,则左侧水的流
入速率应为_______________mL/min。
查看答案和解析>>
科目: 来源: 题型:
Li-Al/FeS电池是一种正在开发的车载电池,该电池中正极的电极反应式为: 2Li++FeS+2e-=Li2S+Fe 有关该电池的下列说法中,正确的是
A.负极的电极反应式为Al-3e-=Al3+ B.放电时电池内部Li+向负极移动
C.充电时该电池的电池反应式为:Li2S+Fe=2Li+FeS
D.放电时,在正极上是Li+得电子被还原
查看答案和解析>>
科目: 来源: 题型:阅读理解
(14分)不同的金属在化学反应中表现出来的活泼程度不同,瑞典化学家贝采里乌斯和俄国化学家贝开托夫称之为金属活动顺序。另一方面,同一金属在不同条件或不同化学反应中也可以表现出不同的活泼程度。
⑴根据金属活动性顺序,工业上冶炼金属可以采用不同的冶炼方法。其中可以用“热分解法”冶炼的金属有 。
腐蚀速率/g.m-2.h-1
 ⑵工业上用氯化铁溶液腐蚀铜制电路板。根据金属活动性顺序及该反应原理,比较Cu2+、Fe3+、Fe2+的氧化性由强到弱的顺序: 。
⑵工业上用氯化铁溶液腐蚀铜制电路板。根据金属活动性顺序及该反应原理,比较Cu2+、Fe3+、Fe2+的氧化性由强到弱的顺序: 。
⑶合金Fe-Cr在不同酸中反应情况不同,其在三种稀硫
酸、稀硝酸和稀盐酸中的腐蚀速率如图所示,则下列
有关说法正确的是 (填写序号)。
A.酸的氧化性越强,对该合金的腐蚀速率越大
B.稀硝酸对该合金的腐蚀性比另两种酸弱
C.合金中Cr含量增加,稀硝酸对该合金的腐蚀性减弱
⑷已知粗铜中含有少量的锌、铁、银、金等金属和少量
|
以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯,
并对阳极泥和电解液中金属进行回收。
步骤一:电解精制
电解时,粗铜应与电源的 极相连。电解过程中,硫酸铜的浓度会 (填“变大”、“不变”或“变小”)。
步骤二:电解完成后,该小组同学按以下流程对电解液进行处理:

稀硝酸处理阳极泥得到硝酸银稀溶液,请你写出该步反应的离子方程式: 。
残渣含有极少量的黄金,如何回收金,他们查阅了有关资料,了解到了一些有关金的知识,以下是他们获取的一些信息:
| 序号 | 反应 | 平衡常数 |
| 1 | Au + 6HNO3(浓)= Au(NO3)3 + 3NO2↑+ 3H2O | << 1 |
| 2 | Au3+ + 4Cl- = AuCl4- | >>1 |
从表中可知,金很难与硝酸反应,但却可溶于王水(浓硝酸与盐酸按体积比1:3的混合物),请你简要解释金能够溶于王水的原因: 。
查看答案和解析>>
科目: 来源: 题型:
著名化学家徐光宪获得2008年度“国家最高科学技术奖”,以表彰他在稀土串级萃取理论方面作出的贡献。稀土铈(Ce)元素主要存在于独居石中,金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+。下列说法正确的是 ( )
A.电解熔融Ce02制Ce,铈在阳极获得
B.铈溶于氢碘酸的化学方程式可表示为:Ce+4HI=CeI4+2H2↑
C.用Ce(S04)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++2Fe2+=Ce3++2Fe3+
D.四种稳定的核素13658Ce、13858Ce、14058Ce、14258Ce,它们互称为同位素
查看答案和解析>>
科目: 来源: 题型:
用NA表示阿伏加德罗常数,下列说法中正确的是
A.2.4g金属镁变为镁离子时失去的电子数为0.2NA
B.在标准状况下,2.24L三氧化硫中所含分子数为NA
C.12.5 mL 16 mol/L浓硫酸与足量铜反应,生成SO2的分子数为0.1NA
D.电解精炼铜时,电解池中每转移1mol电子时,阳极上溶解的铜原子数为0.5NA
查看答案和解析>>
科目: 来源: 题型:
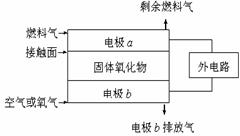 固体氧化物燃料电池(SOFC)以固体氧化物(能传导O2-)作为电解质。其工作原理如右图所示,下列关于固体燃料电池的有关说法正确的是
固体氧化物燃料电池(SOFC)以固体氧化物(能传导O2-)作为电解质。其工作原理如右图所示,下列关于固体燃料电池的有关说法正确的是
A.电极b为电池负极,电极反应式为:O2+4e-=2O2-
B.固体氧化物的作用是让电子在电池内通过
C.若H2作为燃料气,则接触面上发生的反应为:
H2+2OH--4e-=2H++H2O
D.若C2H4作为燃料气,则接触面上发生的反应为:
C2H4+6O2--12e-=2CO2+2H2O
查看答案和解析>>
科目: 来源: 题型:
右图为电解饱和食盐水的简易装置,下列有关说法正确的是
A.电解一段时间后,往蛋壳中溶液中滴加几滴酚酞,呈红色
 B.蛋壳表面缠绕铁丝发生还原反应
B.蛋壳表面缠绕铁丝发生还原反应
C.铁丝表面生成的气体能使湿润的淀粉碘化钾试纸变蓝
D.蛋壳可阻止生成的氯气与氢气、氢氧化钠溶液接触
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式书写正确的是 ( )
A.用铜作电极电解硫酸铜溶液: 2Cu2++2H2O通电4H++2Cu+O2↑
B.偏铝酸钠溶液中通入足量二氧化碳:2AlO2—+CO2+3H2O=2Al(OH)3↓+CO32—
C.过量的NaHSO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
D.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
查看答案和解析>>
科目: 来源: 题型:
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O![]() Cd(OH)2 + 2Ni(OH)2有关该电池的说法正确的 ( )
Cd(OH)2 + 2Ni(OH)2有关该电池的说法正确的 ( )
A.充电时阳极反应:Ni(OH)2-e—+ OH-= NiOOH+H2O
B.充电过程是化学能转化为电能的过程
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH-向正极移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com