
科目: 来源: 题型:单选题
| 实验事实 | 结论 | |
| A | NH3的水溶液可以导电 | NH3是电解质 |
| B | 滴有酚酞的Na2CO3溶液中加入BaCl2溶液,溶液褪色 | BaCl2溶液有酸性 |
| C | Na2SiO3溶液中通入CO2产生白色沉淀 | 酸性:H2CO3>H2SiO3 |
| D | 常温下白磷可自燃而氮气须在放电时才与氧气反应 | 非金属性:P>N |
查看答案和解析>>
科目: 来源: 题型:单选题
 =10-8的溶液中:Na+、K+、S2-、SO32-
=10-8的溶液中:Na+、K+、S2-、SO32-查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
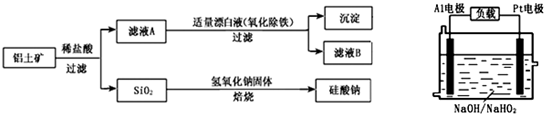
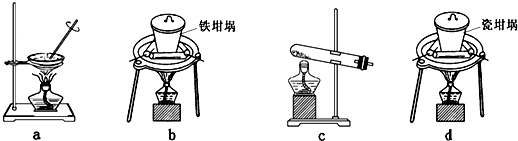
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com