
科目: 来源: 题型:单选题
| 选项 | 操作 | 现象 | 结论 |
| A | 常温下将Al片放入浓硝酸中 | 无明显变化 | Al与浓硝酸不反应 |
| B | 某铁的氧化物溶于稀硫酸中,加入硫氰化钾溶液 | 溶液变红 | 该化合物一定为Fe2O3 |
| C | 将水蒸气通过灼热的铁粉 | 粉末变红 | 铁与水在高温下发生反应 |
| D | 将一小块Na放入无水乙醇中 | 产生气泡 | Na能置换出醇羟基中的氢 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:多选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
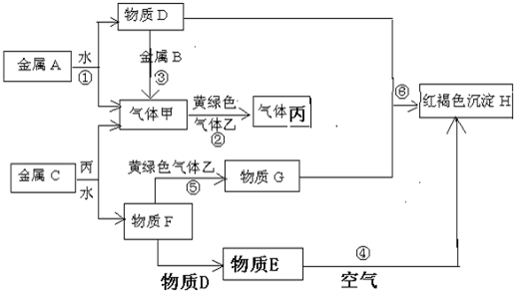
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
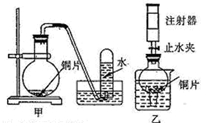 图是甲、乙两位同学探究铜和稀硝酸反应的装置图,请回答下列问题:
图是甲、乙两位同学探究铜和稀硝酸反应的装置图,请回答下列问题:| 实验步骤 | 实验现象及结论 |
| ①向干燥管中加少量铜片,如图装配好仪器,向烧杯中注入稀HNO3 | ______ |
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com