
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
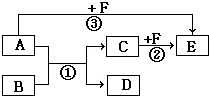 有A、B、C、D、E、F六种物质,它们之间相互转化的关系如图所示(反应条件及部分产物未标出).
有A、B、C、D、E、F六种物质,它们之间相互转化的关系如图所示(反应条件及部分产物未标出).查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
| 不纯物质 | 除杂试剂 | 分离方法 | |
| A | NH4Cl溶液(FeCl3) | NaOH溶液 | 过滤 |
| B | 苯(苯酚) | 浓溴水 | 过滤 |
| C | 苯(甲苯) | KMnO4(酸化),NaOH溶液 | 分液 |
| D | 乙酸乙酯(乙酸) | KOH溶液 | 分液 |
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
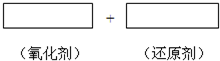 KMnO4的氧化性随pH的减小而增大.其在酸性介质中还原产物是Mn2+;在中性或碱性介质中还原产物主要是MnO2.
KMnO4的氧化性随pH的减小而增大.其在酸性介质中还原产物是Mn2+;在中性或碱性介质中还原产物主要是MnO2.查看答案和解析>>
科目: 来源: 题型:单选题
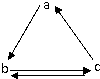 下表所列各组物质中,各物质间能按照如图所示通过一步反应就能完成转化的是
下表所列各组物质中,各物质间能按照如图所示通过一步反应就能完成转化的是| a | b | c | |
| A | Cu | CuSO4 | Cu(OH)2 |
| B | HNO3 | NO | NO2 |
| C | Fe | Fe3O4 | Fe(OH)3 |
| D | Si | SiO2 | H2SiO3 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com