
科目:gzhx 来源:0118 月考题 题型:单选题

 6A+2C
6A+2C科目:gzhx 来源: 题型:
 (2009•龙岩一模)短周期元素A、B、C、D在周期表中位置如图所示,其中元素D原子最外层有3个电子.
(2009•龙岩一模)短周期元素A、B、C、D在周期表中位置如图所示,其中元素D原子最外层有3个电子.
| ||
| ||
科目:gzhx 来源: 题型:
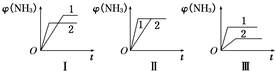 合成氨生产技术的创立开辟了人工固氮的途径,对化学工业技术也产生了重大影响.合成氨反应的化学方程式为N2(g)+3H2(g)⇌2NH3(g)△H=-92.2kJ•mol-1.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷或焦炭与水蒸气反应制得.
合成氨生产技术的创立开辟了人工固氮的途径,对化学工业技术也产生了重大影响.合成氨反应的化学方程式为N2(g)+3H2(g)⇌2NH3(g)△H=-92.2kJ•mol-1.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷或焦炭与水蒸气反应制得.科目:gzhx 来源: 题型:阅读理解
科目:gzhx 来源: 题型:
科目:gzhx 来源: 题型:
现有五种短周期元素A、B、C、D、E,其原子序数依次增大。A、E同主族,A元素原子半径最小。B元素原子的最外层电子数是内层电子数的2倍。C元素最高价氧化物的水化物X与其氢化物Y反应生成一种盐。A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物。试回答下列问题:
(1)写出X与Y反应生成这种盐的化学方程式 。
(2)A、B、D、E四种元素组成的某无机盐受热易分解。写出少量该化合物与足量的 Ba(OH)2溶液反应的离子方程式 。
(3)将B的某种单质用作电极,电解E元素的最高价氧化物水化物的溶液时,阳极的电极反应式为 。
(4)在一密闭容器中注入A2、C2两种气体,发生了“![]() ”的化学反应。在某温度下达到平衡时,各物质的浓度分别是:c(A2)=9.00 mol·L-1,c(C2) =3.00 mol·L-1,c(CA3) =4.00 mol·L-1。则此时该反应的平衡常数K= ;C2的初始浓度为mol·L-1;A2的转化率是 %。
”的化学反应。在某温度下达到平衡时,各物质的浓度分别是:c(A2)=9.00 mol·L-1,c(C2) =3.00 mol·L-1,c(CA3) =4.00 mol·L-1。则此时该反应的平衡常数K= ;C2的初始浓度为mol·L-1;A2的转化率是 %。
科目:gzhx 来源: 题型:
在密闭容器中,X2(g)+Y2(g)![]() 2Z(g),已知起始时,X2、Y2和Z各物质浓度分别为0.1 mol·L-1,0.3 mol·L-1和0.2 mol·L-1,反应在一定条件下达到平衡时,各物质的浓度可能是( )
2Z(g),已知起始时,X2、Y2和Z各物质浓度分别为0.1 mol·L-1,0.3 mol·L-1和0.2 mol·L-1,反应在一定条件下达到平衡时,各物质的浓度可能是( )
A.c(Z)=0.03 mol·L-1 B.c(Y2)=0.35 mol·L-1
C.c(Y2)=0.2 mol·L-1 D.c(Z)=0.4 mol·L-1
科目:gzhx 来源: 题型:
A.c(Z)=0.03 mol·L-1 B.c(Y2)=0.35 mol·L-1
C.c(Y2)=0.2 mol·L-1 D.c(Z)=0.4 mol·L-1
科目:gzhx 来源: 题型:
(1)写出X与Y反应生成这种盐的化学方程式:____________________________________。
(2)A、B、D、E四种元素组成的某无机盐受热易分解。写出少量该化合物与足量的Ba(OH)2溶液反应的离子方程式:________________________________________________________。
(3)将B的某种单质用作电极,电解E元素的最高价氧化物水化物的溶液时,阳极的电极反应式为_____________________________________________________________________。
(4)在一密闭容器中注入A2、C2两种气体,发生了“![]() 2CA3(g);ΔH<
2CA3(g);ΔH<
科目:gzhx 来源: 题型:
科目:gzhx 来源: 题型:
| A、反应达到平衡时,各物质的浓度不再发生变化 | B、反应达到平衡时,各物质的浓度都相等 | C、反应达到平衡时,各物质的浓度之比为1:2:3 | D、降低温度时,反应的正反应速率增大,而逆反应速率减小 |
科目:gzhx 来源:2010年黑龙江省高一下学期期中考试化学试题 题型:选择题
关于化学平衡状态和化学反应限度的说法正确的是
A.当一个可逆反应达到化学平衡状态时,正向反应速率和逆向反应速率都等于零
B.一个可逆反应达到的平衡状态就是这个反应在该条件下所能达到的限度
C.化学平衡状态时,各物质的浓度保持相等
D.化学反应的限度由反应物的本性决定,是不可改变的
科目:gzhx 来源:2014届贵州省高一下学期期中考试化学试卷(解析版) 题型:选择题
下列关于化学反应限度的说法中正确的是( )
A.一个可逆反应达到的平衡状态就是这个反应在该条件下所能达到的限度
B.当一个可逆反应达到平衡状态时,正向反应速率和逆向反应速率相等且等于零
C.平衡状态时,各物质的浓度保持相等
D.化学反应的限度不可以通过改变条件而改变
科目:gzhx 来源:2012届江苏省高二下学期期中考试化学试题 题型:计算题
N2和H2发生合成氨反应N2(g)+3H2(g) 2NH3(g)。在一定条件下达到平衡时,各物质的浓度是c(N2)=3mol/L,c(H2)=9mol/L,c(NH3)=4mol/L,求该温度时的平衡常数及N2、H2的起始浓度。
2NH3(g)。在一定条件下达到平衡时,各物质的浓度是c(N2)=3mol/L,c(H2)=9mol/L,c(NH3)=4mol/L,求该温度时的平衡常数及N2、H2的起始浓度。
科目:gzhx 来源: 题型:013
A(g)+2B(g) C(g)+2D(g)在恒温条件下达到平衡,能充分说明这一事实的是
C(g)+2D(g)在恒温条件下达到平衡,能充分说明这一事实的是
[ ]
A.反应容器内压强不再变化
B.各反应物的浓度不再变化
C.单位时间内生成nmolA,则同时生成2nmolB
D.反应容内A、B、C、D四种物质的生成速率相等
科目:gzhx 来源:物理教研室 题型:013
A(g)+2B(g)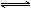 C(g)+2D(g)在恒温条件下达到平衡,能充分说明这一事实的是
C(g)+2D(g)在恒温条件下达到平衡,能充分说明这一事实的是
[ ]
A.反应容器内压强不再变化
B.各反应物的浓度不再变化
C.单位时间内生成nmolA,则同时生成2nmolB
D.反应容内A、B、C、D四种物质的生成速率相等
科目:gzhx 来源:2013年高考化学备考复习卷7:化学反应速率与化学平衡(解析版) 题型:选择题
科目:gzhx 来源:不详 题型:多选题
| A.在这一反应中,各物质的消耗速率相等 |
| B.若反应中消耗4 mol H2O,则必定同时生成2 mol Fe(OH)3 |
| C.v[Fe(OH)2]=2v(H2O)=4v(O2) |
| D.反应中消耗1 mol O2,必定同时消耗2 mol H2O |
科目:gzhx 来源: 题型:
关于化学平衡状态和化学反应限度的说法正确的是
A.当一个可逆反应达到化学平衡状态时,正向反应速率和逆向反应速率都等于零
B.一个可逆反应达到的平衡状态就是这个反应在该条件下所能达到的限度
C.化学平衡状态时,各物质的浓度保持相等
D.化学反应的限度由反应物的本性决定,是不可改变的
科目:gzhx 来源: 题型:
关于化学平衡状态和化学反应限度的说法正确的是
A.当一个可逆反应达到化学平衡状态时,正向反应速率和逆向反应速率都等于零
B.一个可逆反应达到的平衡状态就是这个反应在该条件下所能达到的限度
C.化学平衡状态时,各物质的浓度保持相等
D.化学反应的限度由反应物的本性决定,是不可改变的