
科目:gzhx 来源: 题型:
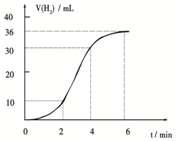
(12分)金属钒(V)在材料科学上有重要作用,被称为“合金的维生素”。以下是测定矿石中钒的含量的两个反应:
![]()
![]() (1)用稀硫酸溶解五氧化二钒,得到(VO2)2SO4溶液。写出该反应的化学方程式
(1)用稀硫酸溶解五氧化二钒,得到(VO2)2SO4溶液。写出该反应的化学方程式
___________________________________________________________________;
该反应______(选填“是”或“不是”)氧化还原反应。
(2)用已知浓度的硫酸酸化的H2C2O4(H2C2O4中C为+3价)溶液,滴定(VO2)2SO4溶液,完成下列离子方程式,短线上填写物质的化学式或离子符号。
VO2+ + H2C2O4 + _____→ VO2+ + CO2 + ________
反应中做氧化剂的是__________,被还原的元素是_______________。
欲知该反应能否用盐酸酸化,还需要知道的是__________________________相对大小。
科目:gzhx 来源: 题型:
 金属镁及其化合物不仅在国防上有重要应用,在化学研究中也有广泛应用.
金属镁及其化合物不仅在国防上有重要应用,在化学研究中也有广泛应用.| 编号 | 电极材料 | 电解质溶液 | 电子流动 方向 |
| 1 | Mg-Al | 稀盐酸 | Mg流向Al |
| 2 | Mg-Al | NaOH溶液 |
科目:gzhx 来源: 题型:022
叠氮化物在工业上有重要作用,N3-叫做叠氮离子。则:
(1)一个叠氮离子N3-中共有_____个电子。
(2)写出三种由三个原子组成,含有与N3-相同电子数的分子或离子的化学式:______,________,___________。
科目:gzhx 来源:物理教研室 题型:022
(1)一个叠氮离子N3-中共有_____个电子。
(2)写出三种由三个原子组成,含有与N3-相同电子数的分子或离子的化学式:______,________,___________。
科目:gzhx 来源: 题型:
2008年10月14日长江商报报道:湖北监利钒污染致近千人患严重皮肤病。监利县有投产和在建的非法钒冶炼厂达9家,非法钒冶炼厂所造成的污染使得草木枯萎,饮水变咸,清河变浊,人畜奇怪病变,曾经的鱼米之乡正受到前所未有的污染威胁。钒和钒(V)的化合物在工业上有重要用途。如五氧化二钒是工业接触法制硫酸的催化剂。查阅资料知,利用钒矿石制五氧化二钒和钒的工艺流程图如下:
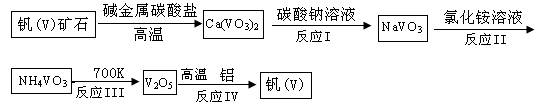
(1)钒(V)的原子序数为23,下列对钒在元素周期表中位置和元素类别判断正确的是 。
A.它位于第五周期第ⅤB族 B.它位于第四周期第ⅤB族 C.它是过渡元素
D.它位于第五周期第ⅤA族 E.它位于第四周期第ⅤA族 F.它与铁位于同一周期
(2)工业上,接触法制硫酸在接触室里发生反应:2SO2+O2![]() 2SO3,催化剂一般是V2O5??,下列对五氧化二钒作用的描述正确的是 。
2SO3,催化剂一般是V2O5??,下列对五氧化二钒作用的描述正确的是 。
A.能增大该反应所需要的能量 B.能提高二氧化硫的转化率
C.能改变该反应的反应热(△H) D.能同程度增大正、逆反应速率
E.能增加SO2和O2分子的能量
(3)写出下列化学方程式:
反应I: ;反应III: ;反应IV: 。
(4)预测反应II发生的原因是 ;IV的反应类型是 。
科目:gzhx 来源: 题型:
科目:gzhx 来源: 题型:
| ||
| ||
科目:gzhx 来源: 题型:阅读理解
科目:gzhx 来源:2010年吉林省高一上学期期中考试化学试卷 题型:填空题
(14分) 下图各物质中,A、B、C是常见金属单质,甲、乙、丙是气体且乙是有特殊颜色的气体(图中有些反应的产物和反应的条件没有全部标出)。
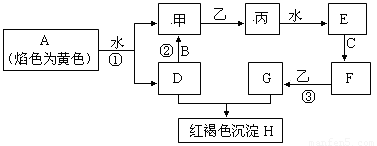
请根据以上信息回答下列问题:
(1)写出:H的化学式_________,乙的两种重要用途________________________________
(2)写出有关反应的离子方程式:
反应①__________________________________________________________
反应②__________________________________________________________
(3)判断反应③己经发生的常用试剂是______________________
(4)胶态磁流体(液溶胶)在医学上有重要用途,C单质对应元素的某种纳米级氧化物是磁流体中的重要粒子,该磁流体的主要制备过程如下:(Ⅰ)将NH3通入F、G的混合溶液(F、G物质的量比为1:2)中会生成两种碱。(Ⅱ)这两种碱恰好反应就得到该氧化物。写出(Ⅱ)中反应的化学方程式为:_________________________,确定该磁流体己成功制取的方法_________________________________
科目:gzhx 来源:2010年吉林省吉林一中高一上学期期中考试化学试卷 题型:填空题
(14分)下图各物质中,A、B、C是常见金属单质,甲、乙、丙是气体且乙是有特殊颜色的气体(图中有些反应的产物和反应的条件没有全部标出)。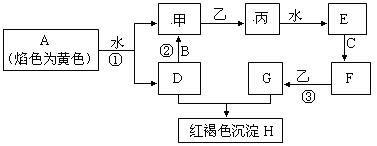
请根据以上信息回答下列问题:
(1)写出:H的化学式_________,乙的两种重要用途________________________________
(2)写出有关反应的离子方程式:
反应①__________________________________________________________
反应②__________________________________________________________
(3)判断反应③己经发生的常用试剂是______________________
(4)胶态磁流体(液溶胶)在医学上有重要用途,C单质对应元素的某种纳米级氧化物是磁流体中的重要粒子,该磁流体的主要制备过程如下:(Ⅰ)将NH3通入F、G的混合溶液(F、G物质的量比为1:2)中会生成两种碱。(Ⅱ)这两种碱恰好反应就得到该氧化物。写出(Ⅱ)中反应的化学方程式为:_________________________,确定该磁流体己成功制取的方法_________________________________
科目:gzhx 来源: 题型:
(14分) 下图各物质中,A、B、C是常见金属单质,甲、乙、丙是气体且乙是有特殊颜色的气体(图中有些反应的产物和反应的条件没有全部标出)。
请根据以上信息回答下列问题:
(1)写出:H的化学式_________,乙的两种重要用途________________________________
(2)写出有关反应的离子方程式:
反应①__________________________________________________________
反应②__________________________________________________________
(3)判断反应③己经发生的常用试剂是______________________
(4)胶态磁流体(液溶胶)在医学上有重要用途,C单质对应元素的某种纳米级氧化物是磁流体中的重要粒子,该磁流体的主要制备过程如下:(Ⅰ)将NH3通入F、G的混合溶液(F、G物质的量比为1:2)中会生成两种碱。(Ⅱ)这两种碱恰好反应就得到该氧化物。写出(Ⅱ)中反应的化学方程式为:_________________________,确定该磁流体己成功制取的方法_________________________________
科目:gzhx 来源:2012-2013学年福建省三明市高三5月质检理综化学试卷(解析版) 题型:填空题
铬、铁、镍、铜等金属及其化合物在工业上有重要用途。
(1)基态铬原子的价电子排布式为 。
(2)CrO2Cl2和NaClO均可作化工生产的氧化剂或氯化剂。制备CrO2Cl2的反应为:K2Cr2O2+3CCl4
2KC+2CrO2Cl2+3COCl2↑。
①上述反应式中非金属元素电负性由大到小的顺序是 (用元素符号表示)。
②常温时CrO2Cl2是一种易溶于CCl4的液体,则固态CrO2Cl2属于 晶体。
③COCl2分子中所有原子均满足8电子构型,COCl2分子中σ键和π键的个数比为 。
(3)NiO、FeO的晶体结构均与氯化钠的晶体结构相同,其中Ni2+和Fe2+的离子半径分别为6.9×10-2nm和7.8×10-2nm。则熔点:NiO FeO(填”<”、 “=”或 “>”)。
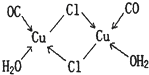
(4)CuCl的盐酸溶液能吸收CO生成复合物氯化羰基亚铜[Cu2Cl2(CO)2·2H2O],其结构如图。下列说法不正确的是 (填标号)。
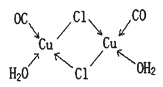
A.该复合物中存在化学健类型只有离子键、配位键
B.该复合物中Cl原子的杂化类型为sp3
C.该复合物中只有CO和H2O作为配位体
D.CO与N2的价电子总数相同,其结构为C=O
(5)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是 。
科目:gzhx 来源: 题型:
(1)若①⑤⑥三种元素在周期表中相对位置如下图。①与⑤、①与⑥形成的液体化合物是常见的重要溶剂,则这三种元素最高价含氧酸酸性由强到弱的顺序是___________________。
![]()
(2)若下图中甲、乙、丙、丁、戊均为上述9种元素中的某些元素组成的单质或由其中两种元素组成的化合物。

①若甲是O2、乙是N2H4,置换反应是在强碱性溶液中进行的原电池反应,则负极发生的电极反应式为_______________。
②若戊为SO3,则乙可能是____________(填化学式)。
(3)若下图中A是常见的金属单质,B、C、D、E分别是上述9种元素中的某些元素组成的单质或其中两种元素组成的化合物。

①若该置换反应是在高温下进行的,在工业上有重要应用价值。物质C是一种两性化合物,则该反应的化学方程式为_____________________________________。
②若该置换反应是用A作阳极,在B的水溶液中进行电解反应。则反应a中阴极的电极反应式为______________________。
科目:gzhx 来源: 题型:
下图是中学化学常见物质之间的转化关系图,有些反应中的部分物质被略去。在通常情况下,A为红棕色粉末,C是一种黄绿色气体,B、D均为金属。其中反应①在工业上有重要应用。

淆回答下列问题:
(1)C的电子式为 。 (2)I的化学式为 。
(3)反应①的化学方程式为 。
(4)反应②的离子方程式为 。
科目:gzhx 来源:0107 期中题 题型:推断题
科目:gzhx 来源: 题型:
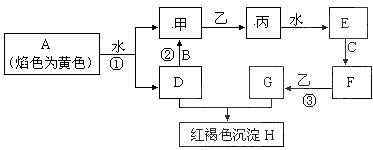
下图各物质中,A、B、C是常见金属单质,甲、乙、丙是气体且乙是有特殊颜色的气体(图中有些反应的产物和反应的条件没有全部标出)。

请根据以上信息回答下列问题:
(1)写出:H的化学式_________,乙的两种重要用途________________________________
(2)写出有关反应的离子方程式:
反应①__________________________________________________________
反应②__________________________________________________________
(3)判断反应③己经发生的常用试剂是______________________
(4)胶态磁流体(液溶胶)在医学上有重要用途,C单质对应元素的某种纳米级氧化物是磁流体中的重要粒子,该磁流体的主要制备过程如下:(Ⅰ)将NH3通入F、G的混合溶液(F、G物质的量比为1:2)中会生成两种碱。(Ⅱ)这两种碱恰好反应就得到该氧化物。写出(Ⅱ)中反应的化学方程式为:_________________________,确定该磁流体己成功制取的方法_________________________________
科目:gzhx 来源:2012-2013学年河南省郑州四中高三(上)第四次调考化学试卷(解析版) 题型:解答题
科目:gzhx 来源:山东海阳一中2008年高考模拟考试理科综合化学部分 题型:022
已知:A、H为常见的金属单质,D、F在常温下为气态单质,B为淡黄色固体,J为红褐色沉淀.请按要求填空:

(1)写出B的电子式:____________________________.
(2)写出用A作电极电解G溶液(如图),在电极上生成E的反
应式________________________.

(3)反应①的化学方程式是___________________________.
反应④在生产中有重要应用,被称为________反应.
(4)反应⑥的离子方程式是________.
科目:gzhx 来源: 题型:
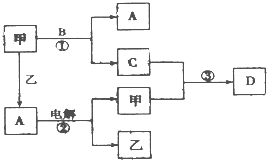 A、B、C、D是由短周期元素组成的四种常见的化合物,D为红棕色气体,甲、乙是两种单质,这些单质和化合物之间存在如图所示的转化关系:
A、B、C、D是由短周期元素组成的四种常见的化合物,D为红棕色气体,甲、乙是两种单质,这些单质和化合物之间存在如图所示的转化关系:科目:gzhx 来源: 题型:
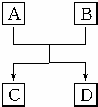 已知A、B、C、D组成的元素都属于短周期,它们之间的简单转化关系如图所示.
已知A、B、C、D组成的元素都属于短周期,它们之间的简单转化关系如图所示.
| ||
| ||
| ||
| ||
| ||
| ||