现在有一杯水,你想这样用什么工具来,测出这杯水的哪些数据?答案解析
科目:czhx
来源:黄浦区
题型:问答题
甲、乙两同学想了解碳酸钾溶液的酸碱性.他们做了以下研究:
[猜想与假设]碳酸钾溶液的酸碱性可能有______种情况;
[设计与实验]用pH试纸来检测碳酸钾溶液的酸碱性:
|
实 验 操 作 |
检测结果 |
| 甲同学 |
取pH试纸放在玻璃片上;
用玻璃棒蘸取碳酸钾溶液沾在pH试纸上;
将试纸显示的颜色与标准比色卡比较. |
pH>7 |
| 乙同学 |
将pH试纸直接浸入碳酸钾溶液中,把试纸显示的颜色与标准比色卡比较. |
PH>7 |
[结论和分析]根据两位同学的实验可得出碳酸钾溶液酸碱性的结论:______
[评价与反思]根据两位同学的实验操作,你认为______同学操作不规范.为什么?______
如果实验室没有pH试纸,又要一次测定未知溶液的酸碱性,可选用______试液来进行实验.
查看答案和解析>>
科目:czhx
来源:2005年上海市黄浦区中考化学试卷(解析版)
题型:解答题
甲、乙两同学想了解碳酸钾溶液的酸碱性.他们做了以下研究:
[猜想与假设]碳酸钾溶液的酸碱性可能有______种情况;
[设计与实验]用pH试纸来检测碳酸钾溶液的酸碱性:
| 实 验 操 作 | 检测结果 |
| 甲同学 | 取pH试纸放在玻璃片上;
用玻璃棒蘸取碳酸钾溶液沾在pH试纸上;
将试纸显示的颜色与标准比色卡比较. | pH>7 |
| 乙同学 | 将pH试纸直接浸入碳酸钾溶液中,把试纸显示的颜色与标准比色卡比较. | PH>7 |
[结论和分析]根据两位同学的实验可得出碳酸钾溶液酸碱性的结论:______
[评价与反思]根据两位同学的实验操作,你认为______同学操作不规范.为什么?______
如果实验室没有pH试纸,又要一次测定未知溶液的酸碱性,可选用______试液来进行实验.
查看答案和解析>>
科目:czhx
来源:
题型:填空题
甲、乙两同学想了解碳酸钾溶液的酸碱性.他们做了以下研究:
[猜想与假设]碳酸钾溶液的酸碱性可能有________种情况;
[设计与实验]用pH试纸来检测碳酸钾溶液的酸碱性:
| 实 验 操 作 | 检测结果 |
| 甲同学 | 取pH试纸放在玻璃片上;
用玻璃棒蘸取碳酸钾溶液沾在pH试纸上;
将试纸显示的颜色与标准比色卡比较. | pH>7 |
| 乙同学 | 将pH试纸直接浸入碳酸钾溶液中,把试纸显示的颜色与标准比色卡比较. | PH>7 |
[结论和分析]根据两位同学的实验可得出碳酸钾溶液酸碱性的结论:________
[评价与反思]根据两位同学的实验操作,你认为________同学操作不规范.为什么?________
如果实验室没有pH试纸,又要一次测定未知溶液的酸碱性,可选用________试液来进行实验.
查看答案和解析>>
科目:czhx
来源:
题型:
归纳与演绎是重要的科学方法,也是常用的化学学习方法.
(1)某研究小组对用双氧水分解生成水和氧气的实验条件进行探究,完成了以下实验:
①往盛有5mL 5%H
2O
2溶液的试管中,伸入带火星的木条,木条不复燃.
②往盛有5mL w%H
2O
2溶液的试管中,加入a g MnO
2,伸入带火星的木条,木条复燃.
③往盛有5mL w%H
2O
2溶液的试管中,加入a g Fe
2O
3,伸入带火星的木条,木条复燃.
④经检验,②③中反应后试管中仍分别含有a gMnO
2和 ag Fe
2O
3问题一:请你写出用双氧水和二氧化锰制氧气的化学反应方程式
问题二:MnO
2和 Fe
2O
3在上述反应中的作用是
;实验②③中的H
2O
2的浓度(w%)以
为宜.
(2)研究小组还对溶液浓度、催化剂的种类等实验条件进行探究.下表选取了部分实验数据:用足量等体积H
2O
2溶液制取相同体积O
2所需要的时间
浓度
时间(min)
条件 |
30% H2O2 |
15% H2O2 |
5% H2O2 |
| Ag MnO2 |
0.2 |
0.8 |
2.0 |
| ag Fe2O3 |
0.7 |
9.0 |
16.0 |
问题三:从上表中能得到哪些结论?(写出一条结论)
.
查看答案和解析>>
科目:czhx
来源:
题型:阅读理解
27、实验室里NaOH固体必须密封保存,其原因是
NaOH在空气里易吸水而潮解,易和CO2反应而变质
,
现实验室里有一包白色NaOH样品,某兴趣小组同学为了确定这样品的成分,对其可能的组成进行了下列探究.
(1)【猜想】依据所学知识,兴趣小组同学对这种白色粉末的成分作了如下猜想:
①可能没有变质,全是NaOH;②可能完全变质,全是Na
2CO
3;你认为还有一种可能是
NaOH部分变质,既含NaOH,又含Na2CO3
.
(2)【实验】为了验证猜想,他们做了下面实验:
实验一:取少量白色粉末溶于水,向所得溶液里滴加酚酞试液,溶液变为红色.
实验二:取少量白色粉末,滴加稀盐酸,有气体生成.
(3)【结论】由上述实验过程和实验现象,分析得到下面结论.
结论一:由实验一得到的结论是白色粉末是NaOH.请你判断该结论是否正确,并简述理由:
不正确,因为Na2CO3溶液也是碱性的
综合分析上述两个实验,你得到的结论是:
该NaOH已经全部或部分变质
(4)【继续探究】兴趣小组同学在分析和研究了上述实验及实验结论后,为了确认白色粉末的成分,查阅资料并做了下面的实验三:取少量白色粉末溶于水,向所得溶液里滴加过量的BaCl
2试液,有白色沉淀产生(反应的方程式为Na
2CO
3+BaCl
2=BaCO
3↓+2NaCl)…
①你认为滴加过量BaCl
2试液的目的是
除去碳酸钠
;
②如何判断BaCl
2试液已经过量?
滴加氯化钡(或氯化钙)溶液不再产生沉淀
;
③你认为还应继续进行的实验是
在液体中滴加几滴酚酞试液,酚酞溶液不变红
,则说明原NaOH固体已经完全变质.
查看答案和解析>>
科目:czhx
来源:
题型:阅读理解
归纳与演绎是重要的科学方法,也是常用的化学学习方法.
(1)我们已经学习过实验室制取O
2、CO
2、H
2(Zn和稀硫酸反应)三种气体的反应原理、制取与收集方法.请你归纳出实验室制取气体反应的共同点
(填序号)
①需要加热 ②使用催化剂 ③没有气体参加反应 ④原料为纯净物 ⑤只生成一种气体
(2)下列是实验室常用的仪器
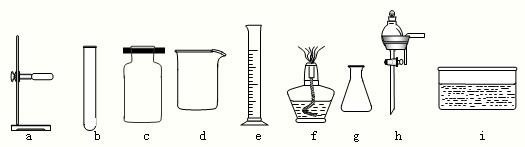
写出仪器名称:a是
,c是
;写出d的一种用途
.
(3)化学上可以通过多种反应制得NH
3(极易溶于水,密度比空气小),例如
①2NH
4Cl(固)+Ca(OH)
2(固)
CaCl
2+2NH
3↑+2H
2O
②NH
4HCO
3(固)
NH
3↑+CO
2↑+H
2O
③CaO(固)+NH
3.H
2O(浓)═NH
3↑+Ca(OH)
2我将选择反应
(只写一个,填序号)作为实验室制取氨气的反应原理.我需要用上面仪器中的
(填序号)来装配氨气发生装置(连接装置已经省略),我采用的收集方法是
.我选择的发生装置还可以用来制取
气体.
(4)某研究小组对用双氧水分解生成水和氧气的实验条件进行探究,完成了以下实验:
①往盛有5ml 5%H
2O
2溶液的试管中,伸入带火星的木条,木条不复燃.
②往盛有5ml w% H
2O
2溶液的试管中,加入a g MnO
2,伸入带火星的木条,木条复燃.
③往盛有5ml w% H
2O
2溶液的试管中,加入a g Fe
2O
3,伸入带火星的木条,木条复燃.
④经检验,②③中反应后试管中仍分别含有a gMnO
2和 ag Fe
2O
3
问题一:请你写出用双氧水和二氧化锰制氧气的化学反应方程式
问题二:MnO2和 Fe2O3在上述反应中的作用是 .
实验②④中的H2O2的浓度(w%)以 为宜. |
研究小组还对溶液浓度、催化剂的种类等实验条件进行探究.下表选取了部分实验数据:用足量等体积H
2O
2溶液制取相同体积O
2所需要的时间
浓度
时间(min)
条件 |
30%H2O2 |
15%H2O2 |
5%H2O2 |
| ag MnO2 |
0.2 |
0.8 |
2.0 |
| ag Fe2O3 |
0.7 |
9.0 |
16.0 |
查看答案和解析>>
科目:czhx
来源:
题型:
某研究小组对用双氧水分解生成水和氧气的实验条件进行探究,完成了以下实验:
①往盛有5 mL 5%H2O2溶液的试管中,伸入带火星的木条,木条不复燃。
②往盛有5 mL w% H2O2溶液的试管中,加入ag MnO2,伸入带火星的木条,木条复燃。
③往盛有5 mL w% H2O2溶液的试管中,加入ag Fe2O3,伸入带火星的木条,木条复燃。
| 问题一:请你写出用双氧水和二氧化锰制氧气的化学反应方程式 (2分) 问题二:MnO2和 Fe2O3在上述反应中的作用是 。 实验②④中的H2O2的浓度(w%)以 为宜。(2分) | |
④经检验,②③中反应后试管中仍分别含有ag MnO
2和 ag Fe
2O
3 研究小组还对溶液浓度、催化剂的种类等实验条件进行探究。下表选取了部分实验数据:用足量等体积H2O2溶液制取相同体积O2所需要的时间
|   浓度时间(min) 浓度时间(min)
条件 | 30%H2O2 | 15%H2O2 | | 问题三:从左表中能得到哪些结论?(2分)(写出一条结论) | | 5%H2O2 |
| ag MnO2 | 0.2 | 0.8 | 2.0 |
| ag Fe2O3 | 0.7 | 9.0 | 16.0 |
查看答案和解析>>
科目:czhx
来源:2007-2008学年江苏省南京市伯乐中学九年级(下)月考化学试卷(解析版)
题型:解答题
实验室里NaOH固体必须密封保存,其原因是______,
现实验室里有一包白色NaOH样品,某兴趣小组同学为了确定这样品的成分,对其可能的组成进行了下列探究.
(1)【猜想】依据所学知识,兴趣小组同学对这种白色粉末的成分作了如下猜想:
①可能没有变质,全是NaOH;②可能完全变质,全是Na2CO3;你认为还有一种可能是______.
(2)【实验】为了验证猜想,他们做了下面实验:
实验一:取少量白色粉末溶于水,向所得溶液里滴加酚酞试液,溶液变为红色.
实验二:取少量白色粉末,滴加稀盐酸,有气体生成.
(3)【结论】由上述实验过程和实验现象,分析得到下面结论.
结论一:由实验一得到的结论是白色粉末是NaOH.请你判断该结论是否正确,并简述理由:______
综合分析上述两个实验,你得到的结论是:______
(4)【继续探究】兴趣小组同学在分析和研究了上述实验及实验结论后,为了确认白色粉末的成分,查阅资料并做了下面的实验三:取少量白色粉末溶于水,向所得溶液里滴加过量的BaCl2试液,有白色沉淀产生(反应的方程式为Na2CO3+BaCl2=BaCO3↓+2NaCl)…
①你认为滴加过量BaCl2试液的目的是______;
②如何判断BaCl2试液已经过量?______;
③你认为还应继续进行的实验是______,则说明原NaOH固体已经完全变质.
查看答案和解析>>
科目:czhx
来源:2008年广东省广州市花都区中考化学模拟试卷(解析版)
题型:填空题
(2008•花都区一模)归纳与演绎是重要的科学方法,也是常用的化学学习方法.
(1)某研究小组对用双氧水分解生成水和氧气的实验条件进行探究,完成了以下实验:
①往盛有5ml 5%H
2O
2溶液的试管中,伸入带火星的木条,木条不复燃.
②往盛有5ml w%H
2O
2溶液的试管中,加入a g MnO
2,伸入带火星的木条,木条复燃.
③往盛有5ml w%H
2O
2溶液的试管中,加入a g Fe
2O
3,伸入带火星的木条,木条复燃.
④经检验,②③中反应后试管中仍分别含有a gMnO
2和 ag Fe
2O
3问题一:请你写出用双氧水和二氧化锰制氧气的化学反应方程式
问题二:MnO
2和 Fe
2O
3在上述反应中的作用是;实验②③中的H
2O
2的浓度(w%)以为宜.
(2)研究小组还对溶液浓度、催化剂的种类等实验条件进行探究.下表选取了部分实验数据:用足量等体积H
2O
2溶液制取相同体积O
2所需要的时间
浓度
时间(min)
条件 | 30% H2O2 | 15% H2O2 | 5% H2O2 |
| Ag MnO2 | 0.2 | 0.8 | 2.0 |
ag Fe2O3
| 0.7 | 9.0 | 16.0 |
问题三:从上表中能得到哪些结论?(写出一条结论)
.
查看答案和解析>>
科目:czhx
来源:
题型:解答题
归纳与演绎是重要的科学方法,也是常用的化学学习方法.
(1)某研究小组对用双氧水分解生成水和氧气的实验条件进行探究,完成了以下实验:
①往盛有5ml 5%H2O2溶液的试管中,伸入带火星的木条,木条不复燃.
②往盛有5ml w%H2O2溶液的试管中,加入a g MnO2,伸入带火星的木条,木条复燃.
③往盛有5ml w%H2O2溶液的试管中,加入a g Fe2O3,伸入带火星的木条,木条复燃.
④经检验,②③中反应后试管中仍分别含有a gMnO2和 ag Fe2O3
问题一:请你写出用双氧水和二氧化锰制氧气的化学反应方程式______
问题二:MnO2和 Fe2O3在上述反应中的作用是______;实验②③中的H2O2的浓度(w%)以______为宜.
(2)研究小组还对溶液浓度、催化剂的种类等实验条件进行探究.下表选取了部分实验数据:用足量等体积H2O2溶液制取相同体积O2所需要的时间
浓度
时间(min)
条件 | 30% H2O2 | 15% H2O2 | 5% H2O2 |
| Ag MnO2 | 0.2 | 0.8 | 2.0 |
ag Fe2O3
| 0.7 | 9.0 | 16.0 |
问题三:从上表中能得到哪些结论?(写出一条结论)
______.
查看答案和解析>>
科目:czhx
来源:不详
题型:问答题
实验室里NaOH固体必须密封保存,其原因是______,
现实验室里有一包白色NaOH样品,某兴趣小组同学为了确定这样品的成分,对其可能的组成进行了下列探究.
(1)【猜想】依据所学知识,兴趣小组同学对这种白色粉末的成分作了如下猜想:
①可能没有变质,全是NaOH;②可能完全变质,全是Na2CO3;你认为还有一种可能是______.
(2)【实验】为了验证猜想,他们做了下面实验:
实验一:取少量白色粉末溶于水,向所得溶液里滴加酚酞试液,溶液变为红色.
实验二:取少量白色粉末,滴加稀盐酸,有气体生成.
(3)【结论】由上述实验过程和实验现象,分析得到下面结论.
结论一:由实验一得到的结论是白色粉末是NaOH.请你判断该结论是否正确,并简述理由:______
综合分析上述两个实验,你得到的结论是:______
(4)【继续探究】兴趣小组同学在分析和研究了上述实验及实验结论后,为了确认白色粉末的成分,查阅资料并做了下面的实验三:取少量白色粉末溶于水,向所得溶液里滴加过量的BaCl2试液,有白色沉淀产生(反应的方程式为Na2CO3+BaCl2=BaCO3↓+2NaCl)…
①你认为滴加过量BaCl2试液的目的是______;
②如何判断BaCl2试液已经过量?______;
③你认为还应继续进行的实验是______,则说明原NaOH固体已经完全变质.
查看答案和解析>>
科目:czhx
来源:
题型:
归纳与演绎是重要的科学方法,也是常用的化学学习方法。
(1)某研究小组对用双氧水分解生成水和氧气的实验条件进行探究,完成了以下实验:
①往盛有5 ml 5%H2O2溶液的试管中,伸入带火星的木条,木条不复燃。
②往盛有5 ml w% H2O2溶液的试管中,加入a g MnO2,伸入带火星的木条,木条复燃。
③往盛有5 ml w% H2O2溶液的试管中,加入a g Fe2O3,伸入带火星的木条,木条复燃。
④经检验,②③中反应后试管中仍分别含有a gMnO2和 ag Fe2O3
问题一:请你写出用双氧水和二氧化锰制氧气的化学反应方程式
问题二:MnO2和 Fe2O3在上述反应中的作用是 ;实验②③中的H2O2的浓度(w%)以 为宜。
(2)研究小组还对溶液浓度、催化剂的种类等实验条件进行探究。下表选取了部分实验数据:用足量等体积H2O2溶液制取相同体积O2所需要的时间
浓度 时间(min)
条件 | 30%H2O2 | 15%H2O2 | 5%H2O2 |
a g MnO2 | 0.2 | 0.8 | 2.0 |
ag Fe2O3 | 0.7 | 9.0 | 16.0 |
问题三:从上表中能得到哪些结论?(写出一条结论)
查看答案和解析>>
科目:czhx
来源:
题型:解答题
归纳与演绎是重要的科学方法,也是常用的化学学习方法.
(1)我们已经学习过实验室制取O2、CO2、H2(Zn和稀硫酸反应)三种气体的反应原理、制取与收集方法.请你归纳出实验室制取气体反应的共同点______(填序号)
①需要加热 ②使用催化剂 ③没有气体参加反应 ④原料为纯净物 ⑤只生成一种气体
(2)下列是实验室常用的仪器

写出仪器名称:a是______,c是______;写出d的一种用途______.
(3)化学上可以通过多种反应制得NH3(极易溶于水,密度比空气小),例如
①2NH4Cl(固)+Ca(OH)2(固) CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O
②NH4HCO3(固) NH3↑+CO2↑+H2O
NH3↑+CO2↑+H2O
③CaO(固)+NH3.H2O(浓)═NH3↑+Ca(OH)2
我将选择反应______(只写一个,填序号)作为实验室制取氨气的反应原理.我需要用上面仪器中的______(填序号)来装配氨气发生装置(连接装置已经省略),我采用的收集方法是______.我选择的发生装置还可以用来制取______气体.
(4)某研究小组对用双氧水分解生成水和氧气的实验条件进行探究,完成了以下实验:
①往盛有5ml 5%H2O2溶液的试管中,伸入带火星的木条,木条不复燃.
②往盛有5ml w% H2O2溶液的试管中,加入a g MnO2,伸入带火星的木条,木条复燃.
③往盛有5ml w% H2O2溶液的试管中,加入a g Fe2O3,伸入带火星的木条,木条复燃.
④经检验,②③中反应后试管中仍分别含有a gMnO2和 ag Fe2O3
问题一:请你写出用双氧水和二氧化锰制氧气的化学反应方程式
______
问题二:MnO2和 Fe2O3在上述反应中的作用是______.
实验②④中的H2O2的浓度(w%)以______为宜. |
研究小组还对溶液浓度、催化剂的种类等实验条件进行探究.下表选取了部分实验数据:用足量等体积H
2O
2溶液制取相同体积O
2所需要的时间
浓度
时间(min)
条件 | 30%H2O2 | 15%H2O2 | 5%H2O2 |
| ag MnO2 | 0.2 | 0.8 | 2.0 |
| ag Fe2O3 | 0.7 | 9.0 | 16.0 |
查看答案和解析>>
科目:czhx
来源:
题型:
归纳与演绎是重要的科学方法,也是常用的化学学习方法。
(1)某研究小组对用双氧水分解生成水和氧气的实验条件进行探究,完成了以下实验:
①往盛有5 ml 5%H2O2溶液的试管中,伸入带火星的木条,木条不复燃。
②往盛有5 ml w% H2O2溶液的试管中,加入a g MnO2,伸入带火星的木条,木条复燃。
③往盛有5 ml w% H2O2溶液的试管中,加入a g Fe2O3,伸入带火星的木条,木条复燃。
④经检验,②③中反应后试管中仍分别含有a gMnO2和 ag Fe2O3
问题一:请你写出用双氧水和二氧化锰制氧气的化学反应方程式
问题二:MnO2和 Fe2O3在上述反应中的作用是 ;实验②③中的H2O2的浓度(w%)以 为宜。
(2)研究小组还对溶液浓度、催化剂的种类等实验条件进行探究。下表选取了部分实验数据:用足量等体积H2O2溶液制取相同体积O2所需要的时间
浓度 时间(min)
条件 | 30%H2O2 | 15%H2O2 | 5%H2O2 |
a g MnO2 | 0.2 | 0.8 | 2.0 |
ag Fe2O3 | 0.7 | 9.0 | 16.0 |
问题三:从上表中能得到哪些结论?(写出一条结论)
查看答案和解析>>
科目:czhx
来源:
题型:解答题
实验室里NaOH固体必须密封保存,其原因是______,
现实验室里有一包白色NaOH样品,某兴趣小组同学为了确定这样品的成分,对其可能的组成进行了下列探究.
(1)【猜想】依据所学知识,兴趣小组同学对这种白色粉末的成分作了如下猜想:
①可能没有变质,全是NaOH;②可能完全变质,全是Na2CO3;你认为还有一种可能是______.
(2)【实验】为了验证猜想,他们做了下面实验:
实验一:取少量白色粉末溶于水,向所得溶液里滴加酚酞试液,溶液变为红色.
实验二:取少量白色粉末,滴加稀盐酸,有气体生成.
(3)【结论】由上述实验过程和实验现象,分析得到下面结论.
结论一:由实验一得到的结论是白色粉末是NaOH.请你判断该结论是否正确,并简述理由:______
综合分析上述两个实验,你得到的结论是:______
(4)【继续探究】兴趣小组同学在分析和研究了上述实验及实验结论后,为了确认白色粉末的成分,查阅资料并做了下面的实验三:取少量白色粉末溶于水,向所得溶液里滴加过量的BaCl2试液,有白色沉淀产生(反应的方程式为Na2CO3+BaCl2=BaCO3↓+2NaCl)
①你认为滴加过量BaCl2试液的目的是______;
②如何判断BaCl2试液已经过量?______;
③你认为还应继续进行的实验是______,则说明原NaOH固体已经完全变质.
查看答案和解析>>
科目:czhx
来源:2008年广东省广州市花都区中考化学一模试卷(解析版)
题型:填空题
归纳与演绎是重要的科学方法,也是常用的化学学习方法.
(1)某研究小组对用双氧水分解生成水和氧气的实验条件进行探究,完成了以下实验:
①往盛有5ml 5%H
2O
2溶液的试管中,伸入带火星的木条,木条不复燃.
②往盛有5ml w%H
2O
2溶液的试管中,加入a g MnO
2,伸入带火星的木条,木条复燃.
③往盛有5ml w%H
2O
2溶液的试管中,加入a g Fe
2O
3,伸入带火星的木条,木条复燃.
④经检验,②③中反应后试管中仍分别含有a gMnO
2和 ag Fe
2O
3问题一:请你写出用双氧水和二氧化锰制氧气的化学反应方程式
问题二:MnO
2和 Fe
2O
3在上述反应中的作用是
;实验②③中的H
2O
2的浓度(w%)以
为宜.
(2)研究小组还对溶液浓度、催化剂的种类等实验条件进行探究.下表选取了部分实验数据:用足量等体积H
2O
2溶液制取相同体积O
2所需要的时间
浓度
时间(min)
条件 | 30% H2O2 | 15% H2O2 | 5% H2O2 |
| Ag MnO2 | 0.2 | 0.8 | 2.0 |
ag Fe2O3
| 0.7 | 9.0 | 16.0 |
问题三:从上表中能得到哪些结论?(写出一条结论)
.
查看答案和解析>>
科目:czhx
来源:2007-2008学年江苏省宿迁市宿豫区九年级(上)期中化学试卷(解析版)
题型:填空题
归纳与演绎是重要的科学方法,也是常用的化学学习方法.
(1)某研究小组对用双氧水分解生成水和氧气的实验条件进行探究,完成了以下实验:
①往盛有5ml 5%H
2O
2溶液的试管中,伸入带火星的木条,木条不复燃.
②往盛有5ml w%H
2O
2溶液的试管中,加入a g MnO
2,伸入带火星的木条,木条复燃.
③往盛有5ml w%H
2O
2溶液的试管中,加入a g Fe
2O
3,伸入带火星的木条,木条复燃.
④经检验,②③中反应后试管中仍分别含有a gMnO
2和 ag Fe
2O
3问题一:请你写出用双氧水和二氧化锰制氧气的化学反应方程式
问题二:MnO
2和 Fe
2O
3在上述反应中的作用是
;实验②③中的H
2O
2的浓度(w%)以
为宜.
(2)研究小组还对溶液浓度、催化剂的种类等实验条件进行探究.下表选取了部分实验数据:用足量等体积H
2O
2溶液制取相同体积O
2所需要的时间
浓度
时间(min)
条件 | 30% H2O2 | 15% H2O2 | 5% H2O2 |
| Ag MnO2 | 0.2 | 0.8 | 2.0 |
ag Fe2O3
| 0.7 | 9.0 | 16.0 |
问题三:从上表中能得到哪些结论?(写出一条结论)
.
查看答案和解析>>
科目:czhx
来源:
题型:
实验室里NaOH固体必须密封保存,其原因是 ,
。现实验室里有一包白色NaOH样品,某兴趣小组同学为了确定这样品的成分,对其可能的组成进行了下列探究。
⑴【猜想】依据所学知识,兴趣小组同学对这种白色粉末的成分作了如下猜想:
①可能没有变质,全是NaOH;②可能完全变质,全是Na2CO3;你认为还有一种可能是
。
⑵【实验】为了验证猜想,他们做了下面实验:
实验一:取少量白色粉末溶于水,向所得溶液里滴加酚酞试液,溶液变为红色。
实验二:取少量白色粉末,滴加稀盐酸,有气体生成。
⑶【结论】由上述实验过程和实验现象,分析得到下面结论。
结论一:由实验一得到的结论是白色粉末是NaOH。
请你判断该结论是否正确,并简述理由:
综合分析上述两个实验,你得到的结论是:
⑷【继续探究】兴趣小组同学在分析和研究了上述实验及实验结论后,为了确认白色粉末的成分,查阅资料并做了下面的实验三:取少量白色粉末溶于水,向所得溶液里滴加过量的BaCl2试液,有白色沉淀产生(反应的方程式为Na2CO3+ BaCl2 =BaCO3↓+2NaCl)……
①你认为滴加过量BaCl2试液的目的是 ;
②如何判断BaCl2试液已经过量? ;
③你认为还应继续进行的实验是 ,则说明原NaOH固体已经完全变质。
查看答案和解析>>
科目:czhx
来源:2007-2008学年江苏省南京市伯乐中学九年级(下)月考化学试卷(3月份)(解析版)
题型:解答题
实验室里NaOH固体必须密封保存,其原因是______,
现实验室里有一包白色NaOH样品,某兴趣小组同学为了确定这样品的成分,对其可能的组成进行了下列探究.
(1)【猜想】依据所学知识,兴趣小组同学对这种白色粉末的成分作了如下猜想:
①可能没有变质,全是NaOH;②可能完全变质,全是Na2CO3;你认为还有一种可能是______.
(2)【实验】为了验证猜想,他们做了下面实验:
实验一:取少量白色粉末溶于水,向所得溶液里滴加酚酞试液,溶液变为红色.
实验二:取少量白色粉末,滴加稀盐酸,有气体生成.
(3)【结论】由上述实验过程和实验现象,分析得到下面结论.
结论一:由实验一得到的结论是白色粉末是NaOH.请你判断该结论是否正确,并简述理由:______
综合分析上述两个实验,你得到的结论是:______
(4)【继续探究】兴趣小组同学在分析和研究了上述实验及实验结论后,为了确认白色粉末的成分,查阅资料并做了下面的实验三:取少量白色粉末溶于水,向所得溶液里滴加过量的BaCl2试液,有白色沉淀产生(反应的方程式为Na2CO3+BaCl2=BaCO3↓+2NaCl)…
①你认为滴加过量BaCl2试液的目的是______;
②如何判断BaCl2试液已经过量?______;
③你认为还应继续进行的实验是______,则说明原NaOH固体已经完全变质.
查看答案和解析>>
科目:czhx
来源:2007年江苏省南京市白下区中考化学一模试卷(解析版)
题型:解答题
归纳与演绎是重要的科学方法,也是常用的化学学习方法.
(1)我们已经学习过实验室制取O
2、CO
2、H
2(Zn和稀硫酸反应)三种气体的反应原理、制取与收集方法.请你归纳出实验室制取气体反应的共同点______(填序号)
①需要加热 ②使用催化剂 ③没有气体参加反应 ④原料为纯净物 ⑤只生成一种气体
(2)下列是实验室常用的仪器

写出仪器名称:a是______,c是______;写出d的一种用途______.
(3)化学上可以通过多种反应制得NH
3(极易溶于水,密度比空气小),例如
①2NH
4Cl(固)+Ca(OH)
2(固)

CaCl
2+2NH
3↑+2H
2O
②NH
4HCO
3(固)
NH
3↑+CO
2↑+H
2O
③CaO(固)+NH
3.H
2O(浓)═NH
3↑+Ca(OH)
2我将选择反应______(只写一个,填序号)作为实验室制取氨气的反应原理.我需要用上面仪器中的______(填序号)来装配氨气发生装置(连接装置已经省略),我采用的收集方法是______.我选择的发生装置还可以用来制取______气体.
(4)某研究小组对用双氧水分解生成水和氧气的实验条件进行探究,完成了以下实验:
①往盛有5ml 5%H
2O
2溶液的试管中,伸入带火星的木条,木条不复燃.
②往盛有5ml w% H
2O
2溶液的试管中,加入a g MnO
2,伸入带火星的木条,木条复燃.
③往盛有5ml w% H
2O
2溶液的试管中,加入a g Fe
2O
3,伸入带火星的木条,木条复燃.
④经检验,②③中反应后试管中仍分别含有a gMnO
2和 ag Fe
2O
3问题一:请你写出用双氧水和二氧化锰制氧气的化学反应方程式
______ |
2H
2O+O
2↑
查看答案和解析>>



 CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O NH3↑+CO2↑+H2O
NH3↑+CO2↑+H2O
 CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O NH3↑+CO2↑+H2O
NH3↑+CO2↑+H2O