
科目:gzhx 来源:2013-2014学年江西省南昌市高二上学期期中测试理科化学试卷(甲)(解析版) 题型:选择题
将2.0molPCl3,和1.0molCl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g)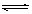 PCl5(g)达到平衡时,PCl5为0.40mol,如果此时移走1.0molPCl3和0.50molCl2,在相同温度下再达平衡时PCl5的物质的量是
PCl5(g)达到平衡时,PCl5为0.40mol,如果此时移走1.0molPCl3和0.50molCl2,在相同温度下再达平衡时PCl5的物质的量是
A.0.40mol B.小于0.20mol C.0.20mol D.大于0.20mol,小于0.40mol
科目:gzhx 来源: 题型:
 硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g)
硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g)| 催化剂 | △ |
科目:gzhx 来源: 题型:阅读理解
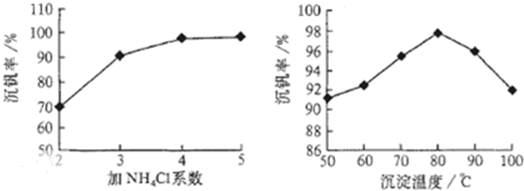
 工业上以黄铁矿为原料生产硫酸主要分为三个阶段进行,即煅烧、催化氧化、吸收.请回答下列个问题:
工业上以黄铁矿为原料生产硫酸主要分为三个阶段进行,即煅烧、催化氧化、吸收.请回答下列个问题:| 催化剂 | △ |
科目:gzhx 来源: 题型:
科目:gzhx 来源: 题型:阅读理解
科目:gzhx 来源: 题型:
 (2009•泰州模拟)二氧化硫是常用的化工原料,但也是大气的主要污染物.
(2009•泰州模拟)二氧化硫是常用的化工原料,但也是大气的主要污染物.| 催化剂 | △ |
科目:gzhx 来源: 题型:
 氮的氧化物和SO2是常见的化工原料,但也是大气的主要污染物.综合治理其污染是化学家研究的主要内容.根据题意完成下列各题:
氮的氧化物和SO2是常见的化工原料,但也是大气的主要污染物.综合治理其污染是化学家研究的主要内容.根据题意完成下列各题:
| ||
科目:gzhx 来源: 题型:
 (2009•抚顺模拟)二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物.综合治理其污染是环境化学当前的重要研究内容之一.
(2009•抚顺模拟)二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物.综合治理其污染是环境化学当前的重要研究内容之一.| 催化剂 | △ |

科目:gzhx 来源: 题型:
 二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物.综合治理其污染是环境化学当前的重要研究内容之一.
二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物.综合治理其污染是环境化学当前的重要研究内容之一.| 催化剂 | △ |
科目:gzhx 来源:2014届浙江省高二下学期期中考试化学试卷(解析版) 题型:选择题
已知反应:2SO2(g)+O2(g) 2SO3(g) ΔH<0。某温度下,将2 mol SO2和
2SO3(g) ΔH<0。某温度下,将2 mol SO2和
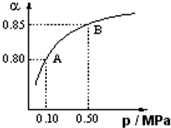
1 mol O2置于10 L体积可变的密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是
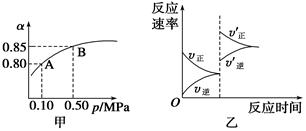

A.由图甲知,A点SO2的平衡浓度一定为0.04 mol/L
B.由图甲知,B点SO2、O2、SO3的平衡浓度之比为2∶1∶2
C.达平衡后,缩小容器容积,则反应速率变化图象可以用图乙表示
D.压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1
科目:gzhx 来源: 题型:
(1)从反应开始至达到化学平衡,生成SO3平均反应速率为___________;平衡时SO2转化率为___________。
(2)下列叙述能证明该反应已经达到化学平衡状态的是___________。(填标号,下同)
A.容器内压强不再发生变化
B.SO2的体积分数不再发生变化
C.容器内气体原子总数不再发生变化
D.相同时间内消耗2 n mol SO2的同时消耗n mol O2
E.相同时间内消耗2 n mol SO2的同时生成n mol O2
科目:gzhx 来源: 题型:
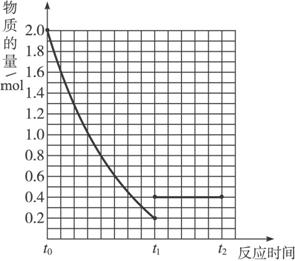
(1)反应进行到t1时,SO2的体积分数为____________。
(2)若在t1时充入一定量的氩气(Ar),SO2的物质的量将____________(填“增大”“减小”或“不变”)。
(3)若在t1时升温,重新达到平衡状态,新平衡的混合物中气体的总物质的量____________2.1 mol(填“<”“>”或“=”=,并简单说明原因_________________________。
(4)若其他条件不变,在t1时再加入0.2 mol SO2、0.1 mol O2和1.8 mol SO3,在下图中作出从t0→t1→t2这段时间内SO2的物质的量的变化曲线。
科目:gzhx 来源:2014届山东省聊城市七校联考高二上学期期末检测化学试卷(解析版) 题型:选择题
已知反应:2SO2(g)+O2(g)  2SO3(g);ΔH<0。某温度下,将2 mol SO2和1 mol
O2置于10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是
2SO3(g);ΔH<0。某温度下,将2 mol SO2和1 mol
O2置于10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是


A.由图甲知,A点SO2的平衡浓度为0.4 mol/L
B.由图甲知,B点SO2、O2、SO3的平衡浓度之比为2∶1∶2
C.达平衡后,缩小容器容积,则反应速率变化图象可以用图乙表示
D.压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1
科目:gzhx 来源:2011-2012年江西省高二上学期期中考试化学(理)试题 题型:选择题
已知反应:2SO2(g)+O2(g)  2SO3(g) ΔH<0。某温度下,将2
mol SO2和1 mol O2置于10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是
( )
2SO3(g) ΔH<0。某温度下,将2
mol SO2和1 mol O2置于10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是
( )
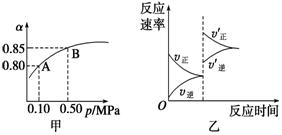
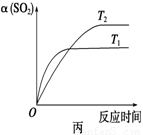
A.由图甲知,A点SO2的平衡浓度为0.4 mol/L
B.由图甲知,B点SO2、O2、SO3的平衡浓度之比为2∶1∶2
C.达平衡后,缩小容器容积,则反应速率变化图象可以用图乙表示
D.压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1
科目:gzhx 来源: 题型:
(1)硫酸生产中,SO2催化氧化生成SO3:
2SO2(s)+O2(g)![]() 2SO3(g).
2SO3(g).
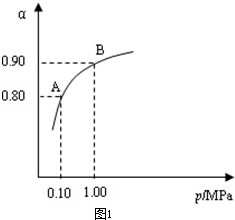
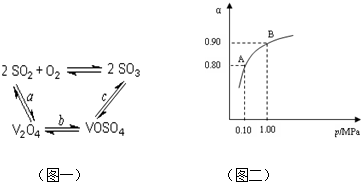
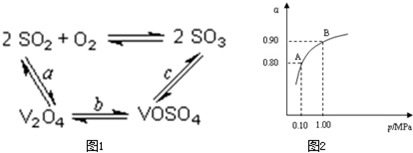
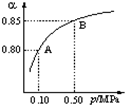
某温度下,SO2的平衡转化率(α)与体系总压强(P)的关系如下图所示。根据图示回答下列问题:

①将2.0 molSO2和1.0molO2置于10 L密闭容器中,反应达平衡后,体系总压强为0.10MPa。该反应的平衡常数等于__________。
②平衡状态由A变到B时,平衡常数K(A)_______K(B)(填“>”、“<”或“=”)。
(2)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol-1
若用标准状况下4.48 L CH4还原NO2至N2,整个过程中转移的电子总数为__________(阿伏加德罗常数的值用NA表示),放出的热量为___________kJ。
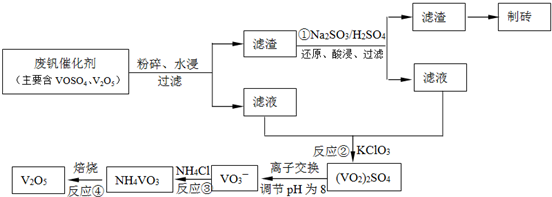
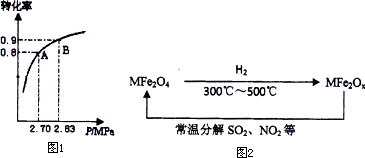
(3)新型纳米材料氧缺位铁酸盐(MFe2Ox,3<x<4,M=Mn、Co、Zn或Ni)由铁酸盐(MFe2O4)经高温还原而得,常温下,它能使工业废气中的酸性氧化物分解除去。转化流程如图所示:
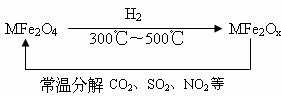
请写出MFe2Ox分解SO2的化学方程式________________(不必配平)。
科目:gzhx 来源:2012-2013学年福建省四地六校高二第三次月考化学试卷(带解析) 题型:单选题
已知反应:2SO2(g)+O2(g)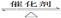 2SO3(g);ΔH<0。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是
2SO3(g);ΔH<0。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是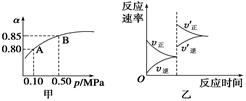
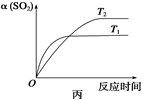
| A.由图甲知,A点SO2的平衡浓度为0.4 mol/L |
| B.由图甲知,B点SO2、O2、SO3的平衡浓度之比为2∶1∶2 |
| C.达平衡后,缩小容器容积,则反应速率变化图象可以用图乙表示 |
| D.压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1 |
科目:gzhx 来源: 题型:
二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物。综合治理其污染是环境化学当前的重要研究内容之一。
(1)硫酸生产中,SO2催化氧化生成SO3:
2SO2(g)+O2(g)![]() 2SO3(g)
2SO3(g)
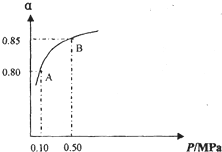
某温度下,SO2的平衡转化率(a)与体系总压强(p)的关系如右图所示。根据图示回答下列问题:
①将2.0mol SO2和1.0mol O2置于10L密闭容器中,反应达平衡后,体系总压强为0.10MPa。该反应的平衡常数等于_____。
②平衡状态由A变到B时.平衡常数K(A)_______K(B)(填“>”、“<”或“=”)。
(2)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160 kJ·mol-1
若用标准状况下4.48L CH4还原NO2至N2整个过程中转移的电子总数为______(阿伏加德罗常数的值用NA表示),放出的热量为______kJ。
(3)新型纳米材料氧缺位铁酸盐(MFe2Ox 3<x<4,M=Mn、Co、Zn或Ni=由铁酸盐(MFe2O4)经高温还原而得,常温下,它能使工业废气中的酸性氧化物分解除去。转化流程如图所示:
请写出MFe2Ox分解SO2的化学方程式 (不必配平)。
科目:gzhx 来源: 题型:
将2 mol SO2和1 mol O2充入一容积固定的密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g)![]() 2SO3(g),下列哪些量不再变化时,并不能说明化学反应已达平衡状态( )
2SO3(g),下列哪些量不再变化时,并不能说明化学反应已达平衡状态( )
A.混合气体的密度
B.混合气体的压强
C.混合气体的平均相对分子质量
D.混合气体的总物质的量
科目:gzhx 来源: 题型:
将2 L乙烯和1 L甲烷的混合气体于150 ℃,1.01×105 Pa下和50 L空气充分燃烧后所得混合气体的体积是(燃烧前后状态相同)( )
A.43 L B.50 L C.53 L D.49 L
科目:gzhx 来源: 题型:
将2 mol A和1 mol B充入某密闭容器中发生反应:2A(g)+B(g)![]() xC(g),达到化学平衡后,C的体积分数为a。假设该反应的条件分别和下列各选项的条件相同,下列判断正确的是( )
xC(g),达到化学平衡后,C的体积分数为a。假设该反应的条件分别和下列各选项的条件相同,下列判断正确的是( )
A.若在恒温恒压下,当x=1时,按1.5 mol A、1 mol C作为起始物质,达到平衡后,C的体积分数仍为a
B.若在恒温恒容下,当x=2时,将1 mol B、2 mol C作为起始物质,达到平衡后,C的体积分数仍为a
C.若在恒温恒压下,当x=3时,按1 mol A、1 mol B、6 mol C作为起始物质,达到平衡后,C的体积分数仍为a
D.若在恒温恒容下,按0.6 mol A、0.3 mol B、1.4 mol C作为起始物质,达到平衡后,C的体积分数仍为a,则x为2或3