
科目:gzhx 来源: 题型:
常温下,下列溶液pH=2的是( )
A.0.01 mol·L-1 CH3COOH溶液
B.10-3 mol·L-1 H2SO4浓缩到原体积的110.
C.pH=1的H2SO4溶液稀释10倍
D.c(OH-)=10-2 mol·L-1 的某溶液
科目:gzhx 来源: 题型:
常温下,下列溶液c(H+)=0.01 mol·L-1的是( )
A.0.01 mol·L-1 CH3COOH溶液
B.10-3 mol·L-1 H2SO4浓缩到原体积的110.
C.pH=1的H2SO4稀释10倍
D.c(OH-)=10-2 mol·L-1的某溶液
科目:gzhx 来源: 题型:单选题
科目:gzhx 来源: 题型:
A.HNO3溶液 B.Ba(OH)2溶液
C.H2SO4溶液 D.HCl溶液
科目:gzhx 来源:2013届江苏省盐城市明达中学高三上学期学情调研考试化学试卷(带解析) 题型:单选题
下列有关实验原理、方法和结论都正确的是
| A.向溶液X 中先滴加稀硝酸,再滴加Ba(NO3)2溶液,出现白色沉淀说明溶液X 中一定含有SO42- |
| B.取少量溶液X,向其中加入适量新制氨水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有Fe2+ |
| C.粗略配制浓度为2 mol·L—1的NaCl溶液,可将58.5gNaCl加入到盛有500mL水的烧杯中,搅拌、溶解 |
| D.对某固体进行焰色反应实验,火焰呈黄色,说明该物质为一定钠盐 |
科目:gzhx 来源:2012-2013学年浙江省苍南县求知中学高二上学期期中考试文科化学试卷(带解析) 题型:计算题
(6分)某同学欲配制250 mL 2 mol·L-1的碳酸钠溶液,并进行有关实验。请回答下列问题:
(1)需称量无水碳酸钠的质量 g。
(2)配制该碳酸钠溶液时使用的仪器除天平(带砝码)、烧杯、玻璃棒外,还必须用到的仪器有 、 等。
(3)取所配制的碳酸钠溶液125 mL,向其加入125 mL 3mol·L-1的硫酸溶液,待充分反应后,生成的气体在标准状况下所占的体积为(假设产生的气体全部逸出) ;设反应后溶液的体积为250mL,则反应后溶液中Na+的物质的量浓度为 。
科目:gzhx 来源:2013届山东济宁金乡一中高二12月月考化学试卷 题型:填空题
(12分)
(1)室温下,在pH=12的某种溶液中,由水电离的c(OH-)为____________。
(2)等体积的下列溶液中,阳离子的总物质的量最大的是____________。
①0.2 mol·L-1的CuSO4溶液
②0.1 mol·L-1的Na2CO3
③0.2 mol·L-1的KCl
④0.1 mol·L-1的Na2SO4
(3)浓度为0.100 mol·L-1的下列各物质的溶液中,c(NH4+)由大到小的顺序是_________________(填序号)。
①NH4Cl ②NH4HSO4 ③NH3·H2O ④CH3COONH4
(4)某二元酸(化学式用H2A表示)在水中的电离方程式是:
H2A====H++HA- , HA- H++A2-
。
H++A2-
。
①则Na2A溶液显__________________(填“酸性”“中性”或“碱性”),理由是_______________________________(用离子方程式表示)。
②若有0.1 mol·L-1 Na2A的溶液,其中各种离子浓度由大到小的顺序是: (填序号)。
A.c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+)
B.c(Na+)>c(OH-)>c(HA-)>c(A2-)>c(H+)
C.c(Na+)>c(H+)>c(A2-)>c(OH-)>c(HA-)
D.c(A2-)>c(Na+)>c(OH-)>c(H+)>c(HA-)
科目:gzhx 来源:2014届浙江省高二上学期期中考试文科化学试卷(解析版) 题型:计算题
(6分) 某同学欲配制250 mL 2 mol·L-1 的碳酸钠溶液,并进行有关实验。请回答下列问题:
(1)需称量无水碳酸钠的质量 g。
(2)配制该碳酸钠溶液时使用的仪器除天平(带砝码)、烧杯、玻璃棒外,还必须用到的仪器有 、 等。
(3)取所配制的碳酸钠溶液125 mL,向其加入125 mL 3mol·L-1 的硫酸溶液,待充分反应后,生成的气体在标准状况下所占的体积为(假设产生的气体全部逸出) ;设反应后溶液的体积为250mL,则反应后溶液中Na+的物质的量浓度为 。
科目:gzhx 来源: 题型:
A.HNO3溶液 B.Ba(OH)2溶液 C.H2SO4溶液 D.HCl溶液
科目:gzhx 来源:2010年海南省高三上学期教学质量监测(一)化学 题型:选择题
将5.4 g Al 投入到200.0 mL 2.0 mol·L-1的某溶液中有氢气产生,充分反应后有金属剩余。该溶液可能为
A、HNO3溶液 B、Ba(OH)2溶液 C、H2SO4溶液 D、HCl溶液
科目:gzhx 来源: 题型:
将5.4 g Al投入到200.0 mL 2.0 mol·L-1的某溶液中有氢气产生,充分反应后有金属剩余。该溶液可能为( )
A.HNO3溶液 B.Ba(OH)2溶液
C.H2SO4溶液 D.HCl溶液
科目:gzhx 来源:2011-2012学年山东济宁金乡一中高二12月月考化学试卷 题型:填空题
(12分)
(1)室温下,在pH=12的某种溶液中,由水电离的c(OH-)为____________。
(2)等体积的下列溶液中,阳离子的总物质的量最大的是____________。
①0.2 mol·L-1的CuSO4溶液
②0.1 mol·L-1的Na2CO3
③0.2 mol·L-1的KCl
④0.1 mol·L-1的Na2SO4
(3)浓度为0.100 mol·L-1的下列各物质的溶液中,c(NH4+)由大到小的顺序是_________________(填序号)。
①NH4Cl ②NH4HSO4 ③NH3·H2O ④CH3COONH4
(4)某二元酸(化学式用H2A表示)在水中的电离方程式是:
H2A====H++HA-, HA- H++A2- 。
H++A2- 。
①则Na2A溶液显__________________(填“酸性”“中性”或“碱性”),理由是_______________________________(用离子方程式表示)。
②若有0.1 mol·L-1 Na2A的溶液,其中各种离子浓度由大到小的顺序是: (填序号)。
| A.c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+) |
| B.c(Na+)>c(OH-)>c(HA-)>c(A2-)>c(H+) |
| C.c(Na+)>c(H+)>c(A2-)>c(OH-)>c(HA-) |
| D.c(A2-)>c(Na+)>c(OH-)>c(H+)>c(HA-) |
科目:gzhx 来源: 题型:
Na2S2O3+2HCl![]() 2NaCl+S+SO2+H2O,一同学在下午活动课中,配制了0.2 mol·L-1的盐酸置于大烧杯中,并取了3 mL 0.1 mol·L-1 的Na2S2O3溶液与3 mL该盐酸反应,产生明显浑浊约需时间t s,由于另有安排,停止了实验。第二天又用了3 mL 0.2 mol·L-1的Na2S2O3溶液与原盐酸反应,产生浑浊的时间也需t s左右。于是他得出结论:浓度对化学反应速率的影响不大,请你评价该同学的这次实验。
2NaCl+S+SO2+H2O,一同学在下午活动课中,配制了0.2 mol·L-1的盐酸置于大烧杯中,并取了3 mL 0.1 mol·L-1 的Na2S2O3溶液与3 mL该盐酸反应,产生明显浑浊约需时间t s,由于另有安排,停止了实验。第二天又用了3 mL 0.2 mol·L-1的Na2S2O3溶液与原盐酸反应,产生浑浊的时间也需t s左右。于是他得出结论:浓度对化学反应速率的影响不大,请你评价该同学的这次实验。
(1)结论是_________。
A.可靠的 B.不可靠的 C.基本正确 D.可能正确,也可能不正确
(2)一般对比实验都要控制条件,且再现性好。
①请评价他实验控制的条件。__________________________________________________。
②请评价他实验现象的对比方法。______________________________________________。
若他的对比方法不好,请你给出正确的对比方法(若他的方法可行,此问可不回答)。___________________________________。
科目:gzhx 来源:2013-2014学年浙江省金丽衢十二校高三第二次联考理综化学试卷(解析版) 题型:实验题
(14分)FeSO4·7H2O广泛用于医药和工业领域,以下是FeSO4·7H2O的实验室制备流程图。根据题意完成下列填空:

(1)铁屑与稀硫酸反应前,应用10% Na2CO3溶液浸泡几分钟,操作目的是_____,浸泡后,用____(填操作方法)分离并洗涤铁屑。
(2)操作a为_______________。
(3)最后得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质;
②____________________。
(4) FeSO4·7H2O是某些补血剂的主要成分,实验室要测定某补血剂中铁元素的含量。
I.方案一:可用KMn04溶液进行氧化还原滴定。在配制100mL 1.00 × 10 - 2 mol·L-1的KMnO4溶液时,所用的仪器有天平、药匙、烧杯、玻璃棒,还有___________(填仪器名称)。在配制过程中,下列说法正确的是____________(填序号字母)。
A.KMnO4溶于水不放热,可以直接在容量瓶中溶解
B.容量瓶洗涤后不需干燥即可直接用于实验
C.定容后摇匀,凹液面低于刻度线,再加水至凹液面最低点与刻度线相平
D.如果定容时加水超过刻度线必须毓配制
II.方案二:将FeSO4·7H2O最终转化为Fe2O3,测定质量变化,操作流程如下:

①步骤④中一系列操作依次是:过滤、洗涤、______、冷却、称量。
②假设实验过程中Fe无损耗,则每片补血剂含铁元素的质量______g(用含a的代数式表示)。
③若步骤③加入X溶液的量不足,则最后测出每片补血剂含铁元素的质量将______(填“偏大,’.“偏小”或“不变”)。
科目:gzhx 来源: 题型:
A.0.01 mol·L-1 CH3COOH溶液
B.10-3 mol·L-1 H2SO4浓缩到原来体积的![]()
C.pH=1的醋酸溶液稀释10倍
D.c(OH-)=10-12 mol·L-1的某溶液
科目:gzhx 来源:2013-2014学年北京市海淀区高三上学期期末考试化学试卷(解析版) 题型:填空题
硫酸工厂的烟气中含有SO2,有多种方法可实现烟气脱硫。
(1)工业制硫酸的过程中,SO2被氧气氧化的化学方程式为 。
(2)“湿式吸收法”利用吸收剂与SO2发生反应从而脱硫。
已知:25℃时,H2SO3
 HSO3 -+H+
K=1.5×10-2
HSO3 -+H+
K=1.5×10-2
H2CO3 HCO3 -+H+ K=4.4×10-7
HCO3 -+H+ K=4.4×10-7
下列试剂中适合用作该法吸收剂的是 (填字母序号)。
a.石灰乳 b. Na2SO3溶液 c. Na2CO3溶液
②“钠碱法”用NaOH溶液作吸收剂,向100 mL 0.2 mol·L-1 的NaOH溶液中通入标准状况下0.448 L SO2气体,反应后测得溶液pH<7,则溶液中下列各离子浓度关系正确的是 (填字母序号)。
a.c(HSO3-)> c(SO32-)> c(H2SO3)
b.c(Na+)>c(HSO3-)> c(H+)> c(SO32-)
c.c(Na+)+c(H+)= c(HSO3-)+c(SO32-)+c(OH-)
(3)某硫酸厂拟用烟气处理含Cr2O72-的酸性废水,在脱硫的同时制备Cr2O3产品。具体流程如下:

①吸收塔中反应后的铬元素以Cr3+形式存在,则其中发生反应的离子方程式为 。
②中和池中的反应除生成Cr(OH)3沉淀外,还会产生某种气体,该气体的化学式为 。
科目:gzhx 来源: 题型:
科目:gzhx 来源:2012-2013学年湖南省益阳市一中高二上学期期末考试理科化学试卷(带解析) 题型:填空题
(20分)选修四模块的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理。请回答下列问题:
(1) 一定温度下,在一个固定容积的密闭容器中,可逆反应 A(g) +2B(g)  4C (g) △H >0 达到平衡时,c(A) ="2" mol·L-1,c ( B) =" 7" mol·L-1,c ( C) =" 4" mol·L-1。试确定B的起始浓度c (B)的取值范围是 ;若改变条件重新达到平衡后体系中C的质量分数增大,下列措施可行的是 。
4C (g) △H >0 达到平衡时,c(A) ="2" mol·L-1,c ( B) =" 7" mol·L-1,c ( C) =" 4" mol·L-1。试确定B的起始浓度c (B)的取值范围是 ;若改变条件重新达到平衡后体系中C的质量分数增大,下列措施可行的是 。
A. 增加C的物质的量 B. 加压
C. 升温 D.使用催化剂
(2)常温下,取 pH=2的盐酸和醋酸溶液各100mL, 向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如右图所示。则图中表示醋酸溶液中pH变化曲线的是 ( 填“A”或“B”)。 设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为 m2。 则
m1 m2 ( 选填“<”、“=”、“>”)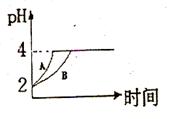
(3) 在体积为3L的密闭容器中,CO与H2在一定条件下反应生成甲醇:CO ( g) + 2H2( g) → CH3OH(g) ΔH= —91kJ·mol-1。反应达到平衡时,平衡常数表达式K= ,升高温度,K值 (填“增大”、“减小”或“不变”)。
(4) 难溶电解质在水溶液中也存在溶解平衡。在常温下,溶液里各离子浓度以它们化学计量数为方次的乘积是一个常数,叫溶度积常数。例如: Cu(OH)2(s) Cu2+ (aq) + 2OH - ( aq),Ksp =" c" (Cu2+ ) c 2(OH - ) =" 2×10" -20。当溶液中各离子浓度计量数方次的乘积大于溶度积时,则产生沉淀。若某CuSO4溶液里c( Cu2+) ="0.02" mol·L-1,如果生成Cu(OH)2沉淀,应调整溶液pH,使pH大于 ; 要使0.2 mol·L-1的CuSO4溶液中Cu2+沉淀较为完全 ( 使Cu2+浓度降至原来的万分之一)则应向溶液里加NaOH溶液,使溶液pH等于 。
Cu2+ (aq) + 2OH - ( aq),Ksp =" c" (Cu2+ ) c 2(OH - ) =" 2×10" -20。当溶液中各离子浓度计量数方次的乘积大于溶度积时,则产生沉淀。若某CuSO4溶液里c( Cu2+) ="0.02" mol·L-1,如果生成Cu(OH)2沉淀,应调整溶液pH,使pH大于 ; 要使0.2 mol·L-1的CuSO4溶液中Cu2+沉淀较为完全 ( 使Cu2+浓度降至原来的万分之一)则应向溶液里加NaOH溶液,使溶液pH等于 。
(5) 常温下,某纯碱(Na2CO3) 溶液中滴入酚酞,溶液呈红色。则该溶液呈 性。在分析该溶液遇酚酞呈红色原因时,甲同学认为是配制溶液所用的纯碱样品中混有NaOH 所致;乙同学认为是溶液中Na2CO3电离出的CO32-水解所致。请你设计一个简单的实验方案用来评判甲乙两位同学的观点是否正确(包括操作、现象和结论) 。
科目:gzhx 来源:2012-2013学年江苏省盐城市高三上学期学情调研考试化学试卷(解析版) 题型:选择题
下列有关实验原理、方法和结论都正确的是
A.向溶液X 中先滴加稀硝酸,再滴加Ba(NO3)2溶液,出现白色沉淀说明溶液X 中一定含有SO42-
B.取少量溶液X,向其中加入适量新制氨水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有Fe2+
C.粗略配制浓度为2 mol·L—1的NaCl溶液,可将58.5gNaCl加入到盛有500mL水的烧杯中,搅拌、溶解
D.对某固体进行焰色反应实验,火焰呈黄色,说明该物质为一定钠盐