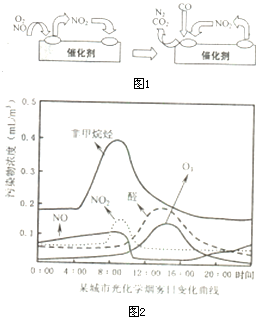
科目:gzhx 来源:通州市2006—2007学年(上)高三期中调研测试、化学试卷 题型:022
| |||||||||||||||||||||||
科目:gzhx 来源:江苏省南通市通州区2010届高三查漏补缺专项练习化学试题 题型:填空题
(10 分)SO2和NOx的排放是造成酸雨的两大罪魁祸首。下图表示了某地区在1940~2002年间,空气中SO2和NOx含量因燃料燃烧、工业生产、交通运输以及其他因素的影响而发生变化的基本统计数据。
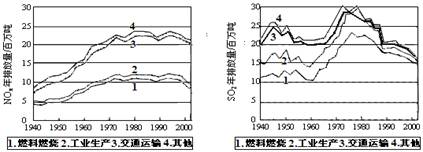
(1)结合上图数据,判断下列说法正确的是 ▲ 。
A.在交通运输中排放的NOx与燃料的不充分燃烧有关
B.在上世纪60年代以前,在交通运输中排放的SO2主要是使用燃煤的内燃机所致
C.近年来在工业生产中SO2排放量的下降,主要是减少了燃烧的煤的质量
D.随着汽车工业的发展,在形成酸雨的因素中,NOx所占比重在逐渐增大
(2)在上图表示的历史进程中,由工业生产所导致的SO2的排放量明显地在逐年减少。请用化学方程式说明人类在为解决SO2污染问题中所进行的一个反应过程:
▲ 。
(3)汽车排放的尾气中含有未燃烧充分的CmHn、以及N2、CO2、NO、CO等。有人设计利用反应2NO + 2CO  N2 + 2CO2 将有害的污染物转化为可参与大气循环的N2和CO2。
N2 + 2CO2 将有害的污染物转化为可参与大气循环的N2和CO2。
在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
|
时间/h |
0 |
1 |
2 |
3 |
4 |
5 |
|
c(NO)/mol·L-1 |
1.00×10-3 |
4.5×10-4 |
2.5×10-4 |
1.5×10-4 |
1.00×10-4 |
1.00×10-4 |
|
c(CO)/mol·L-1 |
3.6×10-3 |
3.05×10-3 |
2.85×10-3 |
2.75×10-3 |
2.70×10-3 |
2.70×10-3 |

 在上述条件下反应能够自发进行,则反应的
在上述条件下反应能够自发进行,则反应的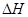 ▲ 0(“>”、“<”、“=”)。
▲ 0(“>”、“<”、“=”)。 在该温度下,反应的平衡常数K= ▲ 。
在该温度下,反应的平衡常数K= ▲ 。
(4)某次降雨过程收集到10L的雨水,向雨水中滴加1mL6mol/L的H2O2,充分反应后测得溶液的pH=3.62 [c(H+) =2.4×10-4 mol/L ]),再向溶液中加入足量的Ba(OH)2溶液,经过滤、晾干、称重,得沉淀的质量为0.1864g。若假设雨水的酸性仅由NOx和SO2的排放所致。请计算排放在空气中的NOx和SO2的物质的量之比接近于 ▲ 。
科目:gzhx 来源:江苏省南通市通州区2010届高三查漏补缺专项练习化学试题 题型:填空题
(10 分)SO2和NOx的排放是造成酸雨的两大罪魁祸首。下图表示了某地区在1940~2002年间,空气中SO2和NOx含量因燃料燃烧、工业生产、交通运输以及其他因素的影响而发生变化的基本统计数据。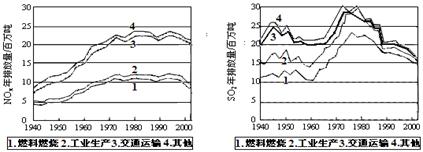
(1)结合上图数据,判断下列说法正确的是 ▲ 。
| A.在交通运输中排放的NOx与燃料的不充分燃烧有关 |
| B.在上世纪60年代以前,在交通运输中排放的SO2主要是使用燃煤的内燃机所致 |
| C.近年来在工业生产中SO2排放量的下降,主要是减少了燃烧的煤的质量 |
| D.随着汽车工业的发展,在形成酸雨的因素中,NOx所占比重在逐渐增大 |
 N2 + 2CO2将有害的污染物转化为可参与大气循环的N2和CO2。
N2 + 2CO2将有害的污染物转化为可参与大气循环的N2和CO2。| 时间/h | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol·L-1 | 1.00×10-3 | 4.5×10-4 | 2.5×10-4 | 1.5×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol·L-1 | 3.6×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |



 在上述条件下反应能够自发进行,则反应的
在上述条件下反应能够自发进行,则反应的 ▲ 0(“>”、“<”、“=”)。
▲ 0(“>”、“<”、“=”)。 在该温度下,反应的平衡常数K= ▲ 。
在该温度下,反应的平衡常数K= ▲ 。科目:gzhx 来源: 题型:阅读理解
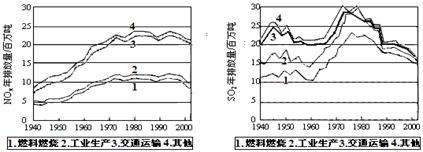
(10 分)SO2和NOx的排放是造成酸雨的两大罪魁祸首。下图表示了某地区在1940~2002年间,空气中SO2和NOx含量因燃料燃烧、工业生产、交通运输以及其他因素的影响而发生变化的基本统计数据。
(1)结合上图数据,判断下列说法正确的是 ▲ 。
A.在交通运输中排放的NOx与燃料的不充分燃烧有关
B.在上世纪60年代以前,在交通运输中排放的SO2主要是使用燃煤的内燃机所致
C.近年来在工业生产中SO2排放量的下降,主要是减少了燃烧的煤的质量
D.随着汽车工业的发展,在形成酸雨的因素中,NOx所占比重在逐渐增大
(2)在上图表示的历史进程中,由工业生产所导致的SO2的排放量明显地在逐年减少。请用化学方程式说明人类在为解决SO2污染问题中所进行的一个反应过程:
▲ 。
(3)汽车排放的尾气中含有未燃烧充分的CmHn、以及N2、CO2、NO、CO等。有人设计利用反应2NO + 2CO ![]() N2 + 2CO2 将有害的污染物转化为可参与大气循环的N2和CO2。
N2 + 2CO2 将有害的污染物转化为可参与大气循环的N2和CO2。
在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
| 时间/h | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol·L-1 | 1.00×10-3 | 4.5×10-4 | 2.5×10-4 | 1.5×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol·L-1 | 3.6×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
![]()
![]()
![]()
![]() 在上述条件下反应能够自发进行,则反应的
在上述条件下反应能够自发进行,则反应的![]() ▲ 0(“>”、“<”、“=”)。
▲ 0(“>”、“<”、“=”)。![]() 在该温度下,反应的平衡常数K= ▲ 。
在该温度下,反应的平衡常数K= ▲ 。
(4)某次降雨过程收集到10L的雨水,向雨水中滴加1mL6mol/L的H2O2,充分反应后测得溶液的pH=3.62 [c(H+) =2.4×10-4 mol/L ]),再向溶液中加入足量的Ba(OH)2溶液,经过滤、晾干、称重,得沉淀的质量为0.1864g。若假设雨水的酸性仅由NOx和SO2的排放所致。请计算排放在空气中的NOx和SO2的物质的量之比接近于 ▲ 。
科目:gzhx 来源: 题型:阅读理解
(10 分)SO2和NOx的排放是造成酸雨的两大罪魁祸首。下图表示了某地区在1940~2002年间,空气中SO2和NOx含量因燃料燃烧、工业生产、交通运输以及其他因素的影响而发生变化的基本统计数据。
(1)结合上图数据,判断下列说法正确的是 ▲ 。
A.在交通运输中排放的NOx与燃料的不充分燃烧有关
B.在上世纪60年代以前,在交通运输中排放的SO2主要是使用燃煤的内燃机所致
C.近年来在工业生产中SO2排放量的下降,主要是减少了燃烧的煤的质量
D.随着汽车工业的发展,在形成酸雨的因素中,NOx所占比重在逐渐增大
(2)在上图表示的历史进程中,由工业生产所导致的SO2的排放量明显地在逐年减少。请用化学方程式说明人类在为解决SO2污染问题中所进行的一个反应过程:
▲ 。
(3)汽车排放的尾气中含有未燃烧充分的CmHn、以及N2、CO2、NO、CO等。有人设计利用反应2NO + 2CO N2 + 2CO2 将有害的污染物转化为可参与大气循环的N2和CO2。
在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
| 时间/h | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol·L-1 | 1.00×10-3 | 4.5×10-4 | 2.5×10-4 | 1.5×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol·L-1 | 3.6×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
在上述条件下反应能够自发进行,则反应的![]() ▲ 0(“>”、“<”、“=”)。在该温度下,反应的平衡常数K= ▲ 。
▲ 0(“>”、“<”、“=”)。在该温度下,反应的平衡常数K= ▲ 。
(4)某次降雨过程收集到10L的雨水,向雨水中滴加1mL6mol/L的H2O2,充分反应后测得溶液的pH=3.62 [c(H+) =2.4×10-4 mol/L ]),再向溶液中加入足量的Ba(OH)2溶液,经过滤、晾干、称重,得沉淀的质量为0.1864g。若假设雨水的酸性仅由NOx和SO2的排放所致。请计算排放在空气中的NOx和SO2的物质的量之比接近于 ▲ 。
科目:gzhx 来源: 题型:阅读理解
(10 分)SO2和NOx的排放是造成酸雨的两大罪魁祸首。下图表示了某地区在1940~2002年间,空气中SO2和NOx含量因燃料燃烧、工业生产、交通运输以及其他因素的影响而发生变化的基本统计数据。

(1)结合上图数据,判断下列说法正确的是 ▲ 。
A.在交通运输中排放的NOx与燃料的不充分燃烧有关
B.在上世纪60年代以前,在交通运输中排放的SO2主要是使用燃煤的内燃机所致
C.近年来在工业生产中SO2排放量的下降,主要是减少了燃烧的煤的质量
D.随着汽车工业的发展,在形成酸雨的因素中,NOx所占比重在逐渐增大
(2)在上图表示的历史进程中,由工业生产所导致的SO2的排放量明显地在逐年减少。请用化学方程式说明人类在为解决SO2污染问题中所进行的一个反应过程:
▲ 。
(3)汽车排放的尾气中含有未燃烧充分的CmHn、以及N2、CO2、NO、CO等。有人设计利用反应2NO +2CO ![]() N2+ 2CO2 将有害的污染物转化为可参与大气循环的N2和CO2。
N2+ 2CO2 将有害的污染物转化为可参与大气循环的N2和CO2。
在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
| 时间/h | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol·L-1 | 1.00×10-3 | 4.5×10-4 | 2.5×10-4 | 1.5×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol·L-1 | 3.6×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
在上述条件下反应能够自发进行,则反应的![]() ▲ 0(“>”、“<”、“=”)。在该温度下,反应的平衡常数K= ▲ 。
▲ 0(“>”、“<”、“=”)。在该温度下,反应的平衡常数K= ▲ 。
(4)某次降雨过程收集到10L的雨水,向雨水中滴加1mL6mol/L的H2O2,充分反应后测得溶液的pH=3.62[c(H+) =2.4×10-4 mol/L ]),再向溶液中加入足量的Ba(OH)2溶液,经过滤、晾干、称重,得沉淀的质量为0.1864g。若假设雨水的酸性仅由NOx和SO2的排放所致。请计算排放在空气中的NOx和SO2的物质的量之比接近于 ▲ 。
科目:gzhx 来源:江苏省南通市通州区2010届高三下学期查漏补缺专题训练 题型:填空题
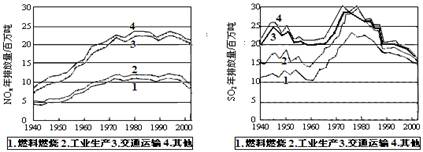
(10 分)SO2和NOx的排放是造成酸雨的两大罪魁祸首。下图表示了某地区在1940~2002年间,空气中SO2和NOx含量因燃料燃烧、工业生产、交通运输以及其他因素的影响而发生变化的基本统计数据。
(1)结合上图数据,判断下列说法正确的是 ▲ 。
A.在交通运输中排放的NOx与燃料的不充分燃烧有关
B.在上世纪60年代以前,在交通运输中排放的SO2主要是使用燃煤的内燃机所致
C.近年来在工业生产中SO2排放量的下降,主要是减少了燃烧的煤的质量
D.随着汽车工业的发展,在形成酸雨的因素中,NOx所占比重在逐渐增大
(2)在上图表示的历史进程中,由工业生产所导致的SO2的排放量明显地在逐年减少。请用化学方程式说明人类在为解决SO2污染问题中所进行的一个反应过程:
▲ 。
(3)汽车排放的尾气中含有未燃烧充分的CmHn、以及N2、CO2、NO、CO等。有人设计利用反应2NO +
2CO  N2
+ 2CO2 将有害的污染物转化为可参与大气循环的N2和CO2。
N2
+ 2CO2 将有害的污染物转化为可参与大气循环的N2和CO2。
在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
|
时间/h |
0 |
1 |
2 |
3 |
4 |
5 |
|
c(NO)/mol·L-1 |
1.00×10-3 |
4.5×10-4 |
2.5×10-4 |
1.5×10-4 |
1.00×10-4 |
1.00×10-4 |
|
c(CO)/mol·L-1 |
3.6×10-3 |
3.05×10-3 |
2.85×10-3 |
2.75×10-3 |
2.70×10-3 |
2.70×10-3 |
在上述条件下反应能够自发进行,则反应的 ▲ 0(“>”、“<”、“=”)。在该温度下,反应的平衡常数K= ▲ 。
▲ 0(“>”、“<”、“=”)。在该温度下,反应的平衡常数K= ▲ 。
(4)某次降雨过程收集到10L的雨水,向雨水中滴加1mL6mol/L的H2O2,充分反应后测得溶液的pH=3.62 [c(H+) =2.4×10-4 mol/L ]),再向溶液中加入足量的Ba(OH)2溶液,经过滤、晾干、称重,得沉淀的质量为0.1864g。若假设雨水的酸性仅由NOx和SO2的排放所致。请计算排放在空气中的NOx和SO2的物质的量之比接近于 ▲ 。
科目:gzhx 来源: 题型:阅读理解
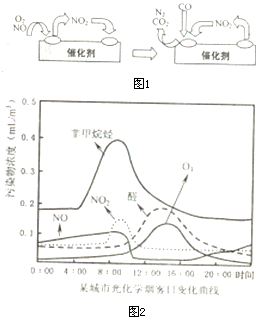
| 光 |
| ||
| ||
| ||
| ||
科目:gzhx 来源: 题型:阅读理解
| 时间/h | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol•L-1 | 1.00×10-3 | 4.5×10-4 | 2.5×10-4 | 1.5×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol•L-1 | 3.6×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
科目:gzhx 来源: 题型:阅读理解
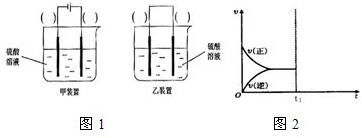
| 光 |
| Cu2O |
| 时间/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
科目:gzhx 来源:志鸿系列训练必修一化学鲁科版 题型:043
人类社会的发展、进步都离不开科学的发展与进步.让我们走进化学科学的殿堂,去了解在漫长的科学发展道路上,化学科学都作出了哪些贡献?现代化学科学的研究方法都有哪些?
科目:gzhx 来源:高一化学 第3章 有机化合物的获得与应用 3.1.1 天然气的利用 甲烷(苏教版必修2) 苏教版 题型:013
|
有机化合物与人类生活水平的提高和人类社会的发展密不可分.下列对有机化合物的认识正确的是 | |
| [ ] | |
A. |
有机化合物都是共价化合物 |
B. |
有机化合物都含有碳、氢元素 |
C. |
有机化合物都具有同分异构现象 |
D. |
有机物种类多是由碳原子的成键特征决定的 |
科目:gzhx 来源:高一化学 第三章 有机化合物 3.1.2 烷烃(人教版必修2) 题型:013
|
有机化合物与人类生活水平的提高和人类社会的发展密不可分.下列对有机化合物的认识正确的是 | |
| [ ] | |
A. |
有机化合物都是共价化合物 |
B. |
有机化合物都含有碳、氢元素 |
C. |
有机化合物都具有同分异构现象 |
D. |
有机物种类多是由碳原子的成键特征决定的 |
科目:gzhx 来源:同步题 题型:填空题
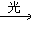 O+O2 ②NO+O3→NO2+O2 ③NO2+O→NO+O2
O+O2 ②NO+O3→NO2+O2 ③NO2+O→NO+O2 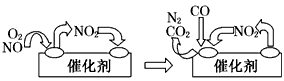
科目:gzhx 来源: 题型:阅读理解
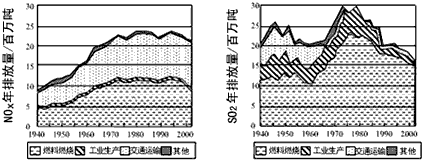
SO2和NOx的排放是造成酸雨的两大罪魁祸首。下图表示了某地区在1940~2002年间,空气中SO2和NOx含量因燃料燃烧、工业生产、交通运输以及其他因素的影响而发生变化的基本统计数据。
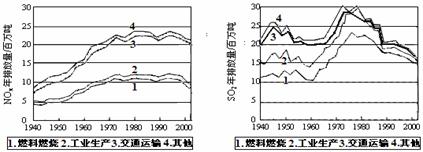
(1)结合上图数据,判断下列说法正确的是 ▲ 。
A.在交通运输中排放的NOx与燃料的不充分燃烧有关
B.在上世纪60年代以前,在交通运输中排放的SO2主要是使用燃煤的内燃机所致
C.近年来在工业生产中SO2排放量的下降,主要是减少了燃烧的煤的质量
D.随着汽车工业的发展,在形成酸雨的因素中,NOx所占比重在逐渐增大
(2)在上图表示的历史进程中,由工业生产所导致的SO2的排放量明显地在逐年减少。请用化学方程式说明人类在为解决SO2污染问题中所进行的一个反应过程:
▲ 。
(3)汽车排放的尾气中含有未燃烧充分的CmHn、以及N2、CO2、NO、CO等。有人设计利用反应2NO + 2CO ![]() N2 + 2CO2 将有害的污染物转化为可参与大气循环的N2和CO2。
N2 + 2CO2 将有害的污染物转化为可参与大气循环的N2和CO2。
在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
时间/h | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/mol·L-1 | 1.00×10-3 | 4.5×10-4 | 2.5×10-4 | 1.5×10-4 | 1.00×10-4 | 1.00×10-4 |
c(CO)/mol·L-1 | 3.6×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
在上述条件下反应能够自发进行,则反应的![]() ▲ 0(“>”、“<”、“=”)。在该温度下,反应的平衡常数K= ▲ 。
▲ 0(“>”、“<”、“=”)。在该温度下,反应的平衡常数K= ▲ 。
(4)某次降雨过程收集到10L的雨水,向雨水中滴加1mL6mol/L的H2O2,充分反应后测得溶液的pH=3.62 [c(H+) =2.4×10-4 mol/L ]),再向溶液中加入足量的Ba(OH)2溶液,经过滤、晾干、称重,得沉淀的质量为0.1864g。若假设雨水的酸性仅由NOx和SO2的排放所致。请计算排放在空气中的NOx和SO2的物质的量之比接近于 ▲ 。
科目:gzhx 来源:2010年山东省潍坊市四县市联考高考化学模拟试卷(解析版) 题型:解答题

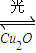 2H2(g)+O2(g)△H>0,不同时段产生O2的量见下表:
2H2(g)+O2(g)△H>0,不同时段产生O2的量见下表:| 时间/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
科目:gzhx 来源:诸城市模拟 题型:问答题
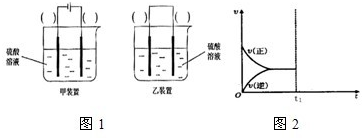
| 光 |
| Cu2O |
| 时间/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
科目:gzhx 来源:模拟题 题型:填空题
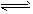 N2+2CO2将有害的污染物转化为可参与大气循环的N2和CO2。在某温度下用气体传感器测得不同时间的NO和CO浓度如下表
N2+2CO2将有害的污染物转化为可参与大气循环的N2和CO2。在某温度下用气体传感器测得不同时间的NO和CO浓度如下表
科目:gzhx 来源:2010年山东省潍坊市四县市联考高考化学模拟试卷(解析版) 题型:解答题

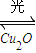 2H2(g)+O2(g)△H>0,不同时段产生O2的量见下表:
2H2(g)+O2(g)△H>0,不同时段产生O2的量见下表:| 时间/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
科目:gzhx 来源: 题型:解答题
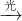 O+O2
O+O2