
科目:czhx 来源: 题型:阅读理解
节约资源和保护环境已经成为我们的基本国策。节能减排、环境保护和生态市建设是市政府近些年的工作重点。硫酸厂生产硫酸的流程是:把含硫矿物燃烧,生成二氧化硫,二氧化硫和氧气在高温和催化剂的作用生成三氧化硫,最后三氧化硫和水化合生成硫酸。写出三氧化硫和水化合生成硫酸的化学方程式
某纯碱样品中含有少量硫酸钠,现欲测定其碳酸钠的质量分数,利用含有少量硫酸的澄清废水进行如下实验:
《实验原理》Na2CO3+H2SO4= Na2SO4 + H2O + CO2↑通过实验测定反应产生的二氧化碳的质量,即可求得原样品中碳酸钠的质量,进而求得碳酸钠在样品中的质量分数。
《实验装置》

《实验步骤》
①如图连接装置(除B、C外)并加入所需药品。
②称量并记录B的质量(m1)。(称量时注意封闭B的两端。)
③按动鼓气球,持续鼓入空气约1分钟。
④连接上B、C。
⑤打开分液漏斗F的活塞,将稀硫酸快速加入D中后,关闭活塞。
⑥按动鼓气球,持续约1分钟。
⑦称量并记录B的质量(m2)。(称量时注意封闭B的两端及E右端的出口。)
⑧计算。
⑴已知碱石灰的主要成分是氢氧化钙和氢氧化钠,则干燥管A的作用是: ,以免使测定结果偏大。
(2) (能或不能)用稀盐酸代替稀硫酸,因为盐酸具有 性,会使测得碳酸钠的质量分数 (填偏大、偏小或不变,下同);若去除干燥管C,则测得碳酸钠的质量分数将会
(3)E装置的作用是
(4)本实验能否省略③、⑥两个步骤? (填能或不能),原因分别是 、
(5)若所取样品的质量为6g,分液漏斗F中盛放5%只含硫酸一种溶质的澄清废水,称得m1为51.20g,m2为53.40g,(计算结果保留两位小数)
求:(1)样品中碳酸钠的质量分数为多少?
(2)D装置中正好反应后,所得溶液的溶质质量分数是多少?
科目:czhx 来源: 题型:阅读理解
节约资源和保护环境已经成为我们的基本国策。节能减排、环境保护和生态市建设是市政府近些年的工作重点。硫酸厂生产硫酸的流程是:把含硫矿物燃烧,生成二氧化硫,二氧化硫和氧气在高温和催化剂的作用生成三氧化硫,最后三氧化硫和水化合生成硫酸。写出三氧化硫和水化合生成硫酸的化学方程式
某纯碱样品中含有少量硫酸钠,现欲测定其碳酸钠的质量分数,利用含有少量硫酸的澄清废水进行如下实验:
《实验原理》Na2CO3+H2SO4= Na2SO4 + H2O + CO2↑通过实验测定反应产生的二氧化碳的质量,即可求得原样品中碳酸钠的质量,进而求得碳酸钠在样品中的质量分数。
《实验装置》
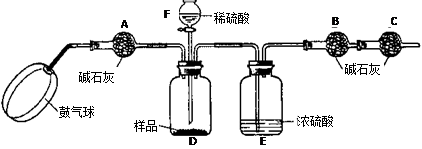
《实验步骤》
①如图连接装置(除B、C外)并加入所需药品。
②称量并记录B的质量(m1)。(称量时注意封闭B的两端。)
③按动鼓气球,持续鼓入空气约1分钟。
④连接上B、C。
⑤打开分液漏斗F的活塞,将稀硫酸快速加入D中后,关闭活塞。
⑥按动鼓气球,持续约1分钟。
⑦称量并记录B的质量(m2)。(称量时注意封闭B的两端及E右端的出口。)
⑧计算。
⑴已知碱石灰的主要成分是氢氧化钙和氢氧化钠,则干燥管A的作用是: ,以免使测定结果偏大。
(2) (能或不能)用稀盐酸代替稀硫酸,因为盐酸具有 性,会使测得碳酸钠的质量分数 (填偏大、偏小或不变,下同);若去除干燥管C,则测得碳酸钠的质量分数将会
(3)E装置的作用是
(4)本实验能否省略③、⑥两个步骤? (填能或不能),原因分别是 、
(5)若所取样品的质量为6g,分液漏斗F中盛放5%只含硫酸一种溶质的澄清废水,称得m1为51.20g,m2为53.40g,(计算结果保留两位小数)
求:(1)样品中碳酸钠的质量分数为多少?
(2)D装置中正好反应后,所得溶液的溶质质量分数是多少?
科目:czhx 来源: 题型:阅读理解
科目:czhx 来源:2012届江苏省镇江市实验初中九年级第二学期第一次素质调研化学试卷(带解析) 题型:计算题
节约资源和保护环境已经成为我们的基本国策。节能减排、环境保护和生态市建设是市政府近些年的工作重点。硫酸厂生产硫酸的流程是:把含硫矿物燃烧,生成二氧化硫,二氧化硫和氧气在高温和催化剂的作用生成三氧化硫,最后三氧化硫和水化合生成硫酸。写出三氧化硫和水化合生成硫酸的化学方程式
某纯碱样品中含有少量硫酸钠,现欲测定其碳酸钠的质量分数,利用含有少量硫酸的澄清废水进行如下实验:
《实验原理》Na2CO3+H2SO4 = Na2SO4 + H2O + CO2↑通过实验测定反应产生的二氧化碳的质量,即可求得原样品中碳酸钠的质量,进而求得碳酸钠在样品中的质量分数。
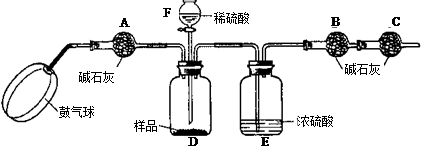
《实验装置》
《实验步骤》
①如图连接装置(除B、C外)并加入所需药品。
②称量并记录B的质量(m1)。(称量时注意封闭B的两端。)
③按动鼓气球,持续鼓入空气约1分钟。
④连接上B、C。
⑤打开分液漏斗F的活塞,将稀硫酸快速加入D中后,关闭活塞。
⑥按动鼓气球,持续约1分钟。
⑦称量并记录B的质量(m2)。(称量时注意封闭B的两端及E右端的出口。)
⑧计算。
⑴已知碱石灰的主要成分是氢氧化钙和氢氧化钠,则干燥管A的作用是: ,以免使测定结果偏大。
(2) (能或不能)用稀盐酸代替稀硫酸,因为盐酸具有 性,会使测得碳酸钠的质量分数 (填偏大、偏小或不变,下同);若去除干燥管C,则测得碳酸钠的质量分数将会
(3)E装置的作用是
(4)本实验能否省略③、⑥两个步骤? (填能或不能),原因分别是 、
(5)若所取样品的质量为6g,分液漏斗F中盛放5%只含硫酸一种溶质的澄清废水,称得m1为51.20g,m2为53.40g,(计算结果保留两位小数)
求:(1)样品中碳酸钠的质量分数为多少?
(2)D装置中正好反应后,所得溶液的溶质质量分数是多少?
科目:czhx 来源:2011-2012学年江苏省镇江市九年级第二学期第一次素质调研化学试卷(解析版) 题型:计算题
节约资源和保护环境已经成为我们的基本国策。节能减排、环境保护和生态市建设是市政府近些年的工作重点。硫酸厂生产硫酸的流程是:把含硫矿物燃烧,生成二氧化硫,二氧化硫和氧气在高温和催化剂的作用生成三氧化硫,最后三氧化硫和水化合生成硫酸。写出三氧化硫和水化合生成硫酸的化学方程式
某纯碱样品中含有少量硫酸钠,现欲测定其碳酸钠的质量分数,利用含有少量硫酸的澄清废水进行如下实验:
《实验原理》Na2CO3+H2SO4 = Na2SO4 + H2O + CO2↑通过实验测定反应产生的二氧化碳的质量,即可求得原样品中碳酸钠的质量,进而求得碳酸钠在样品中的质量分数。
《实验装置》
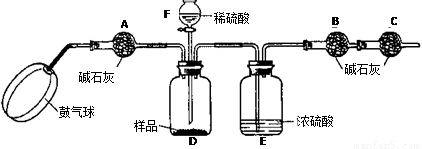
《实验步骤》
①如图连接装置(除B、C外)并加入所需药品。
②称量并记录B的质量(m1)。(称量时注意封闭B的两端。)
③按动鼓气球,持续鼓入空气约1分钟。
④连接上B、C。
⑤打开分液漏斗F的活塞,将稀硫酸快速加入D中后,关闭活塞。
⑥按动鼓气球,持续约1分钟。
⑦称量并记录B的质量(m2)。(称量时注意封闭B的两端及E右端的出口。)
⑧计算。
⑴已知碱石灰的主要成分是氢氧化钙和氢氧化钠,则干燥管A的作用是: ,以免使测定结果偏大。
(2) (能或不能)用稀盐酸代替稀硫酸,因为盐酸具有 性,会使测得碳酸钠的质量分数 (填偏大、偏小或不变,下同);若去除干燥管C,则测得碳酸钠的质量分数将会
(3)E装置的作用是
(4)本实验能否省略③、⑥两个步骤? (填能或不能),原因分别是 、
(5)若所取样品的质量为6g,分液漏斗F中盛放5%只含硫酸一种溶质的澄清废水,称得m1为51.20g,m2为53.40g,(计算结果保留两位小数)
求:(1)样品中碳酸钠的质量分数为多少?
(2)D装置中正好反应后,所得溶液的溶质质量分数是多少?
科目:czhx 来源:2011-2012学年广西南宁三中中考模拟测试化学试卷(八) 题型:计算题
节约资源和保护环境已经成为我们的基本国策。节能减排、环境保护和生态市建设是市政府近些年的工作重点。硫酸厂生产硫酸的流程是:把含硫矿物燃烧,生成二氧化硫,二氧化硫和氧气在高温和催化剂的作用生成三氧化硫,最后三氧化硫和水化合生成硫酸。写出三氧化硫和水化合生成硫酸的化学方程式
某纯碱样品中含有少量硫酸钠,现欲测定其碳酸钠的质量分数,利用含有少量硫酸的澄清废水进行如下实验:
《实验原理》Na2CO3+H2SO4 = Na2SO4 + H2O + CO2↑通过实验测定反应产生的二氧化碳的质量,即可求得原样品中碳酸钠的质量,进而求得碳酸钠在样品中的质量分数。
《实验装置》
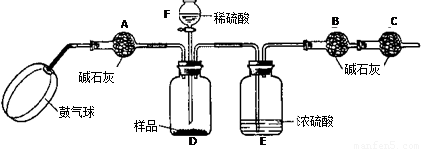
《实验步骤》
①如图连接装置(除B、C外)并加入所需药品。
②称量并记录B的质量(m1)。(称量时注意封闭B的两端。)
③按动鼓气球,持续鼓入空气约1分钟。
④连接上B、C。
⑤打开分液漏斗F的活塞,将稀硫酸快速加入D中后,关闭活塞。
⑥按动鼓气球,持续约1分钟。
⑦称量并记录B的质量(m2)。(称量时注意封闭B的两端及E右端的出口。)
⑧计算。
⑴已知碱石灰的主要成分是氢氧化钙和氢氧化钠,则干燥管A的作用是: ,以免使测定结果偏大。
(2) (能或不能)用稀盐酸代替稀硫酸,因为盐酸具有 性,会使测得碳酸钠的质量分数 (填偏大、偏小或不变,下同);若去除干燥管C,则测得碳酸钠的质量分数将会
(3)E装置的作用是
(4)本实验能否省略③、⑥两个步骤? (填能或不能),原因分别是 、
(5)若所取样品的质量为6g,分液漏斗F中盛放5%只含硫酸一种溶质的澄清废水,称得m1为51.20g,m2为53.40g,(计算结果保留两位小数)
求:(1)样品中碳酸钠的质量分数为多少?
(2)D装置中正好反应后,所得溶液的溶质质量分数是多少?
科目:czhx 来源: 题型:解答题
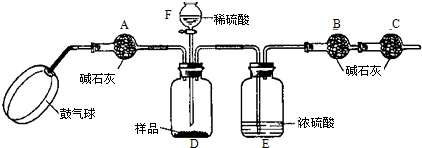
科目:czhx 来源:2011-2012学年江苏省镇江市丹阳市实验初中九年级(下)第一次素质调研化学试卷(解析版) 题型:解答题
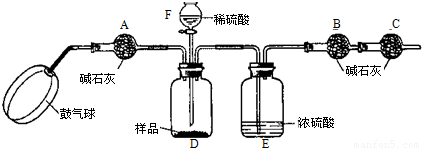
科目:czhx 来源:不详 题型:计算题

科目:czhx 来源: 题型:阅读理解
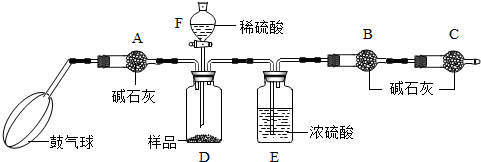
科目:czhx 来源: 题型:阅读理解

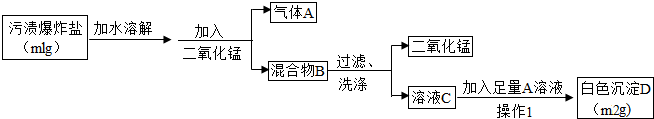
| ||
科目:czhx 来源: 题型:


| 实验操作 | 实验现象 | 实验结论 |
| 氧化钙已经变质 |
科目:czhx 来源: 题型:解答题
科目:czhx 来源: 题型:
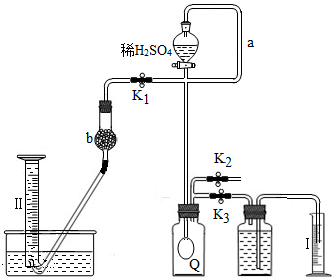
已知某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验.

主要实验步骤如下:
①按图组装仪器,并检查装置的气密性
②将ag试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液
③称量盛有碱石灰的U型管的质量,得到bg
④从分液漏斗滴入稀硫酸,直到不再产生气体时为止

⑤从导管A处缓缓鼓入一定量的空气
⑥再次称量盛有碱石灰的U型管的质量,得到cg
⑦重复步骤 ⑤和⑥的操作,直到U型管的质量基本不变,为dg
⑤和⑥的操作,直到U型管的质量基本不变,为dg
请填空和回答问题:
(1)在用托盘天平称量样品时,如果天平的指针 向左偏转,说明
向左偏转,说明
.
(2)已知碱石灰的主要成分是氧化钙和氢氧化钠,则装置中干燥管B的作
用是 .
(3)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果
(填偏高、偏低或不变).
(4)步骤⑤的目的是 
(5)步骤⑦的目的是
(6)该试样中纯碱的质量分数的计算式为 

科目:czhx 来源: 题型:
科目:czhx 来源:2012届江苏省丹阳市司徒中学九年级下学期第一次质量检测化学试卷(带解析) 题型:计算题
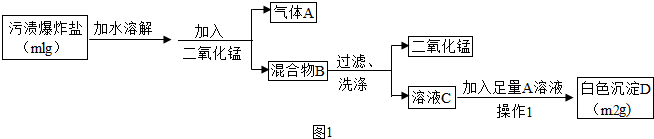
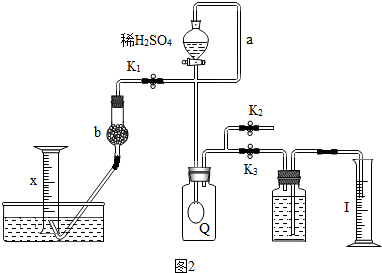
(9分)某纯碱样品中含有少量氯化钠,现欲测定其中碳酸钠的质量分数,进行如下实验:
《实验原理》:Na2CO3+H2SO4=Na2SO4 + H2O +CO2↑;通过实验测定反应产生的二氧化碳的质量,即可求得原样品中碳酸钠的质量,进而求得碳酸钠在样品中的质量分数。
《实验装置》:如图所示。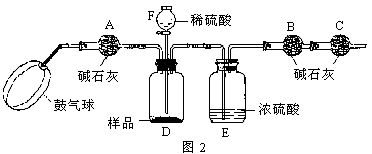
《实验步骤》:①如图连接装置(除B、C外)并加入所需药品。②称量并记录B的质量(m1) (称量时注意封闭B的两端) 。③按动鼓气球,持续约1分钟。④连接上B、C。⑤打开分液漏斗F的活塞,将稀硫酸快速加入D中后,关闭活塞。⑥按动鼓气球,持续约1分钟。⑦称量并记录B的质量(m2)。(称量时注意封闭B的两端及E右端的出口。)⑧计算。请回答:
(1)已知碱石灰的主要成分是氢氧化钙和氢氧化钠,则干燥管A的作用是 ,干燥管C的作用是 ,E装置的作用是 。步骤③中鼓气的目的是 ;步骤⑥中鼓气的目的是 ;本实验能否同时省略③、⑥两个步骤? ,原因是 。
(2)若所取样品的质量为5g,为确保实验顺利进行,分液漏斗F中至少要盛放10%的稀硫酸(密度为1.07g/mL) /mL,若m1为51.20 g ,m2为53.18g ,样品中碳酸钠的质量分数为 。
科目:czhx 来源:不详 题型:计算题
科目:czhx 来源: 题型:

科目:czhx 来源: 题型:探究题
(12分)油条是人们喜欢的早点,中国油条的传统加工配方是用明矾(KAl(SO4)2)作为膨松剂,明矾常引起铝残留影响人体健康问题,现在的膨松剂常用臭粉(碳酸氢铵)、小苏打。
(1)油条中的主要营养素是油脂和
(2)“铝残留影响人体健康”中的铝是指 (选填“原子”或“元素”或“单质”)
(3)已知某膨松剂含碳酸氢铵、碳酸氢钠中的一种或两种,兴趣小组对该膨松剂进行如下探究:
【查阅资料】① 2NaHCO3 Na2CO3+H2O+CO2↑; NH4HCO3
Na2CO3+H2O+CO2↑; NH4HCO3  NH3↑+H2O+CO2↑。
NH3↑+H2O+CO2↑。
②氨气能使湿润的红色石蕊试纸变蓝。浓硫酸可用于吸收氨气。
③ 碱石灰是固体氢氧化钠和氧化钙的混合物,能作干燥剂,和二氧化碳反应,不与氨气反应。
实验I:探究膨松剂的成分
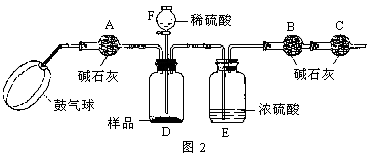
按下图所示连接好装置。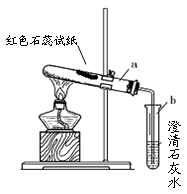
实验记录
| 实验操作 | 主要实验现象 | 实验结论 及解释 | |
| ① | 检查装置的气密性 | | 装置的气密性良好 |
| ② | 点燃酒精灯。 | 试管中白色固体减少,红色石蕊试纸 ,澄清石灰水变浑浊。 | 有二氧化碳和氨气生成 |
| ③ | 继续充分 加热 | 试管中仍有固体。 | |
科目:czhx 来源:2013-2014江苏盐城市盐都区九年级中考第二次调研考试化学试卷(解析版) 题型:探究题
(12分)油条是人们喜欢的早点,中国油条的传统加工配方是用明矾(KAl(SO4)2)作为膨松剂,明矾常引起铝残留影响人体健康问题,现在的膨松剂常用臭粉(碳酸氢铵)、小苏打。
(1)油条中的主要营养素是油脂和
(2)“铝残留影响人体健康”中的铝是指 (选填“原子”或“元素”或“单质”)
(3)已知某膨松剂含碳酸氢铵、碳酸氢钠中的一种或两种,兴趣小组对该膨松剂进行如下探究:
【查阅资料】① 2NaHCO3 Na2CO3+H2O+CO2↑; NH4HCO3
Na2CO3+H2O+CO2↑; NH4HCO3  NH3↑+H2O+CO2↑。
NH3↑+H2O+CO2↑。
②氨气能使湿润的红色石蕊试纸变蓝。浓硫酸可用于吸收氨气。
③ 碱石灰是固体氢氧化钠和氧化钙的混合物,能作干燥剂,和二氧化碳反应,不与氨气反应。
实验I:探究膨松剂的成分
按下图所示连接好装置。

实验记录
实验操作 | 主要实验现象 | 实验结论 及解释 | |
① | 检查装置的气密性 |
| 装置的气密性良好 |
② | 点燃酒精灯。 | 试管中白色固体减少,红色石蕊试纸 ,澄清石灰水变浑浊。 | 有二氧化碳和氨气生成 |
③ | 继续充分 加热 | 试管中仍有固体。 |
|
得出结论:该膨松剂的成分为 (写出化学式)。
实验II:探究产生气体的量
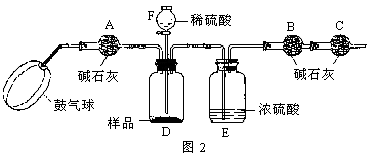
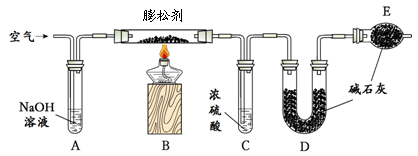
①测定二氧化碳的质量:如下图所示装置(气密性良好,各装置中的试剂为足量)。

将8g膨松剂装入装置B中,加热前,先对已连接好的装置A、B和C通一段时间的空气,再连接装置D、E;加热过程中,装置C的作用是 ;停止加热后,继续通入一段时间的空气,目的是 。实验中,测定实验前后装置 (填字母序号)的质量,其质量差即为样品产生的二氧化碳气体的质量。若没有装置A,可能会造成测定结果 (填“偏大”、“不变”或“偏小”)。
②测定氨气的质量:将上图装置中 (填字母序号) 的连接顺序为对调。另取8g膨松剂装入装置B中,通过测定实验前后盛有浓硫酸的试管质量,其质量差即为样品产生的氨气的质量。若该装置的质量增加了1.36g,则同时共产生二氧化碳质量是多少? (有计算过程,结果精确到0.01)