
科目:gzhx 来源:2016届浙江省高三5月高考模拟理综化学试卷(解析版) 题型:填空题
Ⅰ、次氯酸钠是一种被广泛应用的消毒剂,请回答下列问题:
(1)写出NaClO的电子式___________________。
(2)已知HClO的电离能力介于H2CO3一级与二级电离之间,写出NaClO溶液中通入少量CO2过程中发生的离子反应方程式为________________________
(3)在NaClO溶液中通入少量SO2,其反应离子方程式:________________________
II、某二元化合物X其相对分子质量小于100,常温下为黄绿色或橘黄色气体,性质非常不稳定,若用“惰性气体”等稀释时,爆炸性 则大大降低,X的水溶液质量分数高于30%也有可能引起爆炸。X可由KClO3和草酸(H2C2O4)混合物中加入足量的稀硫酸水浴加热制得,12.25 g KClO3与9 g草酸恰好完全反应生成X、CO2和一种酸式盐。
(1)确定X的化学式_______________
(2)用H2C2O4溶液、稀硫酸和KC1O3制备X最大优点是 ______________
(3)工业废水中Mn2+常用X处理,将Mn2+转化为MnO2,写出X除去Mn2+的离子方程式 _____________
(4)纤维素还原法制X是一种新方法,其原理是:纤维素水解得到的最终产物与稀硫酸、NaClO3反应生成X。完成反应的化学方程式:_____________
(5)实验室用氢氧化钠溶液吸收X尾气,生成等物质的两种钠盐,其中有一种盐为NaClO3完成氢氧化钠溶液吸收X尾气反应的化学方程式:_____________
(6)X和Cl2均能将电镀废水中的CN-氧化为无毒的物质。处理含CN-相同量的电镀废水,所需Cl2的物质的量是X的_______倍
科目:gzhx 来源: 题型:

| m(Cl2) |
| m(次氯酸盐) |
科目:gzhx 来源: 题型:
碱式次氯酸镁[BMH化学式为Mg2ClO(OH)3•H2O]难溶于水,相对稳定,是一种有开发价值的无机抗菌剂.某研发小组通过下列流程制备碱式次氯酸镁:
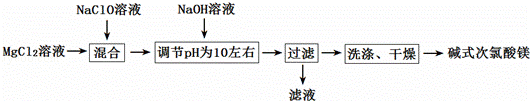
(1)在上述流程中,“过滤”操作用到的硅酸盐材质的仪器有
(2)NaClO的电子式为 ,NaClO溶液可用Cl2与NaOH溶液反应获得,写出该反应的离子方程式
(3)有效氯的含量是衡量次氯酸盐氧化能力的重要指标.次氯酸盐的有效氯含量可用次氯酸盐与盐酸反应所生成的氯气的含量来表示,则生成氯气的离子方程式为
(4)就抗菌和杀菌效果而言,氯制剂具有广谱、高效的特点,像BMH这样难溶又稳定的氯制剂几乎别无他物.在酸性溶液中BMH具有杀菌、漂白作用的原因是 (用离子方程式表示)
(5)在混合溶液中加入NaOH溶液并调节pH在10左右,即生成BMH,其化学方程式为 .
科目:gzhx 来源: 题型:实验题
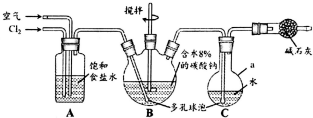 次氯酸(HClO)仅存在于溶液中,有很强的氧化性和漂白作用.某兴趣小组拟用Cl2O与潮湿Na2CO3反应制得Cl2O,再用水吸收Cl2O制备次氯酸溶液,并测定其浓度.
次氯酸(HClO)仅存在于溶液中,有很强的氧化性和漂白作用.某兴趣小组拟用Cl2O与潮湿Na2CO3反应制得Cl2O,再用水吸收Cl2O制备次氯酸溶液,并测定其浓度.科目:gzhx 来源: 题型:解答题

科目:gzhx 来源:0112 同步题 题型:实验题
科目:gzhx 来源: 题型:

| 优 点 | 缺 点 | |
| 甲装置 | ||
| 乙装置 |
科目:gzhx 来源: 题型:
(12分)回答有关氯气制备的几个问题
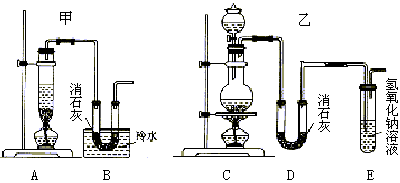
实验室用浓盐酸、二氧化锰共热制氯气,并用氯气和Ca(OH)2制取少量漂白粉。现已知反应:2Cl2+2Ca(OH)2 Ca(ClO)2+CaCl2+2H2O,该反应是放热反应,温度稍高即发生副反应:6Cl2+6Ca(OH)2 Ca(ClO3)2+5CaCl2+6H2O。现有两个同学分别设计的两套实验装置如下图:
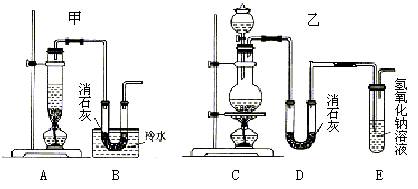
(1)写出制取氯气的化学方程式 。
(2)请从以下几个方面对甲乙两套实验装置的优缺点作出评价,并将符合题目要求的
选项的序号填在表格中。
a.不容易控制反应速率;b.容易控制反应速率;c.有副反应发生;d.可防止副反应发生;e.污染环境;f.可防止污染环境。
| 优 点 | 缺 点 |
甲装置 |
|
|
乙装置 |
|
|
(3)上述装置中甲由A、B两部分组成,乙由C、D、E三部分组成,请从上述装置中选取合理的部分,组装一套较完整的实验装置,装置各部分连接顺序是 (按气流流动的方向) 。该组合中还缺少的装置是 ,原因是 。
(4)实验室若用16mol/L的盐酸100mL与足量的二氧化锰反应,理论上最终生成的次氯酸钙的物质的量最多不超过 mol。
科目:czhx 来源: 题型:
科目:czhx 来源: 题型:
科目:czhx 来源: 题型:解答题
科目:czhx 来源:不详 题型:问答题
科目:czhx 来源:2011-2012学年北京市东城区九年级(上)期末化学试卷(解析版) 题型:解答题
科目:czhx 来源: 题型:
家用消毒液有效成分是次氯酸钠(NaClO),其制备反应的化学方程式是:
Cl2+2NaOH == NaCl+NaClO+H2O。计算7.1g氯气(Cl2)理论上可以制得次氯酸钠的质量。
科目:czhx 来源: 题型:
科目:gzhx 来源: 题型:
科目:gzhx 来源: 题型:实验题
科目:czhx 来源: 题型:解答题
科目:czhx 来源: 题型:
(3分)家用消毒液有效成分是次氯酸钠(NaClO),其制备反应的化学方程式是:
Cl2+2NaOH == NaCl+NaClO+H2O。计算7.1g氯气(Cl2)理论上可以制得次氯酸钠的质量。
科目:czhx 来源: 题型: