
科目:czwl 来源:新课标 1+1轻巧夺冠·优化训练(人教版)银版 九年级物理 (人教版)银版 题型:022
气体和液体相比较,相同点是________;不同点是________.
科目:czhx 来源: 题型:

科目:czhx 来源: 题型:解答题
 为比较相同浓度的FeCl3溶液和CuSO4溶液对H2O2分解的催化效果,某研究小组进行了如下探究:
为比较相同浓度的FeCl3溶液和CuSO4溶液对H2O2分解的催化效果,某研究小组进行了如下探究:科目:czhx 来源: 题型:实验探究题
 为比较相同浓度的FeCl3溶液和CuSO4溶液对H2O2分解的催化效果,某研究小组进行了如下探究:
为比较相同浓度的FeCl3溶液和CuSO4溶液对H2O2分解的催化效果,某研究小组进行了如下探究:科目:czhx 来源:学习周报 化学 人教课标中考版 2009-2010学年 第17期 总173期 人教课标中考版 题型:058
某活动小组同学用加热草酸晶体制得的CO(H2C2O4·2H2O![]() CO↑+CO2↑+3H2O),做炼铁原理实验并进行尾气处理,设计了以下装置(如图甲和图乙所示).
CO↑+CO2↑+3H2O),做炼铁原理实验并进行尾气处理,设计了以下装置(如图甲和图乙所示).
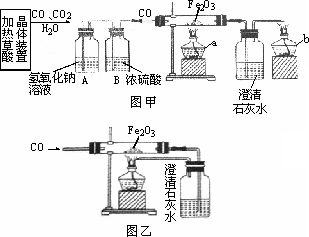
回答下列有关问题:
(1)在加热分解草酸晶体的装置中,有下列仪器供选择使用:①试管、②烧杯、③酒精灯、④蒸发皿、⑤铁架台(含铁夹)、⑥带导管的橡皮塞、⑦集气瓶
其中需要用到的仪器有________(填序号).
(2)硬质玻璃管中发生反应的化学方程式为________.
(3)选择图甲处理尾气,实验时应先点燃________(填“a”或“b”)处的酒精灯.图乙与图甲所示的尾气处理方法相比较,其主要优点是________.
(4)活动小组的同学通过查阅资料得知:常温下,CO能与氯化钯溶液(PdCl2)反应.于是他们选择了将尾气直接通入氯化钯溶液中进行处理.该反应的化学方程式为:CO+PdCl2+H2O![]() Pd↓+CO2+2R,其中R的化学式为________.此法与上述方法相比除了具有图乙比图甲所示方法的优点外,从实验角度看,它还有的优点是________(写出一条合理答案即可).
Pd↓+CO2+2R,其中R的化学式为________.此法与上述方法相比除了具有图乙比图甲所示方法的优点外,从实验角度看,它还有的优点是________(写出一条合理答案即可).
科目:czhx 来源:2016届江西省宜春市九年级上学期期末化学试卷(解析版) 题型:计算题
某活动小组同学用加热草酸晶体制得的CO
已知(H2C2O4•2H2O=CO↑+CO2↑3H2O),做炼铁原理实验丙进行尾气处理,设计以下装置(图甲图乙)

回答下列问题:
(1)在加热分解草酸晶体的装置中,有下列仪器供选择使用:
①试管②烧杯③酒精灯④蒸发皿⑤铁架台(含铁夹)⑥带导管的橡皮塞⑦集气瓶
其中需要用到的仪器有 (填序号)
(2)为了获得干燥纯净的CO,A、B两装置中应分别存放 、 .
(3)硬质玻璃管中发生反应的化学方程式 .
(4)选择图甲处理尾气,实验时应先点燃 (填“a”或“b”)处的酒精灯,图乙与图甲所示的尾气处理方法相比较,其主要优点是 .
(5)活动小组的同学通过查阅资料得知:常温下,CO能与氯化钯PdCl2溶液反应,于是他们选择了将尾气直接通入氯化钯溶液中进行处理,该反应的化学方程式为:CO+PdCl2+H2O=Pd↓+CO2+2R,其中R的化学式为 ,此法与上述方法相比除了具有图乙比图甲所示方法的优点外,从实验角度看它还有的优点是 (写出一条合理答案即可).
【答案】(1)①③⑤⑥;
(2)NaOH溶液,浓H2SO4;
(3)3CO+Fe2O3 2Fe+3CO2;
2Fe+3CO2;
(4)b;节约能源;
(5)HCl,安全、操作简单易行.
【解析】(1)要加热草酸晶体需要有支撑加热的装置,需要有盛放草酸的装置,需要加热装置,需要导气装置,故答案为:①③⑤⑥;
(2)加热后会生成水和二氧化碳、一氧化碳,需要将二氧化碳和水除去,除去水用浓硫酸,除去二氧化碳用氢氧化钠,水要放在后面除去,故答案为:NaOH溶液,浓H2SO4;
(3)一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,故方程式为:3CO+Fe2O3 2Fe+3CO2;
2Fe+3CO2;
(4)一氧化碳具有可燃性,如果先点燃a处的酒精灯,一氧化碳和氧气的混合气在受热时会发生爆炸,故答案为:b;图乙中的一氧化碳又得到了利用,经过点燃来提供热量,故答案为:节约能源;
(5)根据质量守恒定律可知,反应前后的元素种类和原子个数不变,故答案为:HCl,
该操作不需要图甲、图乙中的太多装置,也不需要点燃,避免了爆炸的危险,故答案为:安全、操作简单易行.
【点评】本题主要考查了常见气体的检验和除杂的方法,以及对实验操作的正确的评估.
【题型】填空题
【适用】较难
【标题】2016届江西省宜春市上高二中九年级上学期期末化学试卷(带解析)
【关键字标签】
【结束】
将20g含杂质(杂质不溶于水,也不溶于酸)的锌样品,与一定质量的稀硫酸恰好完全反应,所得溶液质量80.5g,同时生成氢气0.4g,试计算:
(1)样品中锌的质量为: g.
(2)完全反应后所得溶液中溶质的质量分数(写出计算过程).
科目:gzsw 来源: 题型:阅读理解
I、人们对光和作用的认识经历了漫长的历程,请阅读绿色植物光合作用发现历程,回答相关问题。
(1)2400多年前古希腊学者亚里士多德提出:植物体是由“土壤汁”构成的。此后,没有人对他的观点提出质疑。1642年,比利时的赫尔蒙特才首次对亚里士多德的观点提出了质疑。他将柳树和干土分别称重→栽种在密封桶内,只浇水→五年后→柳树增重74.47kg,而土壤只损失0.06kg.赫尔蒙特由此实验得出建造植物体的原料是水,但赫尔蒙特得出这样的结论忽视了 对实验的影响。
(2)随着认知水平的提高,1771年英国化学家普里斯特里进行了这样的探究:他将一支 点燃的蜡烛和一只小鼠分别放在密闭的钟罩里,不久蜡烛熄灭了,小鼠也很快死亡了;他又将绿色植物、点燃的蜡烛与小鼠一起放置在密闭的钟罩中——蜡烛不容易 熄灭,小鼠也不容易窒息死亡。普里斯特里实验结论是绿色植物能够 。
(3)1779年英格豪斯将普里斯特里实验在光下与无光下对照,证明植物更新空气离开 光照。1864年萨克斯进行了如下研究“紫苏——暗处理——部分叶片遮光——光照 一段时间——脱色后加碘液——观察实验现象”。结果证明绿叶在光下制造了淀 粉。萨克斯实验中对紫苏暗处理,是为了耗尽植物体内原有的 ;若不进行暗处理,实验时用碘液处理后遮光和不遮光部分均会 。
(4)1880年恩格尔曼水绵细胞实验证明光合作用的场所是叶绿体,至此人们才认识了光 合作用的原料、条件、产物。但光合作用中产生的O:中的氧原子究竟来是来自于参加光合作用的CO2还是H2O仍无法确定。鲁宾和卡门采用同位素示踪技术进行实 验:用18O标记水和二氧化碳,向绿色植物提供H218O和CO2,放在光下让其进行光合作用,检测产生的氧气均为18O。
从这组实验能否证明光合作用中释放的O2中的氧全部来自于参加光合作用的 H2O?——;如果不能应该如何改进? 。
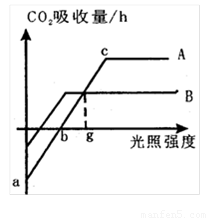
Ⅱ、光合作用原理在农业生产中有着广泛应用,下图是北方地区A、B两种植物光合速率随光照强度改变的变化曲线,请分析回答:
 (1)在较长时间连续阴雨的环境中,生长受到
(1)在较长时间连续阴雨的环境中,生长受到
显著影响的植物是 。
(2)图中的“a”点表示植物的 速率。
如果以缺镁的全营养液培养A植物幼苗,
则b点的移动方向是向 。
(3)c点与b点相比较,c点时叶肉细胞中C3的
含量 (填“高”“低”或“基本一致”)
科目:gzhx 来源: 题型:单选题
科目:gzsw 来源:陕西省宝鸡市2010年高三教学质量检测(理综生物) 题型:综合题
(10分)I、人们对光和作用的认识经历了漫长的历程,请阅读绿色植物光合作用发现历程,回答相关问题。
(1)2400多年前古希腊学者亚里士多德提出:植物体是由“土壤汁”构成的。此后,没有人对他的观点提出质疑。1642年,比利时的赫尔蒙特才首次对亚里士多德的观点提出了质疑。他将柳树和干土分别称重→栽种在密封桶内,只浇水→五年后→柳树增重74.47kg,而土壤只损失0.06kg.赫尔蒙特由此实验得出建造植物体的原料是水,但赫尔蒙特得出这样的结论忽视了 对实验的影响。
(2)随着认知水平的提高,1771年英国化学家普里斯特里进行了这样的探究:他将一支 点燃的蜡烛和一只小鼠分别放在密闭的钟罩里,不久蜡烛熄灭了,小鼠也很快死亡了;他又将绿色植物、点燃的蜡烛与小鼠一起放置在密闭的钟罩中——蜡烛不容易 熄灭,小鼠也不容易窒息死亡。普里斯特里实验结论是绿色植物能够 。
(3)1779年英格豪斯将普里斯特里实验在光下与无光下对照,证明植物更新空气离开 光照。1864年萨克斯进行了如下研究“紫苏——暗处理——部分叶片遮光——光照 一段时间——脱色后加碘液——观察实验现象”。结果证明绿叶在光下制造了淀 粉。萨克斯实验中对紫苏暗处理,是为了耗尽植物体内原有的 ;若不进行暗处理,实验时用碘液处理后遮光和不遮光部分均会 。
(4)1880年恩格尔曼水绵细胞实验证明光合作用的场所是叶绿体,至此人们才认识了光 合作用的原料、条件、产物。但光合作用中产生的O:中的氧原子究竟来是来自于参加光合作用的CO2还是H2O仍无法确定。鲁宾和卡门采用同位素示踪技术进行实 验:用18O标记水和二氧化碳,向绿色植物提供H218O和CO2,放在光下让其进行光合作用,检测产生的氧气均为18O。
从这组实验能否证明光合作用中释放的O2中的氧全部来自于参加光合作用的 H2O?——;如果不能应该如何改进? 。
Ⅱ、光合作用原理在农业生产中有着广泛应用,下图是北方地区A、B两种植物光合速率随光照强度改变的变化曲线,请分析回答:
(1)在较长时间连续阴雨的环境中,生长受到
显著影响的植物是 。
(2)图中的“a”点表示植物的 速率。
速率。
如果以缺镁的全营养液培养A植物幼苗,
则b点的移动方向是向 。
(3)c点与b点相比较,c点时叶肉细胞中C3的
含量 (填“高”“低”或“基本一致”)
科目:gzsw 来源:陕西省宝鸡市2010年高三教学质量检测(理综生物) 题型:选择题
(10分)I、人们对光和作用的认识经历了漫长的历程,请阅读绿色植物光合作用发现历程,回答相关问题。
(1)2400多年前古希腊学者亚里士多德提出:植物体是由“土壤汁”构成的。此后,没有人对他的观点提出质疑。1642年,比利时的赫尔蒙特才首次对亚里士多德的观点提出了质疑。他将柳树和干土分别称重→栽种在密封桶内,只浇水→五年后→柳树增重74.47kg,而土壤只损失0.06kg.赫尔蒙特由此实验得出建造植物体的原料是水,但赫尔蒙特得出这样的结论忽视了 对实验的影响。
(2)随着认知水平的提高,1771年英国化学家普里斯特里进行了这样的探究:他将一支 点燃的蜡烛和一只小鼠分别放在密闭的钟罩里,不久蜡烛熄灭了,小鼠也很快死亡了;他又将绿色植物、点燃的蜡烛与小鼠一起放置在密闭的钟罩中——蜡烛不容易 熄灭,小鼠也不容易窒息死亡。普里斯特里实验结论是绿色植物能够 。
(3)1779年英格豪斯将普里斯特里实验在光下与无光下对照,证明植物更新空气离开 光照。1864年萨克斯进行了如下研究“紫苏——暗处理——部分叶片遮光——光照 一段时间——脱色后加碘液——观察实验现象”。结果证明绿叶在光下制造了淀 粉。萨克斯实验中对紫苏暗处理,是为了耗尽植物体内原有的 ;若不进行暗处理,实验时用碘液处理后遮光和不遮光部分均会 。
(4)1880年恩格尔曼水绵细胞实验证明光合作用的场所是叶绿体,至此人们才认识了光 合作用的原料、条件、产物。但光合作用中产生的O:中的氧原子究竟来是来自于参加光合作用的CO2还是H2O仍无法确定。鲁宾和卡门采用同位素示踪技术进行实 验:用18O标记水和二氧化碳,向绿色植物提供H218O和CO2,放在光下让其进行光合作用,检测产生的氧气均为18O。
从这组实验能否证明光合作用中释放的O2中的氧全部来自于参加光合作用的 H2O?——;如果不能应该如何改进? 。
Ⅱ、光合作用原理在农业生产中有着广泛应用,下图是北方地区A、B两种植物光合速率随光照强度改变的变化曲线,请分析回答:
 (1)在较长时间连续阴雨的环境中,生长受到
(1)在较长时间连续阴雨的环境中,生长受到
显著影响的植物是 。
(2)图中的“a”点表示植物的 速率。
如果以缺镁的全营养液培养A植物幼苗,
则b点的移动方向是向 。
(3)c点与b点相比较,c点时叶肉细胞中C3的
含量 (填“高”“低”或“基本一致”)
科目:gzsw 来源:2016届安徽合肥市高三上第四次段考生物试卷(解析版) 题型:选择题
将水绵浸没在加有适宜培养液的大试管中,以人工白炽灯作为光源,每隔一段时间移动白炽灯增大其与大试管的距离,测定在不同距离下水绵产生气泡的速率,其他条件适宜不变,结果如图所示。下列相关叙述正确的是( )
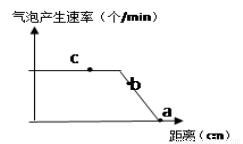
A.b点时限制气泡产生速率的主要因素为光照强度
B.a点与c点的干重相比较,a点较c点少
C.a点时只有线粒体和细胞质基质产生ATP
D.若培养液中缺镁,则a点应向右移
科目:gzsw 来源:2016届安徽省合肥市高三上学期第四次段考生物试卷(解析版) 题型:选择题
将水绵浸没在加有适宜培养液的大试管中,以人工白炽灯作为光源,每隔一段时间移动白炽灯增大其与大试管的距离,测定在不同距离下水绵产生气泡的速率,其他条件适宜不变,结果如图所 示。下列相关叙述正确的是( )
示。下列相关叙述正确的是( )

A.b点时限制气泡产生速率的主要因素为光照强度
B.a点与c点的干重相比较,a点较c点少
C.a点时只有线粒体和细胞质基质产生ATP
D.若培养液中缺镁,则a点应向右移
科目:gzsw 来源:2016届安徽合肥市高三上第四次段考生物试卷(解析版) 题型:选择题
将水绵浸没在加有适宜培养液的大试管中,以人工白炽灯作为光源,每隔一段时间移动白炽灯增大其与大试管的距离,测定在不同距离下水绵产生气泡的速率,其他条件适宜不变,结果如图所示。下列相关叙述正确的是

A.b点时限制气泡产生速率的主要因素为光照强度
B.a点与c点的干重相比较,a点较c点少
C.a点时只有线粒体和细胞质基质产生ATP
D.若培养液中缺镁,则a点应向右移
科目:gzsw 来源: 题型:选择题
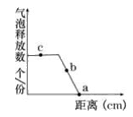
 将水绵浸没在加有适宜培养液的大试管中,以人工白炽灯作为光源,从近向远逐渐移动白炽灯调节其与大试管的距离,测定在不同距离下水绵释放气泡的速率,其他条件不变,结果如图所示.下列相关叙述正确的是( )
将水绵浸没在加有适宜培养液的大试管中,以人工白炽灯作为光源,从近向远逐渐移动白炽灯调节其与大试管的距离,测定在不同距离下水绵释放气泡的速率,其他条件不变,结果如图所示.下列相关叙述正确的是( )| A. | b点时限制气泡产生速率的主要因素为光照强度 | |
| B. | a点与c点的干重相比较,a点较c点少 | |
| C. | a点时只有线粒体和细胞质基质产生ATP | |
| D. | 若培养液中缺镁,则a点应向右移 |
科目:gzsw 来源:2014届宁夏银川市高三9月月考生物试卷(解析版) 题型:选择题
某兴趣小组将水绵浸没在加有适宜培养液(有充足的CO2)的大试管中,以人工白炽灯作为光源,从近向远逐渐移动白炽灯调节其与大试管的距离(不考虑温度对实验的干扰),测定在不同距离下水绵释放气泡的速率,其他条件不变,结果如图所示。下列相关叙述中不正确的是
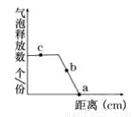
A.b点的限制因素为光照强度
B.如果培养液中缺Mg2+,在同样情况下完成该实验,a点应左移
C.c点与a点的干重相比较,c点较a点低
D.a点时水绵能产生ATP的细胞结构只有线粒体和细胞质基质
科目:gzsw 来源: 题型:单选题
科目:gzhx 来源:学习周报 化学 人教课标高一版(必修1) 2009-2010学年 第10期 总第166期 人教课标版 题型:058
氢气是发射航天器的理想能源,某同学利用废铝片与烧碱溶液反应制取氢气(装置如图所示).

(1)写出铝与烧碱溶液反应的化学方程式:________.
(2)该同学设计的实验步骤如下:
a.组装装置并检验其气密性
b.装入药品,关闭活塞m和n,将装置固定在铁架台上
c.打开分液漏斗的活塞m,使反应开始进行
d.当观察到B中有较多气体时,打开活塞n并点燃气体
①以上某步骤中有一处存在明显的设计错误,请指出错误之处:________;
②该同学在进行c步骤操作时,发现分液漏斗中的溶液不能滴下,你认为可能的原因是________.
(3)为了测定废铝片中铝的含量(假设杂质不与氢氧化钠反应产生氢气),取Wg废铝片,装于烧瓶A中,从分液漏斗向烧瓶中注入足量的氢氧化钠溶液,待反应完毕,量取气体的体积为VL(标准状况).
①测定气体体积时,要用到下列操作:
a.调平B、C仪器中的液面高度:上下移动量气管C,使B、C液面相平
b.读数:视线与凹液面的最低处相平
c.冷却至室温
正确的操作顺序是________;
②该废铝片中铝的质量分数为________.
(4)两份质量相等的同一种废铝片分别与足量的盐酸、氢氧化钠溶液反应,在相同条件下产生氢气的体积比为________.
科目:gzhx 来源: 题型:填空题
煤气化和液化是现代能源工业中重点考虑的能源综合利用方案。最常见的气化方法为用煤生产水煤气,而当前比较流行的液化方法为用煤生产CH3OH。
(1)已知:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH1
2CO(g)+O2(g)=2CO2(g) ΔH2
2H2(g)+O2(g)=2H2O(g) ΔH3
则反应CO(g)+2H2(g)=CH3OH(g)的ΔH=______。
(2)如图是该反应在不同温度下CO的转化率随时间变化的曲线。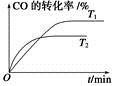
①T1和T2温度下的平衡常数大小关系是K1________K2(填“>”、“<”或“=”)。
②由CO合成甲醇时,CO在250 ℃、300 ℃、350 ℃下达到平衡时转化率与压强的关系曲线如下图所示,则曲线c所表示的温度为________ ℃。实际生产条件控制在250 ℃、1.3×104 kPa左右,选择此压强的理由是____________。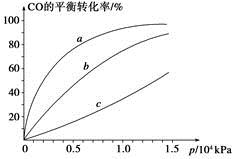
③以下有关该反应的说法正确的是________(填序号)。
A.恒温、恒容条件下,若容器内的压强不发生变化,则可逆反应达到平衡
B.一定条件下,H2的消耗速率是CO的消耗速率的2倍时,可逆反应达到平衡
C.使用合适的催化剂能缩短达到平衡的时间并提高CH3OH的产率
D.某温度下,将2 mol CO和6 mol H2充入2 L密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2 mol·L-1,则CO的转化率为80%
(3)一定温度下,向2 L固定体积的密闭容器中加入1 mol CH3OH(g),发生反应:CH3OH(g) CO(g)+2H2(g),H2的物质的量随时间变化的曲线如图所示。
CO(g)+2H2(g),H2的物质的量随时间变化的曲线如图所示。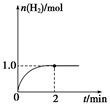
0~2 min内的平均反应速率v(CH3OH)=__________。该温度下,反应CO(g)+2H2(g) CH3OH(g)的平衡常数K=__________。相同温度下,若开始时加入CH3OH(g)的物质的量是原来的2倍,则__________(填序号)是原来的2倍。
CH3OH(g)的平衡常数K=__________。相同温度下,若开始时加入CH3OH(g)的物质的量是原来的2倍,则__________(填序号)是原来的2倍。
A.平衡常数 B.CH3OH的平衡浓度
C.达到平衡的时间 D.平衡时气体的密度
科目:gzhx 来源: 题型:填空题
煤气化和液化是现代能源工业中重点考虑的能源综合利用方案。最常见的气化方法为用煤生产水煤气,而当前比较流行的液化方法为用煤生产CH3OH。
(1)已知:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH1
2CO(g)+O2(g)=2CO2(g) ΔH2
2H2(g)+O2(g)=2H2O(g) ΔH3
则反应CO(g)+2H2(g)=CH3OH(g)的ΔH=______。
(2)如图是该反应在不同温度下CO的转化率随时间变化的曲线。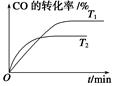
①T1和T2温度下的平衡常数大小关系是K1________K2(填“>”、“<”或“=”)。
②由CO合成甲醇时,CO在250 ℃、300 ℃、350 ℃下达到平衡时转化率与压强的关系曲线如下图所示,则曲线c所表示的温度为________ ℃。实际生产条件控制在250 ℃、1.3×104 kPa左右,选择此压强的理由是____________。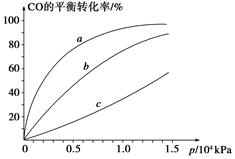
③以下有关该反应的说法正确的是________(填序号)。
A.恒温、恒容条件下,若容器内的压强不发生变化,则可逆反应达到平衡
B.一定条件下,H2的消耗速率是CO的消耗速率的2倍时,可逆反应达到平衡
C.使用合适的催化剂能缩短达到平衡的时间并提高CH3OH的产率
D.某温度下,将2 mol CO和6 mol H2充入2 L密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2 mol·L-1,则CO的转化率为80%
(3)一定温度下,向2 L固定体积的密闭容器中加入1 mol CH3OH(g),发生反应:CH3OH(g)CO(g)+2H2(g),H2的物质的量随时间变化的曲线如图所示。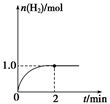
0~2 min内的平均反应速率v(CH3OH)=__________。该温度下,反应CO(g)+2H2(g)CH3OH(g)的平衡常数K=__________。相同温度下,若开始时加入CH3OH(g)的物质的量是原来的2倍,则__________(填序号)是原来的2倍。
A.平衡常数 B.CH3OH的平衡浓度
C.达到平衡的时间 D.平衡时气体的密度