
科目:gzsw 来源:2014届湖北省公安县高三上学期开学考试生物试卷(解析版) 题型:综合题
哺乳动物越冬时,褐色脂肪组织在维持体温恒定方面具有重要作用。为了解寒冷条件下褐色脂肪组织产热的调节机理,研究人员以雄性布氏田鼠为实验材料展开相关研究。实验的部分结果如下表所示。
|
检测项目 |
对照 |
冷处理1d |
冷处理4周 |
|
褐色脂肪组织线粒体中的蛋白质总量(mg) |
3.5 |
5.3 |
10.4 |
|
具有生物活性的甲状腺激素含量(ng/mL血清) |
0.57 |
1.00 |
1.48 |
请回答:
(1)褐色脂肪组织细胞主要通过脂肪氧化分解产热。与相同质量的糖类相比,脂肪氧化分解能够释放更 的热能以维持体温。
(2)实验过程中,随冷处理时间的延长,褐色脂肪组织线粒体中的蛋白质总量逐渐 。其生理意义是:线粒体是 的主要场所。线粒体中的 增多,促使产热增多。
(3)根据上表中的数据,有人推测雄性布氏田鼠在寒冷条件下褐色脂肪组织产热的调节机理是:田鼠处于寒冷环境中,在神经调节下,由 释放的 增多,进而导致 和甲状腺激素分泌增多,甲状腺激素作用于脂肪组织细胞,最终产热增多。
科目:gzsw 来源:2014届江西省高三开学摸底考试生物试卷 题型:综合题
哺乳动物越冬时,褐色脂肪组织在维持体温恒定方面具有重要作用。为了解寒冷条件下褐色脂肪组织产热的调节机理,研究人员以雄性布氏田鼠为实验材料展开相关研究。实验的部分结果如下表所示。
|
检测项目 |
对照 |
冷处理1d |
冷处理4周 |
|
褐色脂肪组织线粒体中的蛋白质总量(mg) |
3.5 |
5.3 |
10.4 |
|
具有生物活性的甲状腺激素含量(ng/mL血清) |
0.57 |
1.00 |
1.48 |
请回答:
(1)褐色脂肪组织细胞主要通过脂肪氧化分解产热。与相同质量的糖类相比,脂肪氧化分解能够释放更 的热能以维持体温。
(2)实验过程中,随冷处理时间的延长,褐色脂肪组织线粒体中的蛋白质总量逐渐 。其生理意义是:线粒体是 的主要场所。线粒体中的 增多,促使产热增多。
(3)根据上表中的数据,有人推测雄性布氏田鼠在寒冷条件下褐色脂肪组织产热的调节机理是:田鼠处于寒冷环境中,在神经调节下,由 释放的 增多,进而导致 和甲状腺激素分泌增多,甲状腺激素作用于脂肪组织细胞,最终产热增多。
科目:gzsw 来源: 题型:综合题
哺乳动物越冬时,褐色脂肪组织在维持体温恒定方面具有重要作用。为了解寒冷条件下褐色脂肪组织产热的调节机理,研究人员以雄性布氏田鼠为实验材料展开相关研究。实验的部分结果如下表所示。
| 检测项目 | 对照 | 冷处理1d | 冷处理4周 |
| 褐色脂肪组织线粒体中的蛋白质总量(mg) | 3.5 | 5.3 | 10.4 |
| 具有生物活性的甲状腺激素含量(ng/mL血清) | 0.57 | 1.00 | 1.48 |
科目:gzsw 来源: 题型:综合题
哺乳动物越冬时,褐色脂肪组织在维持体温恒定方面具有重要作用。为了解寒冷条件下褐色脂肪组织产热的调节机理,研究人员以雄性布氏田鼠为实验材料展开相关研究。实验的部分结果如下表所示。
| 检测项目 | 对照 | 冷处理1d | 冷处理4周 |
| 褐色脂肪组织线粒体中的蛋白质总量(mg) | 3.5 | 5.3 | 10.4 |
| 具有生物活性的甲状腺激素含量(ng/mL血清) | 0.57 | 1.00 | 1.48 |
科目:gzsw 来源: 题型:
| 检测项目 | 对照 | 冷处理1d | 冷处理4周 |
| 褐色脂肪组织线粒体中的蛋白质总量(mg) | 3.5 | 5.3 | 10.4 |
| 具有生物活性的甲状腺激素含量(ng/mL血清) | 0.57 | 1.00 | 1.48 |
科目:gzsw 来源: 题型:
| 检测项目 | 对照 | 冷处理1天 | 冷处理4周 |
| 褐色脂肪组织线粒体中的蛋白质总量(mg) | 3.5 | 5.3 | 10.4 |
| 具有生物活性的甲状腺激素含量(ng/mL血清) | 0.57 | 1.00 | 1.48 |
科目:gzdl 来源: 题型:
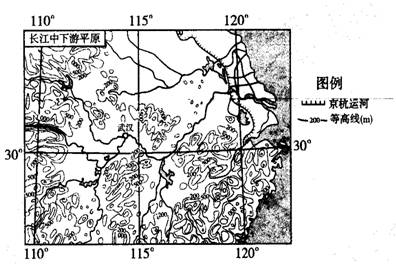 根据材料回答下列问题。
根据材料回答下列问题。
材料 夏天人体感到炎热主要是由
高温引起的,人的皮肤温度为320C,
如果气温高于皮肤温度时,人就会有
热感,气温越高,维持时间越长,人的
热感愈加明显。同样的高温天气条件下,
风小、湿度大、最低气温高都会加剧人
们所感受到的炎热程度。
(1)武汉是长江流域的“三大火炉”之一,简述武汉每年7-8月人们会感到非常闷热的原因。(8分)
(2)2012年12月26日京广高铁全钱开通,加快了珠江三角洲地区产业向湖北区域的转移,分析产业转移对湖北地区人口迁移和城市化进程所产生的有利影响。(6分)
(3)简述图中南部地区通过综合利用农业资源,调整农业结构的重要意义。(8分)
科目:gzdl 来源: 题型:
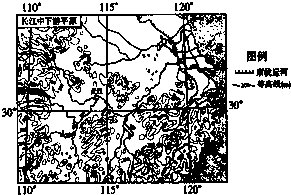 根据材料回答下列问题.
根据材料回答下列问题.科目:gzsw 来源: 题型:
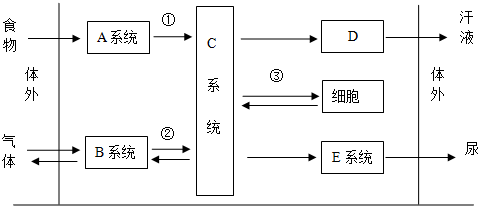
肾脏排尿的意义是( )
①人体排出水分的最主要途径 ②可以排出部分热量,以利于调节体温 ③可以排出多余的Na+④可以排出体内多余的钾盐和葡萄糖 ⑤可以排出代谢废物 ⑥可以维持体内水分和无机盐的平衡
A. ②②③④ B.①③④⑤ C.①③⑤⑥ D.②③④⑤
科目:gzsw 来源: 题型:解答题
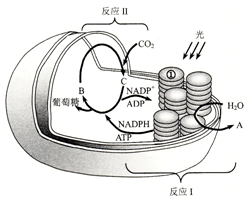 光合作用是维持生命的能量来源,地球上大部分的能量物质也是经过光合作用由太阳能而来.如图是某植物光合作用过程示意图.
光合作用是维持生命的能量来源,地球上大部分的能量物质也是经过光合作用由太阳能而来.如图是某植物光合作用过程示意图.| 组别 | 实验条件 | 30min内上浮叶圆片平均数(片) | ||
| 温度 | 光照强度 | NaHCO3浓度 | ||
| 组1 | 10℃ | 40W白炽灯 | 1% | 3 |
| 组2 | 10℃ | 100W白炽灯 | 1% | 5 |
| 组3 | ? | 100W白炽灯 | 1% | 8 |
| 组4 | 25℃ | 100W白炽灯 | 4% | 10 |
| 组5 | 15℃ | 60W白炽灯 | 0% | 0 |
科目:gzhx 来源: 题型:解答题
| 时间/min | n(SO2)/mol | n(O2)/mol |
| 0 | 0.10 | 0.050 |
| 4 | 0.050 | 0.025 |
| 5 | 0.040 | |
| 8 | 0.020 |
科目:czsw 来源: 题型:解答题
科目:gzyw 来源:河南省期末题 题型:阅读理解与欣赏
科目:gzhx 来源: 题型:
| 容 器 | 甲 | 乙 |
| 反应物投入量 | 1mol CO2、3mol H2 | a mol CO2、3a mol H2、 b mol CH3OH(g)、b mol H2O(g) |
科目:gzhx 来源: 题型:
| 容 器 | 甲 | 乙 |
| 反应物投入量 | 1mol CO2、3mol H2 | a mol CO2、b mol H2、 c mol CH3OH(g)、c mol H2O(g) |
科目:gzhx 来源: 题型:
研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
(1)CO可用于炼铁,已知:Fe2O3(s) + 3C(s)=2Fe(s) + 3CO(g) ΔH 1=+489.0 kJ·mol-1,C(s) +CO2(g)=2CO(g) ΔH 2 =+172.5 kJ·mol-1
则CO还原Fe2O3(s)的热化学方程式为 ▲ 。
(2)分离高炉煤气得到的CO与空气可设计成燃料电池(以KOH溶液为电解液)。
|
 写出该电池的负极反应式: ▲ 。
写出该电池的负极反应式: ▲ 。 (3)CO2和H2充入一定体积的密闭容器中,在两种温度
下发生反应:
CO2(g) +3H2(g) CH3OH(g) +H2O(g)
CH3OH(g) +H2O(g)
|
|
(填“>”或“=”或“<”)。
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
| 容 器 | 甲 | 乙 |
| 反应物投入量 | 1molCO2、3molH2 | a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) |
若甲中平衡后气体的压强为开始的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则c的取值范围为 ▲ 。
(4)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2。紫外光照射时,在不同催化剂(I、II、III)作用下,CH4产量随光照时间的变化见图11。在0~15小时内,CH4的平均生成速率I、II和III从大到小的顺序为 ▲ (填序号)。

|

(5)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系见图12。
①乙酸的生成速率主要取决于温度影响的范围是 ▲ 。
②Cu2Al2O4可溶于稀硝酸,写出有关的离子方程式: ▲ 。
科目:gzhx 来源: 题型:
研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
(1)CO可用于炼铁,已知:Fe2O3(s) + 3C(s)=2Fe(s) + 3CO(g) ΔH 1=+489.0 kJ· mol-1,C(s) +CO2(g)=2CO(g) ΔH 2 =+172.5 kJ·mol-1, 则CO还原Fe2O3(s)的热化学方程式为 ▲ 。
 (2)CO与O2设计成燃料电池(以KOH溶液为电解液)。该电池的负极反应式为 ▲ 。
(2)CO与O2设计成燃料电池(以KOH溶液为电解液)。该电池的负极反应式为 ▲ 。
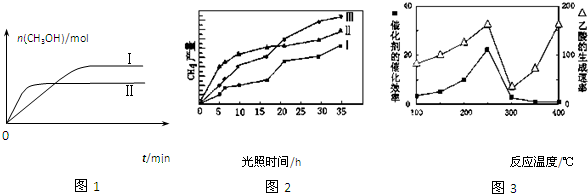
(3)CO2和H2充入一定体积的恒容密闭容器中,在两种温度下发生反应:CO2(g) +3H2(g) CH3OH(g) +H2O(g) 测得CH3OH的物质的量随时间的变化如图5。
CH3OH(g) +H2O(g) 测得CH3OH的物质的量随时间的变化如图5。
|
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
| 容 器 | 甲 | 乙 |
| 反应物投入量 | 1molCO2、3molH2 | a molCO2、3a molH2、 b molCH3OH(g)、b molH2O(g) |
若甲中平衡后气体的压强为开始的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则b的取值范围为 ▲ 。
 (4)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2。紫外光照射时,在不同催化剂(I、II、III)作用下,CH4产量随光照时间的变化如图6。在0~15小时内,CH4的平均生成速率I、II和III从小到大的顺序为 ▲ (填序号)。
(4)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2。紫外光照射时,在不同催化剂(I、II、III)作用下,CH4产量随光照时间的变化如图6。在0~15小时内,CH4的平均生成速率I、II和III从小到大的顺序为 ▲ (填序号)。
|

(5)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系如图7。
①当温度在 ▲ 范围时,温度是乙酸生成速率的主要影响因素。
②Cu2Al2O4可溶于稀硝酸,稀硝酸还原产物为NO,写出有关的离子方程式 ▲ 。
科目:gzhx 来源: 题型:
研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
(1)CO可用于炼铁,已知:Fe2O3(s)+3C(s)=2Fe (s)+3CO(g) ΔH 1=+489.0 kJ· mol-1,
C(s) +CO2(g)=2CO(g) ΔH 2 =+172.5 kJ·mol-1, 则CO还原Fe2O3(s)的热化学方程式为 。
(2)CO与O2设计成燃料电池(以KOH溶液为电解液)。该电池的负极反应式为 。
(3)CO2和H2充入一定体积的恒容密闭容器中,在两种温度下发生反应:CO2(g) +3H2(g) 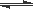 CH3OH(g) +H2O(g) 测得CH3OH的物质的量随时间的变化如图5。
CH3OH(g) +H2O(g) 测得CH3OH的物质的量随时间的变化如图5。
|

①该反应的ΔH 0(填“大于或小于”),曲线I、Ⅱ对应的平衡常数大小关系为
KⅠ KⅡ (填“>、=或<”)。
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
| 容 器 | 甲 | 乙 |
| 反应物投入量 | 1 mol CO2、3 mol H2 | a molCO2、3a molH2、 b molCH3OH(g)、b molH2O(g) |
若甲中平衡后气体的压强为开始的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则b的取值范围为 。
(4)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2。紫外光照射时,在不同催化剂(I、II、III)作用下,CH4产量随光照时间的变化如图6。在0~15小时内,CH4的平均生成速率I、II和III从小到大的顺序为 (填序号)。

(5)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。
在不同温度下催化剂的催化效率与乙酸的生成速率的关系如图7。
①当温度在 范围时,温度是乙酸生成速率的主要影响因素。
②Cu2Al2O4可溶于稀硝酸,稀硝酸还原产物为NO,写出有关的离子方程式 。
科目:gzhx 来源:2016届福建省高三下学期周考五理科综合化学试卷(解析版) 题型:填空题
研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
(1)CO可用于炼铁,已知:
Fe2O3(s)+3C(s)═2Fe(s)+3CO(g)△H1=+489.0kJ•mol-1,
C(s)+CO2(g)═2CO(g)△H2=+172.5kJ•mol-1
则CO还原Fe2O3(s)的热化学方程式为__________。
(2)分离高炉煤气得到的CO与空气可设计成燃料电池(以KOH溶液为电解液)。写出该电池的负极反应式:__________。
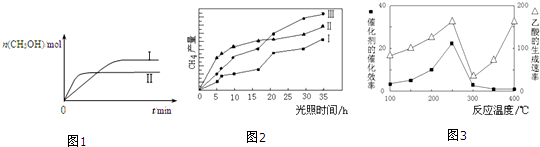
(3)CO2和H2充入一定体积的密闭容器中,在两种温度下发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) 测得CH3OH的物质的量随时间的变化见图1。
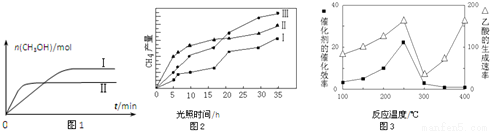
①曲线I、Ⅱ对应的平衡常数大小关系为KⅠ__________KⅡ(填“>”或“=”或“<”).
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
容 器 | 甲 | 乙 |
反应物投入量 | 1molCO2、3molH2 | a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) |
若甲中平衡后气体的压强为开始的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则c的取值范围为__________。
(4)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2.紫外光照射时,在不同催化剂(I、II、III)作用下,CH4产量随光照时间的变化见图2.在0~15小时内,CH4的平均生成速率I、II和III从大到小的顺序为__________(填序号).
(5)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系见图3。
①乙酸的生成速率主要取决于温度影响的范围是__________。
②Cu2Al2O4可溶于稀硝酸,写出有关的离子方程式:__________。