
科目:gzhx 来源: 题型:
| ||
| △ |
| ||
| △ |
| ||
| ||
科目:gzhx 来源:2012-2013学年福建省5月高考三轮模拟化学试卷(解析版) 题型:填空题
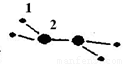
(1)M由两种短周期元素组成,每个M分子含有18个电子,其分子球棍模型如图所示。测得M的摩尔质量为32g/mol。画出编号为2的原子结构示意图: 。
(2)已知1.0mol·L—1NaHSO3溶液的pH为3.5,加入氯水,振荡后溶液pH迅速降低。溶液pH降低的原因是 (用离子方程式表示)。
(3)在常温常压和光照条件下,N2在催化剂(TiO2)表面与H2O反应,生成1molNH3和O2时的能量变化值为382.5kJ,达到平衡后此反应NH3生成量与温度的实验数据如下表。则该反应的热化学方程式为 。
|
T/K |
303 |
313 |
323 |
|
NH3生成量/(10—1mol) |
4.3 |
5.9 |
6.0 |
(4)在溶液中,一定浓度的NH4+能溶解部分Mg(OH)2固体,反应如下:
2NH4+(aq) + Mg(OH)2(s)
 Mg2+(aq)
+2NH3·H2O(aq)
Mg2+(aq)
+2NH3·H2O(aq)
写出上述反应的平衡常数表达式
某研究性学习小组为探究Mg2+与NH3·H2O反应形成沉淀的情况,设计如下两组实验
|
实验① |
等体积1 mol/L氨水和0.1 mol/L MgCl2溶液混合 |
生成白色沉淀 |
|
实验② |
等体积0.1 mol/L氨水和1 mol/L MgCl2溶液混合 |
无现象 |
请分析实验①、②产生不同现象的原因: 。
(5)在室温下,化学反应I—(aq)+ ClO—(aq) = IO—(aq) + Cl—(aq)的反应物初始浓度、溶液中的氢氧根离子初始浓度及初始速率间的关系如下表所示:
|
实验编号 |
I—的初始浓度 (mol·L—1) |
ClO—的初始浓度 (mol·L—1) |
OH—的初始浓度 (mol·L—1) |
初始速率v (mol·L—1· s—1) |
|
1 |
2 × 10—3 |
1.5 × 10—3 |
1.00 |
1.8 × 10—4 |
|
2 |
a |
1.5 × 10—3 |
1.00 |
3.6 × 10—4 |
|
3 |
2 × 10—3 |
3 × 10—3 |
2.00 |
1.8 × 10—4 |
|
4 |
4 × 10—3 |
3 × 10—3 |
1.00 |
7.2 × 10—4 |
已知表中初始反应速率与有关离子浓度关系可以表示为v= k [I—]1 [ClO—]b [OH—]c(温度一定时,k为常数)。
①设计实验2和实验4的目的是 ;
②若实验编号4的其它浓度不变,仅将溶液的酸碱值变更为pH = 13,反应的初始速率v= 。
科目:gzhx 来源:2013-2014学年浙江省高三上学期期末理综化学试卷(解析版) 题型:填空题
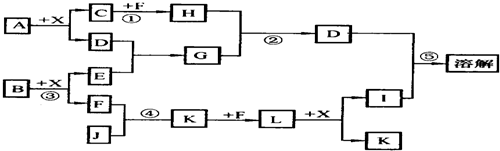
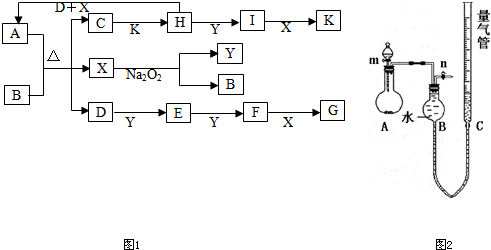
某已知A、B均是由两种短周期元素组成的化合物,A中某元素的质量分数为25%,B的焰色反应呈黄色,C、J、X是同周期的元素的简单氢化物,X为无色液体,C、J为气体,D是一种不溶于水的白色固体。反应生成的水均已略去。它们有如下图所示的关系。
(1)写出化学式:A ,E ,L ;
(2)在反应①②③④⑤中属于氧化还原反应的是 ;
(3)反应③化学方程式为: ;
(4)写出下列离子方程式:反应② ;
G溶液与M溶液的反应 。
科目:gzhx 来源:2012届浙江省杭州市高复高三上学期11月份月考化学试卷 题型:填空题
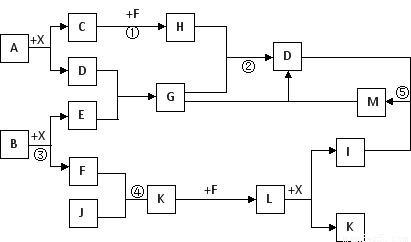
(9分).A~L是由6种短周期元素组成的物质,各物质之间有如下转化关系:
已知:(a) C、E是气体单质,F是日常生活中的常用金属;(b) B、J是氧化物,且J是能使澄清石灰水变浑浊的无色无味气体;(c)化合物A、D、I、L的焰色反应显黄色;(d)白色沉淀K既溶于H溶液,又能溶于D溶液;(e)反应①是工业上生产D和C的重要方法。请回答:
(1)写出F的化学式 ,D的电子式 ,J的结构式 。
(2)写出有关反应的化学方程式:
反应① ;
反应②  。
。
(3)L溶液和G溶液混合能发生反应,其离子方程式为 。
科目:gzhx 来源: 题型:
(9分).A~L是由6种短周期元素组成的物质,各物质之间有如下转化关系:
已知:(a)C、E是气体单质,F是日常生活中的常用金属;(b)B、J是氧化物,且J是能使澄清石灰水变浑浊的无色无味气体;(c) 化合物A、D、I、L的焰色反应显黄色;(d) 白色沉淀K既溶于H溶液,又能溶于D溶液;(e) 反应①是工业上生产D和C的重要方法。请回答:
(1)写出F的化学式 ,D的电子式 ,J的结构式 。
(2)写出有关反应的化学方程式:
反应① ;
反应② 。
(3)L溶液和G溶液混合能发生反应,其离子方程式为 。
科目:gzhx 来源:2013-2014学年山东省滨州市高三3月模拟(一模)考试化学试卷(解析版) 题型:填空题
X、Y、Z均是由两种短周期元素组成的无机物,它们的每个分子中均含有l8个电子,相关信息如下表所示(“/”表示相应的信息略去):
化合物 | X | Y | Z |
分子中含有的原子个数 | / | 4 | / |
摩尔质量/g·mol-l | 32 | 34 | / |
回答下列问题:
(1)X常用作火箭推进剂,其分子的球棍模型为 ,则X的化学式为 .
,则X的化学式为 .
(2)Y的化学性质描述正确的是 。
a.不稳定性 b.弱碱性 c.氧化性 d.还原性
(3)Z的化学式可用H2A表示。将一定量的Z气体通入0.05mol·L-1CuSO4溶液中,二者恰好完全反应。已知Ksp(CuA)=6.0×10-36。若不考虑溶液体积的变化,则:
①反应后溶液的pH= 。
②若反应后溶液中c(A2-)=2.0×10-30mol·L-1,则溶液中c(Cu2+)= mol·L-1。
(4)将一定量的Z气体通人NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,产生的气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发)。

①O点溶液中所含溶质的化学式为 。
②已知a点溶液呈碱性,该溶液中离子的物质的量浓度由大到小的顺序是 。
科目:gzhx 来源:浙江省期中题 题型:推断题

科目:gzhx 来源: 题型:
A~L是由6种短周期元素组成的物质,各物质之间有如下转化关系:

已知:(a) C、E是气体单质,F是日常生活中的常用金属;(b) B、J是氧化物,且J是能使澄清石灰水变浑浊的无色无味气体;(c) 化合物A、D、I、L的焰色反应显黄色;(d) 白色沉淀K既溶于H溶液,又能溶于D溶液;(e) 反应①是工业上生产D和C的重要方法。请回答:
(1)写出元素C在周期表的位置 ,D的电子式 ,J的结构式 。
(2)写出有关反应的化学方程式:反应① ;
反应②(若J是过量的) 。
(3)已知I溶液和L溶液混合能发生反应,其离子方程式为 。
则等浓度的NaAlO2、Na2CO3、NaHCO3、NaOH和苯酚钠溶液的pH从大到小得顺序为
科目:gzhx 来源: 题型:
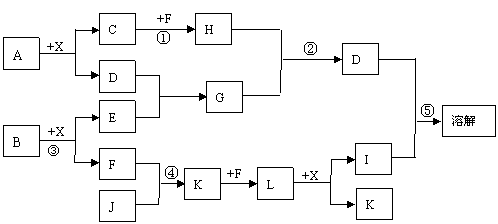
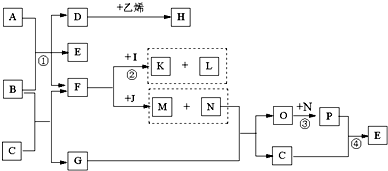
已知A、B均是由两种短周期元素组成的化合物,A中某元素的质量分数为75%,C、J 同为第二周期元素的气态氢物,X为无色液体,D具有两性。反应生成的水均已略去。它们有如下图所示的关系。
![]()
 |
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() 请回答下列问题:
请回答下列问题:
(1)A的化学式是 ,B的电子式为 。
(2)反应③中每生成l mol F,转移电子的数目为 。
(3)反应④的化学方程式为 。
(4)G溶液与过量H气体反应的离子方程式为
科目:gzhx 来源: 题型:
A~L是由6种短周期元素组成的物质,各物质之间有如下转化关系:

已知:
(a) C、E是气体单质,E是一种理想的清洁能源,F是日常生活中的常用金属;
(b) B、J是氧化物,且J是能使澄清石灰水变浑浊的无色无味气体;
(c) 化合物A、D、I、L的焰色反应显黄色;
(d) 白色沉淀K既溶于H溶液,又能溶于D溶液;
(e) 反应①是工业上生产D和C的重要方法。
请回答下列问题:
(1)写出F的化学式 ,D的电子式 。
(2)写出有关反应的化学方程式:
反应① ;
反应② 。
(3)G溶液呈 性(填“酸”、“碱”或“中”),请用离子方程式表示其原因:
。
科目:gzhx 来源:甘肃省天水一中2012届高三百题集化学试题 题型:043
五环以图形简洁美观、寓意隽永而备受人们喜爱.如图所示![]() ,五个环分别代表A、B、C、D、E五种化合物,这五种化合物由五种短周期元素组成,每种化合物仅含两种元素,两环相交是指两种物质含有相同元素.A是沼气的主要成分;B、E分子中所含电子数都为18,B不稳定,具有较强的氧化性,在二氧化锰催化作用下加快分解.E是由六个原子构成的分子,C是工业制玻璃的主要原料之一;D中所含的两种元素的原子个数之比为3∶4.
,五个环分别代表A、B、C、D、E五种化合物,这五种化合物由五种短周期元素组成,每种化合物仅含两种元素,两环相交是指两种物质含有相同元素.A是沼气的主要成分;B、E分子中所含电子数都为18,B不稳定,具有较强的氧化性,在二氧化锰催化作用下加快分解.E是由六个原子构成的分子,C是工业制玻璃的主要原料之一;D中所含的两种元素的原子个数之比为3∶4.
(1)写出A的电子式________.
(2)指出B、E分子中所含共价键类型________(填“极性键”、“非极性键”或“既有极性键又有非极性键”).
(3)写出C、D的化学式________、________.
说明二者有高熔点的理由________.
科目:gzhx 来源:湖南省澧县一中、岳阳县一中2012届高三11月联考化学试题 题型:058
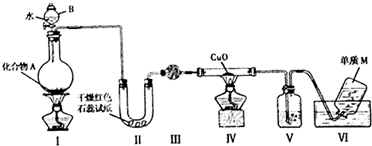
固态化合物A由两种短周期元素组成,可与水发生复分解反应,甲组同学用下图装置(夹持装置略)对其进行探究实验.
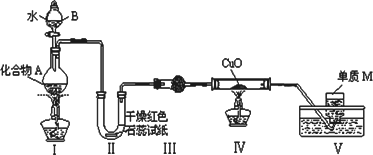
(1)仪器B的名称是________.
(2)实验中,Ⅱ中的试纸变蓝,Ⅳ中黑色粉末逐渐变为红色并有气体M生成,则Ⅳ发生反应的化学方程式为________;Ⅲ中的试剂为________.
(3)乙组同学进行同样实验,但装置连接顺序为Ⅰ——Ⅲ——Ⅳ——Ⅱ——Ⅴ,此时Ⅱ中现象为________,原因是________.
(4)经上述反应,2.5 g化合物A理论上可得0.56 L(标准状况)M;则A的化学式为________.
科目:gzhx 来源: 题型:
(1)在实验室用集气瓶收集气体G和气体H。则收集气体G的方法是(写一种):__________
__________;检验气体H已收集满的方法是:__________。
(2)在实验室进行操作①时,除了使用酒精灯、铁圈、铁架台及夹持仪器外,还缺少的仪器是:____________;在进行操作②时,应在HCl的气氛中加热脱水,其目的是:__________。
(3)A+H2O![]() B+H的基本反应类型为__________,H的电子式为__________。
B+H的基本反应类型为__________,H的电子式为__________。
(4)如下图所示支管中,左管中放入MnO4固体,右管中放入小块钠,再向两管均加入适量8 mol·L-1的盐酸,半分钟后,盖上橡胶塞并将此支管固定在铁架台上。用一照相机对准此支管,按快门,闪光灯闪亮。请回答:
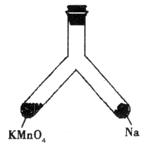
①“照相”之前,左管中反应生成的气体是__________(写化学式),若生成0.5 mol该气体,则转移电子的物质的量是__________mol。
②“照相”时,灯光闪亮,支管随之出现的现象是__________。
科目:gzhx 来源: 题型:
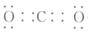
(1)A的化学式是__________________________,
H的电子式是________________________。
(2)反应②的化学方程式是_______________________________。
(3)写出离子方程式:
反应①__________________;反应③_____________________。
(4)在熔融条件下电解Q的化学方程式是_______________________。
科目:gzhx 来源: 题型:
| ||
| ||
科目:gzhx 来源: 题型:
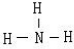
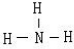
科目:gzhx 来源: 题型:


| ||
| ||
科目:gzhx 来源: 题型:

| ||
| △ |
| ||
| △ |