
科目:gzhx 来源:读想用 高二化学(上) 题型:022
将质量分数分别为25%氨水与5%氨水等质量混合后,所得氨水的质量分数为________;若将上述两溶液等体积混合,所得氨水的质量分数________15%(填“大于”“小于”或“等于”).
科目:gzhx 来源:上海模拟题 题型:不定项选择题

科目:gzhx 来源: 题型:
下列说法正确的是
A.100 ℃时,纯水中c(H +)=1×10-6 mol·L-1,此时纯水显酸性
B.25℃时,pH=10的氨水与pH=4盐酸等体积混合,所得溶液呈酸性
C.25℃时,将pH=a的醋酸溶液稀释10倍后,溶液的pH=b,则b= (a+1)
D.25℃时,![]() 的溶液中,Na+、CO32-、Cl-一定能大量共存
的溶液中,Na+、CO32-、Cl-一定能大量共存
科目:gzhx 来源: 题型:
.25℃时,弱酸的电离平衡常数如右表,下列说法正确的是( )
| 弱酸 | CH3COOH | HCN | H2CO3 |
| K | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
A.等物质的量浓度溶液pH关系:pH(NaCN)> pH(Na2CO3)> pH(CH3COONa)
B.amol/L HCN与bmol/LNaOH溶液等体积混合后所得溶液中c(Na+)>c(CN-),则a一定小于b
C.往冰醋酸中逐滴加水,溶液导电能力先增大,后减小
D.NaHCO3和Na2CO3的混合液中:c(Na+)+c(H+)=c(OH-)+c(HCO-3)+c(CO32-)
科目:gzhx 来源:物理教研室 题型:013
A.1.7
B.2.0
C.12.0
D.12.3
科目:gzhx 来源: 题型:013
已知氨水越浓,密度越小,现将20%氨水与10%氨水等体积混合,则混合后溶液的质量分数为
[ ]
科目:gzhx 来源:物理教研室 题型:013
已知氨水越浓,密度越小,现将20%氨水与10%氨水等体积混合,则混合后溶液的质量分数为
[ ]
科目:gzhx 来源: 题型:
下列叙述正确的是( ▲ )
A.某液体物质的摩尔质量大于18 g·mol-1,则该物质密度一定比水大
B.c mol·L-1 KCl溶液的密度为ρg/cm3,则此KCl溶液的质量分数为74.5c÷1000ρ×100%
C.将90 % H2SO4溶液与10 % H2SO4溶液等体积混合,其质量分数一定等于50 %
D.同温同压下,分别将充满HCl、NO2的两支试管倒立于蒸馏水中足够长时间,假设不考虑溶质扩散,两支试管中溶液的物质的量浓度之比为3:2
科目:gzhx 来源:0116 期末题 题型:单选题
科目:gzhx 来源: 题型:
下列关于电解质溶液的叙述中正确的是 ( )
A.Na2CO3、NaHCO3两种盐的溶液中,离子种类不相同
B.常温下1mol・LCH3COOH溶液与1mol/NaOH溶液等体积混合,所得溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
C.溶质的物质的量浓度相同时NH4C1和NH4HSO4两种溶液中c(NH4+)前者小于后者
D.常温下,某溶液中由水电离出的c(H+)为10-5mol/L,则此溶液可能是盐酸
科目:gzhx 来源:同步题 题型:不定项选择题
科目:gzhx 来源: 题型:
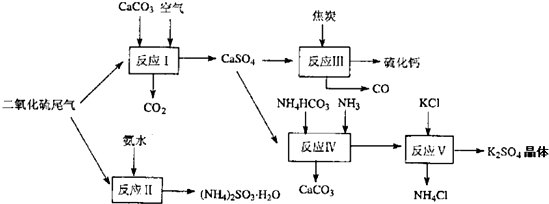
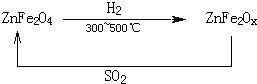
科目:gzhx 来源: 题型:阅读理解
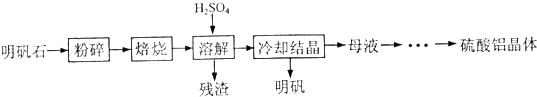
| 物质 | α-Al2O3 | γ-Al2O3 |
| 性质 | 不溶于水和酸 | 不溶于水,溶于强酸或强碱,加热至1200℃可转化为α-Al2O3 |
| 温度/℃ 溶解度/g |
0 | 20 | 40 | 60 | 80 | 100 |
| Al2(SO4)3 | 31.2 | 36.4 | 46.1 | 59.2 | 73.0 | 89.0 |
| 明矾 | 3.0 | 5.9 | 11.7 | 25 | 71 | 154 |
科目:gzhx 来源: 题型:阅读理解
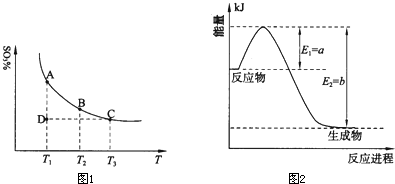
| 10-7y |
| x-y |
| 10-7y |
| x-y |
科目:gzhx 来源: 题型:阅读理解
科目:gzhx 来源: 题型:阅读理解
| ||