
科目:gzhx 来源:2012-2013学年新疆兵团农二师华山中学高一上学期期末考试化学试卷(带解析) 题型:填空题
氧化还原反应在工农业生产和日常生活中有广泛运用。(1)人通过呼吸作用吸入氧气,氧化体内的葡萄糖(C6H12O6)提供能量以维持生命活动,反应为:C6H12O6+6O2 = 6CO2+6H2O+能量,该反应中的还原剂是 。
(2)罐头厂在装食物罐头时,通常要添加一些对人体无害的防腐剂,防止食物被空气中的氧气氧化而变质。此类食物防腐剂应具有 。(填“氧化性”或“还原性”);
(3)Fe3+在工业上有重要用途。例如印刷电路板是由高分子材料和铜箔复合而成,可用FeCl3溶液作“腐蚀剂”刻制印刷电路,写出离子方程式 。
(4)缺铁性贫血患者应补充Fe2+,通常以硫酸亚铁的形式,而硫酸铁则无这种药效。当用硫酸亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是 。如果药片已经失效,应如何检验?写出主要操作与现象:
科目:gzhx 来源:2015届新疆兵团农二师华山中学高一上学期期末考试化学试卷(解析版) 题型:填空题
氧化还原反应在工农业生产和日常生活中有广泛运用。(1)人通过呼吸作用吸入氧气,氧化体内的葡萄糖(C6H12O6)提供能量以维持生命活动,反应为:C6H12O6+6O2 = 6CO2+6H2O+能量,该反应中的还原剂是 。
(2)罐头厂在装食物罐头时,通常要添加一些对人体无害的防腐剂,防止食物被空气中的氧气氧化而变质。此类食物防腐剂应具有 。(填“氧化性”或“还原性”);
(3)Fe3+在工业上有重要用途。例如印刷电路板是由高分子材料和铜箔复合而成,可用FeCl3溶液作“腐蚀剂”刻制印刷电路,写出离子方程式 。
(4)缺铁性贫血患者应补充Fe2+,通常以硫酸亚铁的形式,而硫酸铁则无这种药效。当用硫酸亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是 。如果药片已经失效,应如何检验?写出主要操作与现象:
科目:gzhx 来源:2011-2012学年山西省大同市实验中学高一上学期期中考试化学试卷 题型:填空题
(4分)氧化还原反应在工农业生产和日常生活中有广泛的应用。
(1)人通过呼吸作用吸入氧气,氧化体内的葡萄糖(C6H12O6)提供能量以维持生命活动。反应为:C6H12O6+6O2=6CO2+6H2O+能量,该反应中的还原剂是 。
(2)罐头厂在装食物罐头时,通常要添加一些对人体无害的防腐剂,防止食物被空气中的氧气氧化而变质。此类食物防腐剂应具有 (填“氧化性”或“还原性”)
科目:gzhx 来源:浙江省期末题 题型:填空题
科目:gzhx 来源: 题型:填空题
科目:gzhx 来源:江西省期末题 题型:填空题
科目:gzhx 来源: 题型:
氧化还原反应在工农业生产和日常生活中有广泛运用
(1)人通过呼吸作用吸入氧气,氧化体内的葡萄糖(C6H12O6)提供能量以维持生命活动,反应为:C6H12O6+6O2→6CO2+6H2O+能量,该反应中的还原剂是 。
(2)罐头厂在装食物罐头时,通常要添加一些对人体无害的防腐剂,防止食物被空气中的氧气氧化而变质。此类食物防腐剂应具有 。(填“氧化性”或“还原性”);
(3)铁是生物体中不可缺少的微量元素,铁在人体中是以Fe2+和Fe3+的形式存在的,而Fe2+更容易被吸收。服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中维生素C所起的作用是 。(填“氧化作用”或“还原作用”);
(4)缺铁性贫血患者应补充Fe2+,通常以硫酸亚铁的形式,而硫酸铁则无这种药效。当用硫酸亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是 。
(5)Fe3+在工业上有重要用途。例如印刷电路板是由高分子材料和铜箔复合而成,可用FeCl3溶液作“腐蚀剂”刻制印刷电路,生成CuCl2和FeCl2,写出离子方程式 。
科目:gzhx 来源:期末题 题型:填空题
科目:gzhx 来源:2008-2009学年度三亚市第一中学第一学期高一期中考试、化学试卷 题型:022
氧化还原反应在工农业生产和日常生活中有广泛运用
(1)人通过呼吸作用吸入氧气,氧化体内的葡萄糖(C6H12O6)提供能量以维持生命活动,反应为:C6H12O6+6O2→6CO2+6H2O+能量,该反应中的还原剂是________.
(2)罐头厂在装食物罐头时,通常要添加一些对人体无害的防腐剂,防止食物被空气中的氧气氧化而变质.此类食物防腐剂应具有________.(填“氧化性”或“还原性”);
(3)铁是生物体中不可缺少的微量元素,铁在人体中是以Fe2+和Fe3+的形式存在的,而Fe2+更容易被吸收.服用维生素C可使食物中的Fe3+转化为Fe2+.在这个过程中维生素C所起的作用是________.(填“氧化作用”或“还原作用”);
(4)缺铁性贫血患者应补充Fe2+,通常以硫酸亚铁的形式,而硫酸铁则无这种药效.当用硫酸亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是___________________.
(5)Fe3+在工业上有重要用途.例如印刷电路板是由高分子材料和铜箔复合而成,可用FeCl3溶液作“腐蚀剂”刻制印刷电路,生成CuCl2和FeCl2,写出离子方程式_________________.
科目:gzhx 来源: 题型:
氧化还原反应在工农业生产和日常生活中有广泛运用:
(1)人通过呼吸作用吸入氧气,氧化体内的葡萄糖(C6H12O6)提供能量以维持生命活动,反应为:C6H12O6+6O2―→6CO2+6H2O+能量,该反应中的还原剂是__________。
(2)罐头厂在装食物罐头时,通常要添加一些对人体无害的抗氧化剂,此类食物抗氧化剂,防止食物被空气中的氧气氧化而变质。此类食物添加剂应具有__________(填“氧化性”或“还原性”)。
(3)铁是生物体中不可缺少的微量元素,铁在人体中是以Fe2+和Fe3+的形式存在的,而 Fe2+更容易被吸收。服用维生素C可使食物中的 Fe3+转化为Fe2+。在这个过程中维生素C所起的作用是__________(填“氧化作用”或“还原作用”)。
科目:gzhx 来源: 题型:
科目:gzhx 来源:同步题 题型:填空题
科目:gzhx 来源:2014届贵州省高一上学期期中考试化学试卷 题型:填空题
(10分)氧化还原反应在农业生产中和日常生活中有广泛的运用。
(1)人通过呼吸作用吸入氧气,氧化体内的葡萄糖(C6H12O6),提供能量以维持生命活动,反应的化学方程式为C6H12O6+6O2→6CO2+6H2O+能量,该反应中的还原剂是 。
(2)罐头厂在装食物罐头时,通常要添加一些对人体无害的防腐剂,防止食物被空气中的氧气氧化而变质。此类食物防腐剂应具有 (填“氧化性”或“还原性”)
(3)铁是生物体中不可缺少的微量元素,铁在人体中是以Fe2+和Fe3+的形式存在的,而Fe2+更容易被吸收。服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中,维生素C所起的作用是 填“氧化作用”和“还原作用”)
(4)全世界每年有近1/10的钢铁因生锈而损失,人们常用稀硫酸除去钢铁表面的铁锈(Fe2O3),请写出除铁锈的离子方程式: ,然而这并不能解决根本问题,实质上我们应该怎样防止铁生锈,生活中通常采用 方法(符合题意一种即可)防止铁生锈。
科目:gzhx 来源: 题型:
(10分)氧化还原反应在农业生产中和日常生活中有广泛的运用。
(1)人通过呼吸作用吸入氧气,氧化体内的葡萄糖(C6H12O6),提供能量以维持生命活动,反应的化学方程式为C6H12O6+6O2→6CO2+6H2O+能量,该反应中的还原剂是 。
(2)罐头厂在装食物罐头时,通常要添加一些对人体无害的防腐剂,防止食物被空气中的氧气氧化而变质。此类食物防腐剂应具有 (填“氧化性”或“还原性”)
(3)铁是生物体中不可缺少的微量元素,铁在人体中是以Fe2+和Fe3+的形式存在的,而Fe2+更容易被吸收。服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中,维生素C所起的作用是 填“氧化作用”和“还原作用”)
(4)全世界每年有近1/10的钢铁因生锈而损失,人们常用稀硫酸除去钢铁表面的铁锈(Fe2O3),请写出除铁锈的离子方程式: ,然而这并不能解决根本问题,实质上我们应该怎样防止铁生锈,生活中通常采用 方法(符合题意一种即可)防止铁生锈。
科目:gzhx 来源:2011-2012学年贵州省凯里一中高一上学期期中考试化学试卷 题型:填空题
(10分)氧化还原反应在农业生产中和日常生活中有广泛的运用。
(1)人通过呼吸作用吸入氧气,氧化体内的葡萄糖(C6H12O6),提供能量以维持生命活动,反应的化学方程式为C6H12O6+6O2→6CO2+6H2O+能量,该反应中的还原剂是 。
(2)罐头厂在装食物罐头时,通常要添加一些对人体无害的防腐剂,防止食物被空气中的氧气氧化而变质。此类食物防腐剂应具有 (填“氧化性”或“还原性”)
(3)铁是生物体中不可缺少的微量元素,铁在人体中是以Fe2+和Fe3+的形式存在的,而Fe2+更容易被吸收。服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中,维生素C所起的作用是 填“氧化作用”和“还原作用”)
(4)全世界每年有近1/10的钢铁因生锈而损失,人们常用稀硫酸除去钢铁表面的铁锈(Fe2O3),请写出除铁锈的离子方程式: ,然而这并不能解决根本问题,实质上我们应该怎样防止铁生锈,生活中通常采用 方法(符合题意一种即可)防止铁生锈。
科目:gzhx 来源: 题型:填空题
科目:gzhx 来源:贵州省凯里一中2011-2012学年高一上学期期中考试化学试题 题型:022
氧化还原反应在农业生产中和日常生活中有广泛的运用.
(1)人通过呼吸作用吸入氧气,氧化体内的葡萄糖(C6H12O6),提供能量以维持生命活动,反应的化学方程式为C6H12O6+6O2→6CO2+6H2O+能量,该反应中的还原剂是________.
(2)罐头厂在装食物罐头时,通常要添加一些对人体无害的防腐剂,防止食物被空气中的氧气氧化而变质.此类食物防腐剂应具有________(填“氧化性”或“还原性”)
(3)铁是生物体中不可缺少的微量元素,铁在人体中是以Fe2+和Fe3+的形式存在的,而Fe2+更容易被吸收.服用维生素C可使食物中的Fe3+转化为Fe2+.在这个过程中,维生素C所起的作用是________填“氧化作用”和“还原作用”)
(4)全世界每年有近1
/10的钢铁因生锈而损失,人们常用稀硫酸除去钢铁表面的铁锈(Fe2O3),请写出除铁锈的离子方程式:________,然而这并不能解决根本问题,实质上我们应该怎样防止铁生锈,生活中通常采用________方法(符合题意一种即可)防止铁生锈.科目:gzhx 来源: 题型:
科目:gzhx 来源:2011-2012学年山东省高三上学期第二次定时练习化学试卷1 题型:实验题
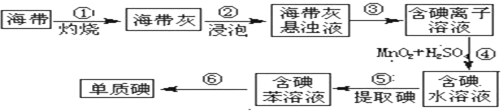
(10分)碘在工农业生产和日常生活中有重要用途。
(1)右图为海带制碘的流程图。
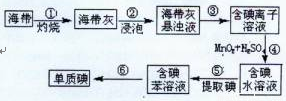
步骤③和⑤的实验操作名称分别是 、 ;
步骤④中发生反应的离子方程式为 ;
若步骤⑤采用四氯化碳来提取碘,将四氯化碳加入含碘水溶液中并振荡,观察到的现象是 。
(2)把滤纸用淀粉和碘化钾溶液浸泡,晾干后就是实验室常用的淀粉碘化钾试纸。利用淀粉碘化钾试纸可检验具有某种特性的气体。你认为淀粉碘化钾试纸用于检验具有 的气体(填序号)
A.酸性 B.碱性 C.氧化性 D.还原性
理由是 。
科目:gzhx 来源:2012-2013学年河南省开封市高三第二次质量检测理综化学试卷(解析版) 题型:填空题
氯气及其化合物在工农业生产和人类生活中都有着重要的应用。
(1)Ca(ClO)2、NaClO、NaClO2等含氯化合物都是常用的消毒剂和漂白剂是因为它们都具有__________性,请写出工业上用氯气和NaOH溶液生产消毒剂NaClO的离子方程式____________________。
(2)棕黄色强刺激性气体Cl2O为国际公认高效安全灭菌消毒剂之一,实验室可用潮湿的Cl2与Na2CO3反应制取少量Cl2O,配平并补充完整下列反应方程式:
______Cl2+_______Na2CO3+________=_______NaHCO3+____NaCl+____ Cl2O
(3)黄色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2,此反应的离子方程式为__________。
②ClO2遇浓盐酸会生成Cl2,每生成1mol Cl2转移电子的物质的量为__________。
③ClO2可将废水中的Mn2+转化为MnO2而除去,本身还原为Cl-,该反应过程中氧化剂与还原剂的物质的量之比为_________________。
(4)用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应4HCl+O2 2Cl2+2H2O,可实现氯的循环利用。
2Cl2+2H2O,可实现氯的循环利用。
已知:①上述反应中,4mol HCl被氧化放出115.6kJ的热量。
②
则断开1 mol H-O键与断开1 mol H-Cl键所需能量相差约为_________kJ,H2O中
H—O键比HC1中H—Cl键(填“强”或“弱”)__________。