
题目列表(包括答案和解析)
催化剂在科研、医药生产和电子工业等前沿领域有着广泛应用。
(1)为探究二氧化锰对氯酸钾分解的催化作用。在相同条件下,同学们按下表进行实验并记录相关数据。(其他影响实验的因素均相同)
| 编号 | KClO3质量/g | 其他物质质量/g | 待测数据 |
| 实验1 | 2.0 |
| |
| 实验2 | a | MnO2 0.5 |
① 表中a的数值应是 。
② 表中的待测数据指 (填字母序号)。
A.氧气的质量 B.反应后固体的质量
C.氧气的体积 D.单位时间内产生氧气的体积
 ③ 设计“实验1”的目的是 。
③ 设计“实验1”的目的是 。
(2)同学们继续探究二氧化锰是否参与了氯酸钾的分解反应。
氯酸钾和二氧化锰混合加热的化学方程式为:2KClO3====2KCl + 3O2↑。已知氯酸钾与二氧化锰混合加热时连续发生如下反应,试分析后按要求填空。
![]() (I) 2KClO3 + 2MnO2===2KMnO4 + Cl2↑+ O2↑;
(I) 2KClO3 + 2MnO2===2KMnO4 + Cl2↑+ O2↑;
(II) (用化学方程式表示);
![]() (III)K2MnO4 + Cl2===2KCl + MnO2 + O2↑。
(III)K2MnO4 + Cl2===2KCl + MnO2 + O2↑。
通过以上分析,同学们得出结论:二氧化锰参与了氯酸钾的分解反应。
【拓展】氟利昂释放出的氯原子参与了臭氧层的破坏,其微观示意图如下:
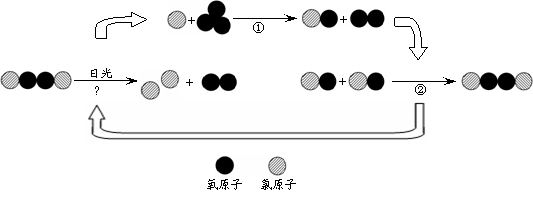 |
综合图中①②③的反应过程,写出臭氧层被破坏的化学方程式 。
催化剂在科研、医药生产和电子工业等前沿领域有着广泛应用。
(1)为探究二氧化锰对氯酸钾分解的催化作用。在相同条件下,同学们按下表进行实验并记录相关数据。(其他影响实验的因素均相同)
编号 | KClO3质量/g | 其他物质质量/g | 待测数据 |
实验1 | 2.0 |
| |
实验2 | a | MnO2 0.5 |
① 表中a的数值应是 。
② 表中的待测数据指 (填字母序号)。
A.氧气的质量 B.反应后固体的质量
C.氧气的体积 D.单位时间内产生氧气的体积
③ 设计“实验1”的目的是 。
(2)同学们继续探究二氧化锰是否参与了氯酸钾的分解反应。
氯酸钾和二氧化锰混合加热的化学方程式为:2KClO3== ==2KCl + 3O2↑。已知氯酸钾与二氧化锰混合加热时连续发生如下反应,试分析后按要求填空。
==2KCl + 3O2↑。已知氯酸钾与二氧化锰混合加热时连续发生如下反应,试分析后按要求填空。
![]() (I) 2KClO3 + 2MnO2===2KMnO4 + Cl2↑+ O2↑;
(I) 2KClO3 + 2MnO2===2KMnO4 + Cl2↑+ O2↑;
(II) (用化学方程式表示);
![]() (III)K2MnO4 + Cl2===2KCl + MnO2 + O2↑。
(III)K2MnO4 + Cl2===2KCl + MnO2 + O2↑。
通过以上分析,同学们得出结论:二氧化锰参与了氯酸钾的分解反应。
【拓展】氟利昂释放出的氯原子参与了臭氧层的破坏,其微观示意图如下:
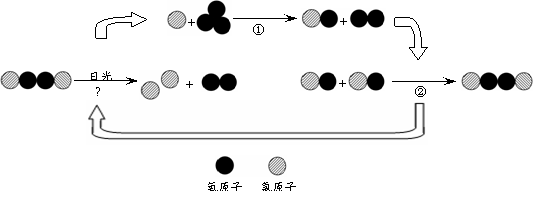 |
综合图中①②③的反应过程,写出臭氧层被破坏的化学方程式 。
催化剂在科研、医药生产和电子工业等前沿领域有着广泛应用。
(1)为探究二氧化锰对氯酸钾分解的催化作用。在相同条件下,同学们按下表进行实验并记录相关数据。(其他影响实验的因素均相同)
编号 | KClO3质量/g | 其他物质质量/g | 待测数据 |
实验1 | 2.0 |
| |
实验2 | a | MnO2 0.5 |
① 表中a的数值应是 。
② 表中的待测数据指 (填字母序号)。
A.氧气的质量 B.反应后固体的质量
C.氧气的体积 D.单位时间内产生氧气的体积
③ 设计“实验1”的目的是 。
(2)同学们继续探究二氧化锰是否参与了氯酸钾的分解反应。
氯酸钾和二氧化锰混合加热的化学方程式为:2KClO3= ===2KCl + 3O2↑。已知氯酸钾与二氧化锰混合加热时连续发生如下反应,试分析后按要求填空。
===2KCl + 3O2↑。已知氯酸钾与二氧化锰混合加热时连续发生如下反应,试分析后按要求填空。
(I) 2KClO3 + 2MnO2===2KMnO4 + Cl2↑+ O2↑;
(II) (用化学方程式表示);
(III)K2MnO4 + Cl2==![]() =2KCl + MnO2 + O2↑。
=2KCl + MnO2 + O2↑。
通过以上分析,同学们得出结论:二氧化锰参与了氯酸钾的分解反应。
【拓展】氟利昂释放出的氯原子参与了臭氧层的破坏,其微观示意图如下:
 |
综合图中①②③的反应过程,写出臭氧层被破坏的化学方程式 。
(5分)
催化剂在科研、医药生产和电子工业等前沿领域有着广泛应用。
(1)为探究二氧化锰对氯酸钾分解的催化作用。在相同条件下,同学们按下表进行实验并记录相关数据。(其他影响实验的因素均相同)
| 编号 | KClO3质量/g | 其他物质质量/g | 待测数据 |
| 实验1 | 2.0 |
|
|
| 实验2 | a | MnO2 0.5 |
|
① 表中a的数值应是 。
② 表中的待测数据指 (填字母序号)。
A.氧气的质量 B.反应后固体的质量
C.氧气的体积 D.单位时间内产生氧气的体积
 ③ 设计“实验1”的目的是 。
③ 设计“实验1”的目的是 。
(2)同学们继续探究二氧化锰是否参与了氯酸钾的分解反应。
氯酸钾和二氧化锰混合加热的化学方程式为:2KClO3====2KCl + 3O2↑。已知氯酸钾与二氧化锰混合加热时连续发生如下反应,试分析后按要求填空。
 (I)2KClO3 + 2MnO2===2KMnO4 + Cl2↑+ O2↑;
(I)2KClO3 + 2MnO2===2KMnO4 + Cl2↑+ O2↑;
(II) (用化学方程式表示);
 (III)K2MnO4 + Cl2===2KCl + MnO2 + O2↑。
(III)K2MnO4 + Cl2===2KCl + MnO2 + O2↑。
通过以上分析,同学们得出结论:二氧化锰参与了氯酸钾的分解反应。
【拓展】氟利昂释放出的氯原子参与了臭氧层的破坏,其微观示意图如下:
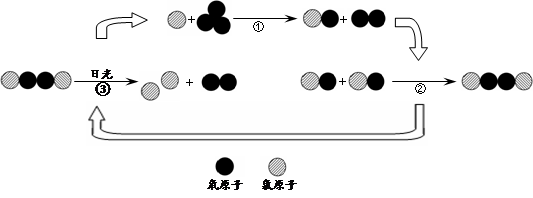
综合图中①②③的反应过程,写出臭氧层被破坏的化学方程式
(5分)
催化剂在科研、医药生产和电子工业等前沿领域有着广泛应用。
(1)为探究二氧化锰对氯酸钾分解的催化作用。在相同条件下,同学们按下表进行实验并记录相关数据。(其他影响实验的因素均相同)
|
编号 |
KClO3质量/g |
其他物质质量/g |
待测数据 |
|
实验1 |
2.0 |
|
|
|
实验2 |
a |
MnO2 0.5 |
|
① 表中a的数值应是 。
② 表中的待测数据指 (填字母序号)。
A.氧气的质量 B.反应后固体的质量
C.氧气的体积 D.单位时间内产生氧气的体积
 ③ 设计“实验1”的目的是 。
③ 设计“实验1”的目的是 。
(2)同学们继续探究二氧化锰是否参与了氯酸钾的分解反应。
氯酸钾和二氧化锰混合加热的化学方程式为:2KClO3====2KCl + 3O2↑。已知氯酸钾与二氧化锰混合加热时连续发生如下反应,试分析后按要求填空。
 (I)
2KClO3 + 2MnO2===2KMnO4 + Cl2↑+ O2↑;
(I)
2KClO3 + 2MnO2===2KMnO4 + Cl2↑+ O2↑;
(II) (用化学方程式表示);
 (III)K2MnO4 + Cl2===2KCl + MnO2 + O2↑。
(III)K2MnO4 + Cl2===2KCl + MnO2 + O2↑。
通过以上分析,同学们得出结论:二氧化锰参与了氯酸钾的分解反应。
【拓展】氟利昂释放出的氯原子参与了臭氧层的破坏,其微观示意图如下:
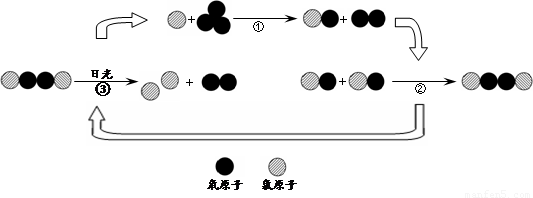
综合图中①②③的反应过程,写出臭氧层被破坏的化学方程式
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com