Θ®2006?ΤήœΦ«χ»ΐΡΘΘ©Μ·―ß Β―ι “ΒΡΩΣΖ≈»’Θ§άœ ΠΑ≤≈≈Μ·―ß–Υ»Λ–ΓΉιΒΡΆ§―ßΩΣ’ΙΝΥ”–ΙΊNaClΚΆNa
2CO
3’βΝΫ÷÷≥ΘΦϊΒΡ―ΈΒΡ Β―ιΘ§ Β―ι»ΈΈώ»γœ¬ΘΚ

ΒΎ“Μ–ΓΉιΒΡΆ§―ßΘΚΫΪ ß»Ξ±ξ«©ΒΡΝΫΤΩΈό…Ϊ»ή“ΚΘ®Ζ÷±πΈΣNaClΚΆNa
2CO
3Θ©«χ±πΩΣά¥
ΒΎΕΰ–ΓΉιΒΡΆ§―ßΘΚ≥ΐ»ΞNaClΙΧΧε÷–ΒΡ…ΌΝΩNa
2CO
3ΒΎ»ΐ–ΓΉιΒΡΆ§―ßΘΚ≤βΕ®Na
2CO
3ΚΆ…ΌΝΩNaClΒΡΙΧΧεΜλΚœΈο÷–Na
2CO
3÷ ΝΩΖ÷ ΐ
Θ®1Θ©ΒΎ“Μ–ΓΉιΒΡΆ§―ßΈΣΝΥ«χ±πΝΫΤΩΈό…Ϊ»ή“ΚΘ§ΦΉΓΔ““ΓΔ±ϊΓΔΕΓΥΡΈΜΆ§―ßΖ÷±π―Γ‘ώœ¬Ν–Έο÷ Ϋχ–– Β―ιΘ°Τδ÷–ΚœάμΒΡ «
ΦΉΓΔ±ϊ
ΦΉΓΔ±ϊ
Θ®Χν–¥–ρΚ≈Θ©Θ°
ΦΉΘΚœΓ―ΈΥα ““ΘΚAgNO
3»ή“Κ ±ϊΘΚ≥Έ«ε ·Μ“Υ° ΕΓΘΚάΕ…ΪΒΡ ·»ο ‘÷Ϋ
Θ®2Θ©ΒΎΕΰ–ΓΉιΈΣΝΥ≥ΐ»ΞNaCl»ή“Κ÷–ΒΡ…ΌΝΩNa
2CO
3Θ§…ηΦΤΝΥ»γœ¬ΒΡ Β―ιΘΚ
«κΜΊ¥πœ¬Ν–Έ ΧβΘΚ
ΔΌ–¥≥ω≥ΝΒμAΒΡΜ·―ß Ϋ
CaCO3
CaCO3
ΘΜΔΎΦΉΆ§―ß»œΈΣΘΚΦ”»κCaCl
2»ή“ΚΚσΘ§Ζ÷άκ≥ΐ»Ξ≥ΝΒμAΒΡ Β―ι≤ΌΉςΖΫΖ® «
Ιΐ¬Υ
Ιΐ¬Υ
ΘΜΔέ““Ά§―ßΖΔœ÷¥ΥΖΫΑΗΚή»ί“Ή“ΐ»κ–¬ΒΡ‘”÷ Θ§ΥϊΟ«Χα≥ω–¬ΒΡΖΫΑΗΘΚΫΪΜλΚœΈο»ήΫβΘ§»τΒΈΦ”―ΈΥα÷Ν≤Μ‘Ό≤ζ…ζΤχΧεΈΣ÷ΙΘ§‘ρΦ»Ρή≥ΐ»ΞNa
2CO
3‘”÷ Θ§”÷Ρή”––ßΒΊΖά÷Ι–¬‘”÷ ΒΡ“ΐ»κΘ°–¥≥ω”–ΙΊΖ¥”ΠΒΡΖΫ≥Χ Ϋ
Na2CO3+2HCl®T2NaCl+H2O+CO2Γϋ
Na2CO3+2HCl®T2NaCl+H2O+CO2Γϋ
Θ°
Θ®3Θ©ΒΎ»ΐ–ΓΉιΒΡΆ§―ßΗυΨίœ¬Ν–ΥυΗχ≥ωΒΡ“©ΤΖΓΔ Β―ιΉΑ÷ΟΚΆ Β―ι÷–Ω…≤βΒΟΒΡ ΐΨίΘ§…ηΦΤ Β―ιά¥¥÷¬‘≤βΕ®Na
2CO
3ΚΆNaClΒΡΙΧΧεΜλΚœΈοag÷–Na
2CO
3ΒΡ÷ ΝΩΖ÷ ΐΘ°
“©ΤΖΘΚΉψΝΩΒΡœΓH
2SO
4ΓΔCaCl
2»ή“ΚΓΔΦν ·Μ“Θ®…’ΦνΚΆ―θΜ·ΗΤΒΡΜλΚœΈοΘ©ΓΔ≈®ΝρΥα
Β―ιΉΑ÷Ο»γΆΦ2ΘΚ
‘Ύ Β―ι÷–Ω…≤βΒΟΒΡ ΐΨίΘΚΔΌ≥δΖ÷Ζ¥”ΠΚσΘ§…ζ≥…≥ΝΒμΒΡ÷ ΝΩΈΣbgΘΜ ΔΎΖ¥”Π«ΑΉΑ÷ΟΚΆ“©ΤΖΒΡ÷ ΝΩΈΣc gΘΜΔέ≥δΖ÷Ζ¥”ΠΚσΉΑ÷ΟΚΆ“©ΤΖΒΡ÷ ΝΩΈΣd gΘ°
«κ…ηΦΤΕΰΗω Β―ιΖΫΑΗΧν»κœ¬±μ÷–Θ®Φν ·Μ“ΚΆ≈®ΝρΥα“―±Μ―Γ”ΟΘ§œ¬±μ÷–≤Μ‘ΌΧν–¥Θ©ΘΚ
| ΖΫΑΗ |
―Γ”ΟΒΡ“©ΤΖ |
―Γ”ΟΒΡ Β―ιΉΑ÷ΟΦΑΉιΉΑ ±Ϋ”ΩΎΝ§Ϋ”Υ≥–ρ |
–η≤βΒΟΒΡ Β―ι ΐΨίΘ®¥”…œ ωΩ…≤βΒΟΒΡ ΐΨί÷–―Γ»ΓΘ© |
ΜλΚœΈο÷–Na2CO3ΒΡ÷ ΝΩΖ÷ ΐΦΤΥψ Ϋ |
| ―Γ”ΟΒΡ Β―ιΉΑ÷Ο–ρΚ≈ |
ΉιΉΑ ±Ϋ”ΩΎ±ύΚ≈Υ≥–ρ |
| “Μ |
CaCl2»ή“Κ CaCl2»ή“Κ |
AΓΔBΓΔDΓΔF |
Θ®Έψ–κΧν–¥Θ© |
agΓΔbg agΓΔbg |
|
| Εΰ |
œΓH2SO4 œΓH2SO4 |
AΓΔCΓΔE AΓΔCΓΔE |
ΔΌΔήΔίΔΎΔέ ΔΌΔήΔίΔΎΔέ |
agΓΔcgΓΔdg |
|

![]() »ΐ÷÷Έό…Ϊ»ή“Κ”Π―Γ”ΟΘ® Θ©
»ΐ÷÷Έό…Ϊ»ή“Κ”Π―Γ”ΟΘ® Θ©![]() »ή“Κ B.
»ή“Κ B. ![]() »ή“Κ C. œΓ
»ή“Κ C. œΓ![]() D. œΓ
D. œΓ![]()
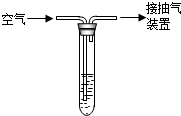 ΝρΜρΚ§ΝρΈο÷ ‘ΎΩ’Τχ÷–»Φ…’…ζ≥…SO2Θ§SO2 «“Μ÷÷Έό…ΪΓΔ”–¥ΧΦΛ–‘ΤχΈΕΒΡ”–ΕΨΤχΧεΘ°
ΝρΜρΚ§ΝρΈο÷ ‘ΎΩ’Τχ÷–»Φ…’…ζ≥…SO2Θ§SO2 «“Μ÷÷Έό…ΪΓΔ”–¥ΧΦΛ–‘ΤχΈΕΒΡ”–ΕΨΤχΧεΘ°