
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)


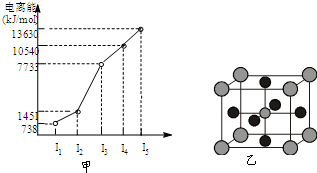 ”–XΓΔYΓΔZΓΔWΥΡ÷÷‘ΣΥΊΘ§‘≠Ή”–ρ ΐ“ά¥ΈΦθ–ΓΘ°“―÷ΣX «ΒΎΥΡ÷ήΤΎΒΡ÷ςΉε‘ΣΥΊΘ§Τδ≤ΩΖ÷ΒγάκΡή»γΆΦΦΉΥυ ΨΘΜXΓΔY‘ΣΥΊΨΏ”–œύΆ§ΒΡΉνΗΏ’ΐΜ·ΚœΦέΘΜZ ‘≠Ή”pΙλΒάΙ≤”–3ΗωΒγΉ”ΘΜW‘≠Ή”ΦέΒγΉ”≈≈≤Φ ΫΈΣnsnnpnΘ°
”–XΓΔYΓΔZΓΔWΥΡ÷÷‘ΣΥΊΘ§‘≠Ή”–ρ ΐ“ά¥ΈΦθ–ΓΘ°“―÷ΣX «ΒΎΥΡ÷ήΤΎΒΡ÷ςΉε‘ΣΥΊΘ§Τδ≤ΩΖ÷ΒγάκΡή»γΆΦΦΉΥυ ΨΘΜXΓΔY‘ΣΥΊΨΏ”–œύΆ§ΒΡΉνΗΏ’ΐΜ·ΚœΦέΘΜZ ‘≠Ή”pΙλΒάΙ≤”–3ΗωΒγΉ”ΘΜW‘≠Ή”ΦέΒγΉ”≈≈≤Φ ΫΈΣnsnnpnΘ°‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΒΡΥΡ÷÷‘ΣΥΊAΓΔBΓΔCΓΔDΖ÷±π¥Π”ΎΒΎ“Μ÷ΝΒΎΥΡ÷ήΤΎΘ§Τδ÷–A‘≠Ή”ΚΥ «“ΜΗω÷ Ή”ΘΜB‘≠Ή”ΚΥΆβΒγΉ””–6÷÷≤ΜΆ§ΒΡ‘ΥΕ·Ή¥Χ§Θ§B”κCΩ…–Έ≥…’ΐΥΡΟφΧε–ΆΖ÷Ή”Θ§D‘≠Ή”ΆβΈßΒγΉ”≈≈≤ΦΈΣ3d104s1ΓΘ «κΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©’βΥΡ÷÷‘ΣΥΊ÷–ΒγΗΚ–‘Ήν¥σΒΡ « (Χν‘ΣΥΊΖϊΚ≈)ΓΔΒΎ“ΜΒγάκΡήΉν–ΓΒΡ « (Χν‘ΣΥΊΖϊΚ≈)ΘΜ
Θ®2Θ©CΥυ‘ΎΒΡ÷ςΉε‘ΣΥΊΤχΧ§«βΜ·Έο÷–Θ§Ζ–ΒψΉνΒΆΒΡ « (ΧνΜ·―ß Ϋ)ΘΜ
Θ®3Θ©B‘ΣΥΊΩ…–Έ≥…Εύ÷÷ΒΞ÷ Θ§Τδ÷–ΓΑ÷Μ”–“Μ≤ψ‘≠Ή”ΚώΓ±ΒΡΈο÷ Θ§±ΜΙΪ»œΈΣΡΩ«Α άΫγ…œ“―÷ΣΒΡΉν±ΓΓΔΉνΦα”≤ΓΔ¥ΪΒΦΒγΉ”ΥΌΕ»ΉνΩλΒΡ–¬–Ά≤ΡΝœΘ§ΗΟ≤ΡΝœΨßΧεΫαΙΙ»γΆΦΥυ ΨΘ§Τδ‘≠Ή”ΒΡ‘”Μ·άύ–ΆΈΣ ΘΜ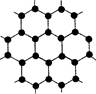
Θ®4Θ©DΒΡ¥ΉΥα―ΈΨßΧεΨ÷≤ΩΫαΙΙ»γ”“ΆΦΘ§ΗΟΨßΧε÷–Κ§”–ΒΡΜ·―ßΦϋ « (Χν―Γœν–ρΚ≈)ΘΜ
ΔΌΦΪ–‘Φϋ ΔΎΖ«ΦΪ–‘Φϋ Δέ≈δΈΜΦϋ ΔήΫπ τΦϋ
Θ®5Θ©Ρ≥―ß…ζΥυΉωΒΡ”–ΙΊD‘ΣΥΊΒΡ Β―ιΝς≥Χ»γœ¬ΆΦΘΚ
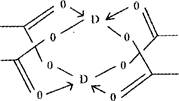
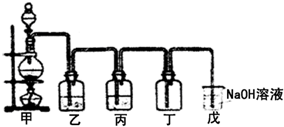
ΒΎΔΌ≤Ϋ≤ζ…ζΒΡΉΊ…ΪΒΡ―Χ τ”Ύ (Χν“Μ÷÷Ζ÷…ΔœΒ)Θ§»γΒΎΔΎ≤ΫΦ”¥σΝΩΥ°Θ§»ή“Κ≥ …ΪΘ§
–¥≥ωΒΎΔί≤ΫΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΘΚ ΓΘ
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com