
题目列表(包括答案和解析)
| 族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 2 | 3Li 锂 69.41 |
4Be 铍?90.12 |
5B?硼?10.81 | 6C?碳?1201 | 7N?氮?14.01 | 8O?氧?16.00 | 9F? 氟?19.00 |
10Ne?氖?20.18 |
| 3 | 11Na?钠?22.99 | 12Mg?镁?24.31 | 13Al?铝?26.98 | 14Si?硅?28.09 | 15P?磷?30.97 | 16S?硫?32.06 | 17Cl?氯?35.45 | 18Ar?氩?39.95 |
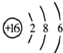 ,该元素的原子核外有
,该元素的原子核外有(12分)实验室用98%的浓硫酸配制成稀硫酸,并与锌粒反应制取氢气。
(1)查阅资料。
20℃时不同质量分数硫酸的密度(g/mL)
| 质量 分数 | 0% (纯水) | 1% | 4% | 10% | 16% | 24% | 32% | 36% | 44% | 49% | 60% | 98% |
| 密度 | 1.00 | 1.01 | 1.02 | 1.07 | 1.11 | 1.17 | 1.24 | 1.27 | 1.34 | 1.39 | 1.50 | 1.84 |
分析以上数据,可以得出结论(写2条)
① ;
② ;
(2)计算。配制200g24.5%的稀硫酸,需 g98%浓硫酸和 g水。实际操作时,取98%浓硫酸 mL(精确到1mL);
(3)配制稀硫酸。分别用量筒量取所需水和浓硫酸,先将 倒入烧杯中,然后
;
(4)制取氢气。
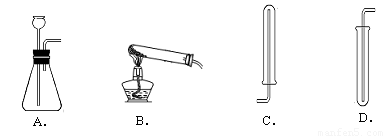
①下图中可用于制取、收集氢气的装置是(填字母) ;
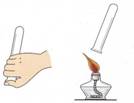
②检验氢气纯度的方法如图所示,标明氢气不纯的现象是 。
(12分)实验室用98%的浓硫酸配制成稀硫酸,并与锌粒反应制取氢气。
(1)查阅资料。
20℃时不同质量分数硫酸的密度(g/mL)
|
质量 分数 |
0% (纯水) |
1% |
4% |
10% |
16% |
24% |
32% |
36% |
44% |
49% |
60% |
98% |
|
密度 |
1.00 |
1.01 |
1.02 |
1.07 |
1.11 |
1.17 |
1.24 |
1.27 |
1.34 |
1.39 |
1.50 |
1.84 |
分析以上数据,可以得出结论(写2条)
① ;
② ;
(2)计算。配制200g24.5%的稀硫酸,需 g98%浓硫酸和 g水。实际操作时,取98%浓硫酸 mL(精确到1mL);
(3)配制稀硫酸。分别用量筒量取所需水和浓硫酸,先将 倒入烧杯中,然后
;
(4)制取氢气。
①下图中可用于制取、收集氢气的装置是(填字母) ;
②检验氢气纯度的方法如图所示,标明氢气不纯的现象是 。
| 族/周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 第二 周期 |
3 Li 锂 6.941 |
4 Be 铍 9.012 |
5 B 硼 10.8l |
① | 7 N 氮 14.0l |
8 O 氧 16.00 |
9 F 氟 19.00 |
10 Ne 氖 20.18 |
| 第三 周期 |
11 Na 钠 22.99 |
② 24.31 |
13 Al 铝 26.98 |
14 Si 硅 28.09 |
③ 30.97 |
16 S 硫 32.06 |
17 Cl 氯 35.45 |
18 Ar 氩 39.95 |


| 族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 2 | 3 Li 锂 6.941 |
4 Be 铍? 9.012 |
5 B? 硼? 10.81 |
6 C? 碳? 12.01 |
7 N? 氮? 14.01 |
8 O? 氧? 16.00 |
9 F? 氟? 19.00 |
10Ne? 氖? 20.18 |
| 3 | 11Na 钠?22.99 |
12Mg 镁?24.31 |
13 Al 铝?26.98 |
14 Si 硅?28.09 |
15 P? 磷?30.97 |
16 S? 硫?32.06 |
17 Cl? 氯?35.45 |
18 Ar? 氩?39.95 |
 所表示的粒子符号为
所表示的粒子符号为湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com