
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
ЈЁ2009?ұҰЫжЗш¶юДЈЈ©ПВұнЦР¶ФУР№ШЦчМвЦӘК¶өД№йДЙЈ¬УРҙнОуөДТ»ЧйКЗЈЁЎЎЎЎЈ©
|
19ЎўПВБРЛө·ЁЦРЈ¬І»ХэИ·өДКЗЈЁЎЎЎЎЈ©
|
ИЬТәҫЯУР№г·әөДУГНҫЈ¬ёщҫЭИЬТәУР№ШЦӘК¶Ј¬»ШҙрПВБРОКМвЈә
ЈЁ1Ј©ФЪ20ЎжКұЈ¬ПтКўУР40gВИ»ҜДЖ№ММеөДЙХұӯЦРјУИл100gЛ®Ј¬ід·ЦҪБ°иәуЈ¬ИФУР4g№ММеОҙИЬҪвЈ®
ўЩЛщөГИЬТәКЗ20ЎжКұВИ»ҜДЖөДЎЎЎЎ ИЬТәЈЁМоЎ°ұҘәНЎұ»тЎ°І»ұҘәНЎұЈ©
ўЪ20ЎжКұЈ¬ВИ»ҜДЖөДИЬҪв¶ИОӘЎЎЎЎ gЈ®
ЈЁ2Ј©ПЦУГЦКБҝ·ЦКэОӘ12%өДВИ»ҜДЖИЬТәЈЁГЬ¶ИФјОӘ1.09g/cm3Ј©Ј¬ЕдЦЖ20gЦКБҝ·ЦКэОӘ6%өДВИ»ҜДЖИЬТәЈ®
ўЩРиТӘЦКБҝ·ЦКэОӘ12%өДВИ»ҜДЖИЬТәЎЎЎЎ mLЈЁјЖЛгҪб№ыҫ«И·өҪ0.1Ј©Ј¬РиТӘЛ®ЎЎЎЎ ЎЎmLЈЁЛ®өДГЬ¶ИОӘ1g/cm3Ј©Ј®
ўЪёГИЬТәЕдЦЖ№эіМЦРУГөҪөДТЗЖчіэБЛБҝНІЎўЙХұӯІЈБ§°фНвЈ¬»№РиТӘЎЎЎЎЎЎ ЎЎБҝИЎЛщРиТӘөД12%өДВИ»ҜДЖИЬТәКұЈ¬УҰСЎУГЎЎЎЎЎЎ ЎЎЈЁМоЎ°10mLЎұ»тЎ°20mLЎұ»тЎ°50mLЎұЈ©№жёсөДБҝНІЈ®
ўЫ°СЕдЦЖәГөДЙПКцИЬТәЧ°ИлЎЎЎЎ ЎЎЦРЈЁМоЎ°№гҝЪЖҝЎұ»тЎ°ПёҝЪЖҝЎұЈ©Ј¬ёЗәГЖҝИыІўМщЙПұкЗ©Ј®
ФЪС§П°ЛбәНјоөДЦӘК¶КұЈ¬НхАПКҰҪ«јёҝйЗвСх»ҜДЖ·ЕФЪұнГжГуЦРЈ¬·ЕЦГФЪҪМКТөДіч№сАпЈ¬№эБЛјёМмЈ¬ұнГжГуЦРҝйЧҙ№ММеіцПЦБЛРн¶а°ЧЙ«·ЫД©Ј¬Н¬С§ГЗҫНҙЛХ№ҝӘМҪҫҝЈ®
ЈЁ1Ј©РЎҪЬІВПл·ЫД©КЗМјЛбДЖЈ¬ФӯТтөД»ҜС§·ҪіМКҪКЗЎЎ Ј®
ЈЁ2Ј©РЎцОУГБҪЦЦІ»Н¬АаұрөДОпЦКјмСйіцБЛМјЛбДЖөДҙжФЪЈ¬ЛыСЎУГөДКФјБКЗЎЎ әНЎЎ ЎЎЈ®
ЈЁ3Ј©РЎФҙИЎЙЩБҝ№ММеСщЖ·Ј¬ЕдіЙИЬТәјУИлОЮЙ«·УМӘАҙјмСйЈ¬·ўПЦИЬТәұдәмЙ«Ј¬ЛөГчИЬТәЦРТ»¶ЁҙжФЪөДОпЦККЗЎЎ ЎЎЈЁМо»ҜС§КҪЈ©
ЈЁ4Ј©ПІ»¶¶ҜКЦөДЧіЧіН¬С§ЙијЖіцБЛКөСйЧ°ЦГИзНјЛщКҫЈ®КөСйКұПтКФ№ЬАпөДЛ®ЦРјУИл№ММеЗвСх»ҜДЖәуЈ¬ФӯАҙUРО№ЬДЪБҪұЫФЪН¬Т»Л®ЖҪГжЙПөДәмД«Л®Ј¬УТГжТәГжҪ«ЎЎ ЎЎЈ®ЈЁМоЎ°ЙПЙэЎұ»тЎ°ПВҪөЎұЈ©ФӯТтКЗЎЎ Ј®Из№ыТӘ№ЫІмөҪПа·ҙөДПЦПуЈ¬ҝЙТФПтЛ®ЦРјУИлЎЎ Ј®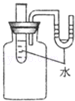
ЈЁ5Ј©73gЦКБҝ·ЦКэОӘ20%өДСОЛбУл127gЗвСх»ҜДЖИЬТәЗЎәГНкИ«ЦРәНЈ¬јЖЛгЛщөГИЬТәЦРИЬЦКөДЦКБҝ·ЦКэЈҝ
 С§№эҪрКфөД»о¶ҜРФЛіРтТФәуЈ¬ГчГчН¬С§¶ФЖдТ»ПөБРЦӘК¶ҪшРРБЛСРҫҝЈ®
С§№эҪрКфөД»о¶ҜРФЛіРтТФәуЈ¬ГчГчН¬С§¶ФЖдТ»ПөБРЦӘК¶ҪшРРБЛСРҫҝЈ®| XСОИЬТә | YСОИЬТә | ZСОИЬТә | |
| Ni | ОЮ | ОЮ | УР |
| Mn | ОЮ | УР | УР |
№ъјКѧУУЕСЎ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com