
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
 Θ®2012?ΡœΆ®ΡΘΡβΘ©»γΆΦΥυ ΨΘ§ΗτΑεIΙΧΕ®≤ΜΕ·Θ§Μν»ϊΔρΩ…Ή‘”…“ΤΕ·Θ§MΓΔNΝΫΗω»ίΤς÷–ΨυΖΔ…ζΖ¥”ΠΘΚAΘ®gΘ©+3BΘ®gΘ©?2CΘ®gΘ©ΓςH=-192kJ?mol-1Θ°œρMΓΔN÷–Θ§ΕΦΆ®»κx mol AΚΆy mol BΒΡΜλΚœΤχΧεΘ§≥θ ΦMΓΔN»ίΜΐœύΆ§Θ§±Θ≥÷Έ¬Ε»≤Μ±δΘ°œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©
Θ®2012?ΡœΆ®ΡΘΡβΘ©»γΆΦΥυ ΨΘ§ΗτΑεIΙΧΕ®≤ΜΕ·Θ§Μν»ϊΔρΩ…Ή‘”…“ΤΕ·Θ§MΓΔNΝΫΗω»ίΤς÷–ΨυΖΔ…ζΖ¥”ΠΘΚAΘ®gΘ©+3BΘ®gΘ©?2CΘ®gΘ©ΓςH=-192kJ?mol-1Θ°œρMΓΔN÷–Θ§ΕΦΆ®»κx mol AΚΆy mol BΒΡΜλΚœΤχΧεΘ§≥θ ΦMΓΔN»ίΜΐœύΆ§Θ§±Θ≥÷Έ¬Ε»≤Μ±δΘ°œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©Ρ≥Ά§―ß”ΟNaHCO3ΚΆKHCO3Ήι≥…ΒΡΜλΚœΈοΫχ–– Β―ιΘ§≤βΒΟ»γœ¬ ΐΨί(―ΈΥαΒΡΈο÷ ΒΡΝΩ≈®Ε»œύΒ»)Θ§‘ρœ¬Ν–Ζ÷ΈωΆΤάμ÷–≤Μ’ΐ»ΖΒΡ «(ΓΓΓΓ)
|
| 50 mL―ΈΥα | 50 mL―ΈΥα | 50 mL―ΈΥα |
| m(ΜλΚœΈο) | 9.2 g | 15.7 g | 27.6 g |
| V(CO2)(±ξΉΦΉ¥Ωω) | 2.24 L | 3.36 L | 3.36 L |
A.―ΈΥαΒΡΈο÷ ΒΡΝΩ≈®Ε»ΈΣ3.0molΓΛLΘ≠1 BΘ°ΗυΨί±μ÷– ΐΨίΡήΦΤΥψ≥ωΜλΚœΈο÷–NaHCO3ΒΡ÷ ΝΩΖ÷ ΐ
CΘ°Φ”»κΜλΚœΈο9.2 g ±―ΈΥαΙΐΝΩ DΘ°15.7 gΜλΚœΈο«ΓΚΟ”κ―ΈΥαΆξ»ΪΖ¥”Π
Ρ≥Ά§―ß”ΟNaHCO3ΚΆKHCO3Ήι≥…ΒΡΜλΚœΈοΫχ–– Β―ιΘ§≤βΒΟ»γœ¬ ΐΨί(―ΈΥαΒΡΈο÷ ΒΡΝΩ≈®Ε»œύΒ»)Θ§‘ρœ¬Ν–Ζ÷ΈωΆΤάμ÷–≤Μ’ΐ»ΖΒΡ «(ΓΓΓΓ)
|
|
50 mL―ΈΥα |
50 mL―ΈΥα |
50 mL―ΈΥα |
|
m(ΜλΚœΈο) |
9.2 g |
15.7 g |
27.6 g |
|
V(CO2)(±ξΉΦΉ¥Ωω) |
2.24 L |
3.36 L |
3.36 L |
A.―ΈΥαΒΡΈο÷ ΒΡΝΩ≈®Ε»ΈΣ3.0 molΓΛLΘ≠1 BΘ°ΗυΨί±μ÷– ΐΨίΡήΦΤΥψ≥ωΜλΚœΈο÷–NaHCO3ΒΡ÷ ΝΩΖ÷ ΐ
CΘ°Φ”»κΜλΚœΈο9.2 g ±―ΈΥαΙΐΝΩ DΘ°15.7 gΜλΚœΈο«ΓΚΟ”κ―ΈΥαΆξ»ΪΖ¥”Π
Θ®16Ζ÷Θ©œ¬±μ «‘ΣΥΊ÷ήΤΎ±μΒΡ“Μ≤ΩΖ÷Θ§’κΕ‘±μ÷–”ΟΉ÷ΡΗ±ξ≥ωΒΡ‘ΣΥΊΘ§ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®≥ΐΧΊ±πΉΔΟςΆβΘ§ΤδΥϋ“Μ¬…”ΟΜ·―ß Ϋ±μ ΨΘ©
| A | | | |||||||||||||||
| | | | | W | T | M | | | |||||||||
| B | D | | Z | J | L | U | V | R | |||||||||
| X | E | | | | | | Y | | | G | | | | | | Q | |
Θ®15Ζ÷Θ©¬»Μ·Χζ «≥ΘΦϊΒΡΥ°¥ΠάμΦΝΘ§ΈόΥ°FeCl3ΒΡ»έΒψΈΣ555KΓΔΖ–ΒψΈΣ588KΓΘΙΛ“Β…œ÷Τ±ΗΈόΥ°FeCl3ΒΡ“Μ÷÷ΙΛ“’»γœ¬ΘΚ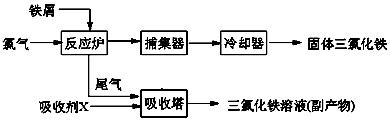
Θ®1Θ© ‘–¥≥ωΈϋ ’Υΰ÷–Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΘΚ____________________________ΓΘ
Θ®2Θ©“―÷ΣΝυΥ°Κœ¬»Μ·Χζ‘ΎΥ°÷–ΒΡ»ήΫβΕ»»γœ¬ΘΚ
| Έ¬Ε»/Γφ | 0 | 10 | 20 | 30 | 50 | 80 | 100 |
| »ήΫβΕ»(g/100gH20) | 74.4 | 81.9 | 91.8 | 106.8 | 315.1 | 525.8 | 535.7 |
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com